Clear Sky Science · ru
Влияние длины алкильной цепи на ингибирующую коррозию эффективность производных 2-тиоксо-2,3-дигидрохиназолин-4(1H)-она для углеродистой стали в растворе HCl
Защита повседневных металлов от скрытого повреждения
От мостов и зданий до автомобилей и бытовой техники — углеродистая сталь тихо поддерживает большую часть современной инфраструктуры. Но у этого основного материала есть уязвимость: в кислых средах, например при промывке промышленного оборудования или в процессах нефтегазовой отрасли, он может растворяться гораздо быстрее, чем ожидают. В этом исследовании изучается, способны ли два небольших, простых в синтезе органических соединения действовать как невидимые щиты для стали, замедляя это тихое разрушение и продлевая срок службы важной инфраструктуры.
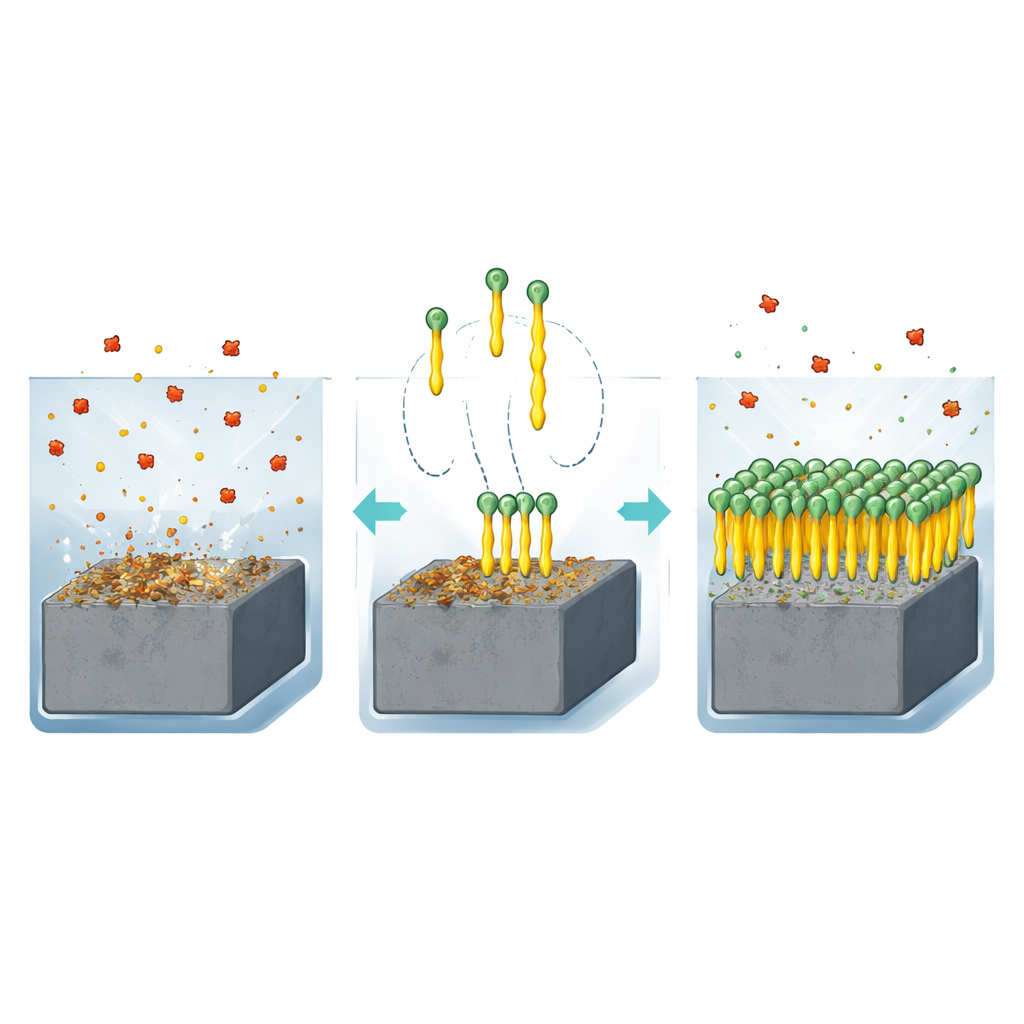
Почему стали нужен химический телохранитель
Когда углеродистая сталь находится в кислой жидкости, такой как соляная кислота, атомы на её поверхности реагируют и переходят в раствор. Со временем эта коррозия может истончать трубы, ослаблять резервуары и ставить под угрозу безопасность. Один из самых практичных способов бороться с этим — вносить в раствор очень малые количества специальных молекул, называемых ингибиторами. Эти молекулы присоединяются к поверхности стали и образуют защитную пленку, которая препятствует дальнейшей атаке. Авторы сосредоточились на семействе соединений, известных как хиназолиноны, содержащих азот, серу и кислород, которые могут прочно притягиваться к металлу. Они сконструировали две очень простые версии, отличающиеся только длиной одной углеродной цепи: короткой метильной группой (Q‑C1) и более длинной бутильной группой (Q‑C4).
Испытание двух небольших молекул в роли щитов для стали
Чтобы оценить, насколько хорошо эти соединения защищают сталь, исследователи погружали образцы углеродистой стали в концентрированную соляную кислоту с ингибиторами и без них. Тщательно взвешивая образцы до и после выдержки, они могли определить, сколько металла растворилось. Также были использованы электрокхимические методы, отслеживающие, насколько легко электрический заряд проходит через границу металл–раствор, что даёт чувствительную оценку скорости коррозии. В широком диапазоне концентраций обе молекулы заметно снизили потерю стали, при этом более длинноцепочечный Q‑C4 достигал почти 89% защиты в оптимальных условиях. Однако защитный эффект ослабевал при повышенных температурах, что указывает на то, что ингибирующая пленка становится менее стабильной по мере того, как тепло способствует отрыванию молекул от поверхности.
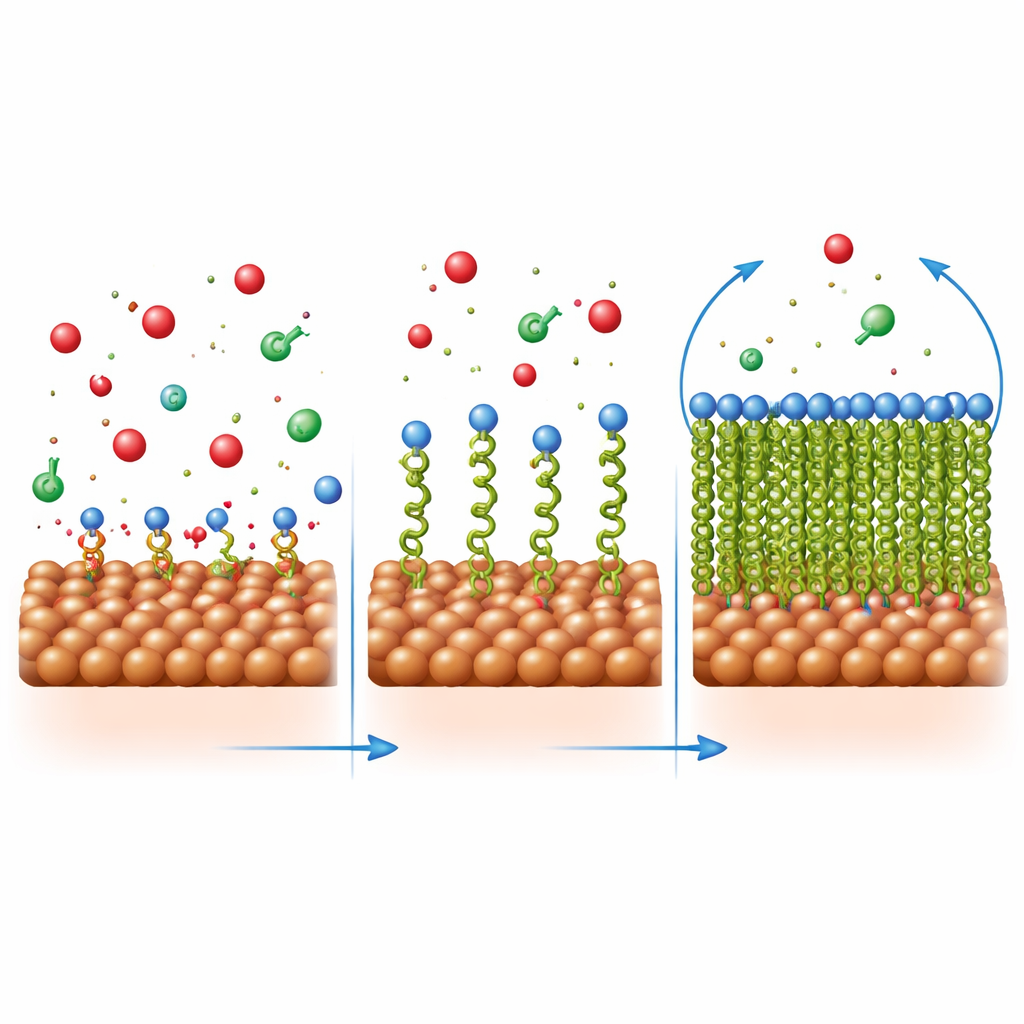
Как формируется и удерживается защитная пленка
Исследователи изучили, как эти молекулы располагаются на стали, анализируя зависимость покрытия от концентрации. Поведение соответствовало простой модели «одного слоя», то есть каждая молекула ингибитора занимает своё место на поверхности, а не накапливается в толстые слои. Расчёты изменений энергии показали, что присоединение включает как физическое притяжение (за счёт зарядовых взаимодействий), так и химическую связь (за счёт совместного использования электронов с металлом). Микроскопические изображения подтвердили эту картину: голая сталь в кислоте имела каверны и трещины, тогда как сталь в ингибированном растворе выглядела гораздо более гладкой и покрытой равномерным слоем. Элементный анализ и инфракрасная спектроскопия подтвердили присутствие органических молекул на поверхности стали и то, что их функциональные группы взаимодействовали с атомами железа.
Почему более длинная цепь работает лучше
Хотя обе молекулы имеют одинаковую «головку», которая захватывает сталь, их «хвосты» ведут себя по-разному. Более длинная бутильная цепь в Q‑C4 более гидрофобна, чем короткая метильная в Q‑C1. После того как головка закрепляется на металле, этот хвост способствует формированию более плотной и цельной плёнки, которая держит кислотный раствор на расстоянии. Компьютерные моделирования на основе теории функционала плотности подтвердили это: по расчётам Q‑C4 обладает немного большей способностью отдавать электроны и более «мягкой» электронной структурой, что способствует более сильному взаимодействию с металлом. В совокупности эти свойства помогают Q‑C4 компактнее упаковываться и создавать более эффективный барьер, оставляя меньше открытых участков, где может начаться коррозия.
Что это значит для реальной защиты стали
Проще говоря, исследование показывает, что очень простые и недорогие органические молекулы могут обеспечить значительную защиту углеродистой стали в агрессивных кислых средах, и что даже такая скромная модификация, как длина углеродной цепи, может заметно повлиять на эффективность. Ингибитор с более длинным хвостом формирует более плотное и стойкое покрытие, существенно уменьшая коррозию по сравнению с его короткоцепочечным аналогом. Несмотря на то, что защита снижается при повышенной температуре, работа даёт ясную дорожную карту: меняя молекулярную структуру, особенно длину цепи, инженеры могут проектировать оптимизированные ингибиторы, которые проще синтезировать, эффективны в малых дозах и пригодны для масштабного применения в промышленности, чтобы делать стальные конструкции более безопасными и долговечными.
Цитирование: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Ключевые слова: коррозия углеродистой стали, ингибиторы коррозии, соединения хиназолинона, кислые среды, защита поверхности