Clear Sky Science · es
Efecto de la longitud de la cadena alquilo en el rendimiento de inhibición de corrosión de derivados de 2‑tioxo‑2,3‑dihidroquinazolin‑4(1H)‑ona para acero al carbono en solución de HCl
Protegiendo los metales cotidianos del daño oculto
Desde puentes y edificios hasta automóviles y electrodomésticos, el acero al carbono sostiene en silencio gran parte de la vida moderna. Sin embargo, este metal todoterreno tiene una debilidad: en ambientes ácidos, como los usados para limpiar equipos industriales o en el procesamiento de petróleo y gas, puede disolverse sorprendentemente rápido. Este estudio explora si dos moléculas orgánicas pequeñas y fáciles de sintetizar pueden actuar como escudos invisibles sobre el acero, frenando este daño silencioso y alargando la vida útil de infraestructuras vitales.
Por qué el acero necesita un guardaespaldas químico
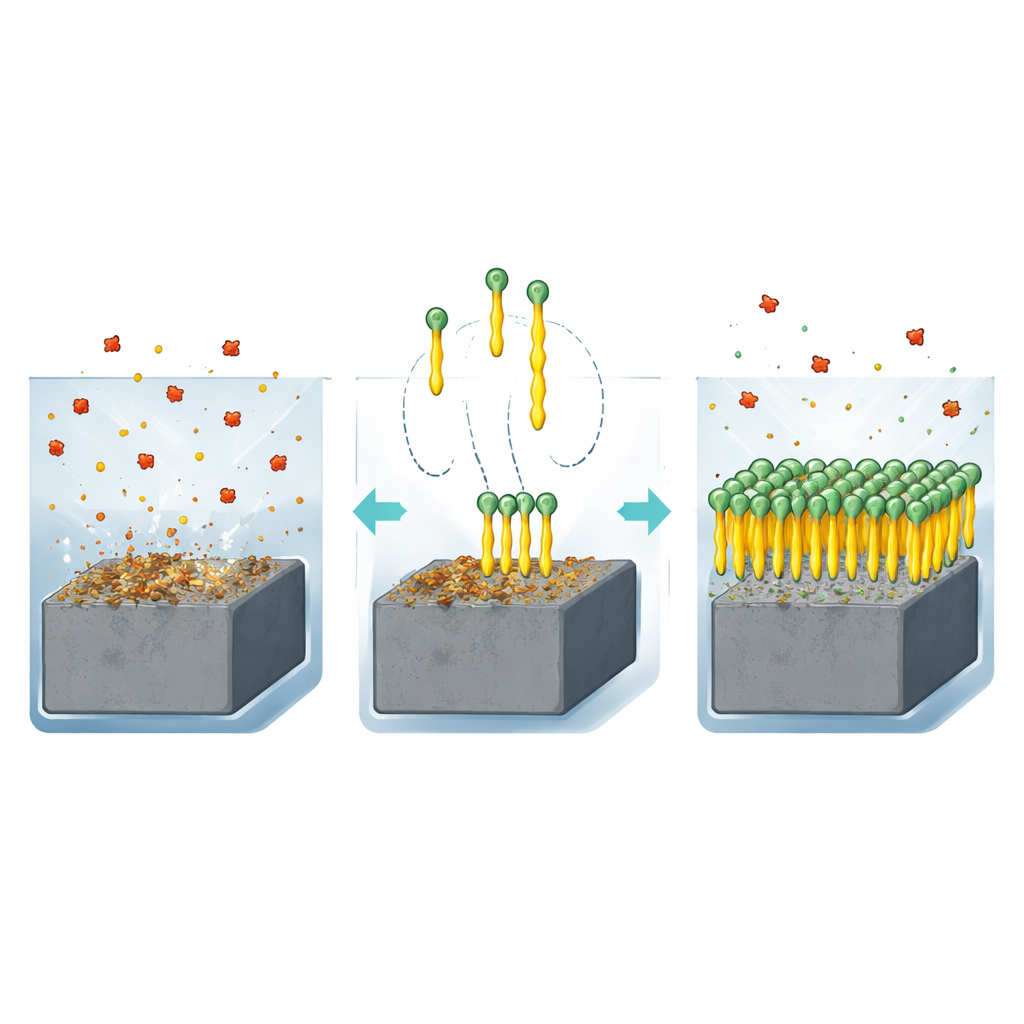
Cuando el acero al carbono se expone a un líquido ácido como el ácido clorhídrico, los átomos de su superficie reaccionan y se desprenden hacia la solución. Con el tiempo, esta corrosión puede adelgazarlas tuberías, debilitar los tanques y comprometer la seguridad. Una de las formas más prácticas de combatir este proceso es añadir pequeñas cantidades de moléculas especiales llamadas inhibidores al líquido. Estas moléculas se adsorben en la superficie del acero y forman una película protectora que bloquea el ataque. Los autores se centraron en una familia de compuestos conocidos como quinazolinonas, que contienen nitrógeno, azufre y oxígeno capaces de adherirse con fuerza al metal. Diseñaron dos versiones muy sencillas, idénticas salvo por la longitud de una sola cadena de carbono: un grupo metilo corto (Q‑C1) y una cadena butilo más larga (Q‑C4).
Probando dos moléculas pequeñas como escudos del acero
Para evaluar la eficacia de estos compuestos, el equipo sumergió muestras de acero al carbono en ácido clorhídrico concentrado con y sin los inhibidores. Pesar cuidadosamente las muestras antes y después de la exposición permitió determinar cuánto metal se había disuelto. También emplearon pruebas electroquímicas, que registran con qué facilidad se mueve la carga eléctrica a través de la interfaz acero‑solución, aportando una medida sensible de la tasa de corrosión. En una gama de concentraciones, ambas moléculas redujeron significativamente la pérdida de acero, alcanzando la de cadena más larga Q‑C4 casi un 89 % de protección en sus mejores condiciones. Sin embargo, el efecto protector se debilitó a temperaturas más altas, lo que sugiere que la película inhibidora se vuelve menos estable cuando el calor fomenta la desorción de las moléculas de la superficie.
Cómo se forma y mantiene la película protectora
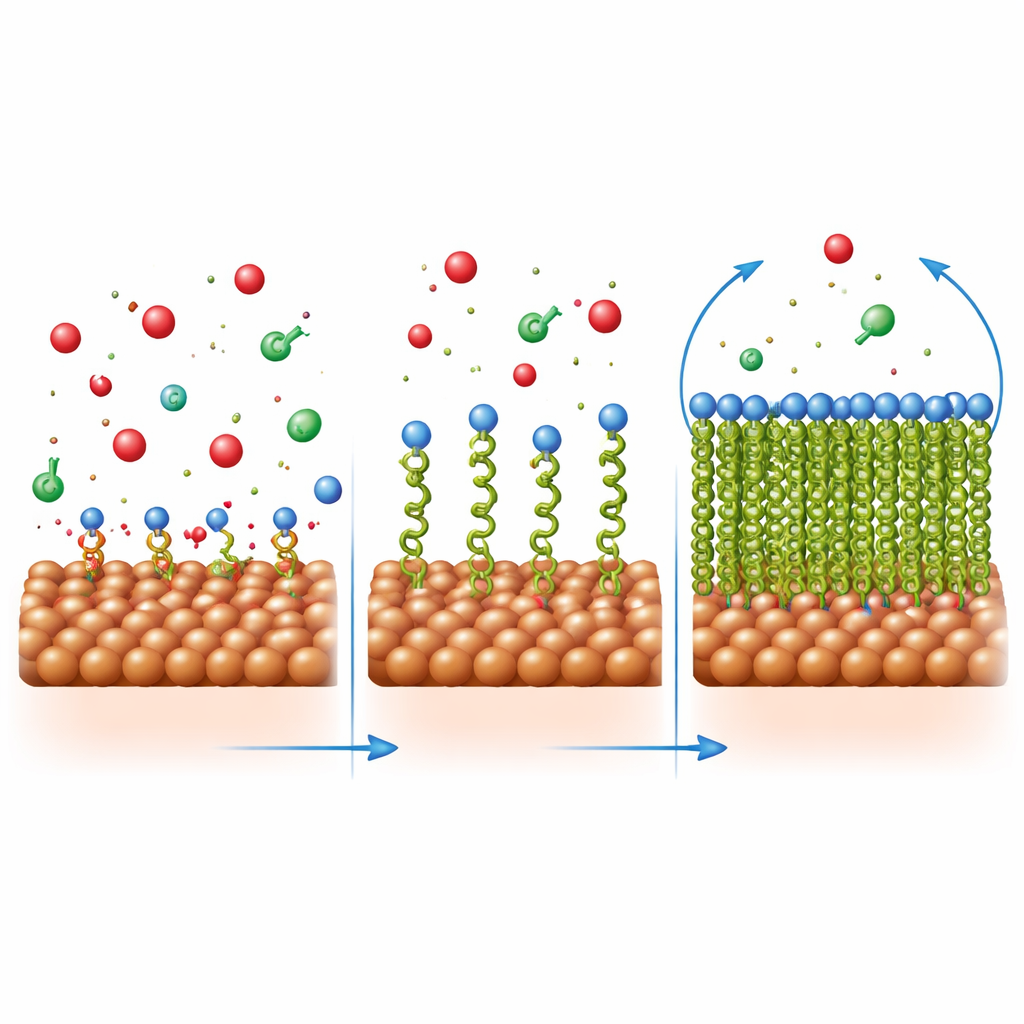
Los investigadores investigaron cómo se adhieren estas moléculas al acero analizando cómo varía la cobertura con la concentración. El patrón siguió un modelo simple de “una capa”, lo que indica que cada molécula inhibidora ocupa un sitio distinto en la superficie en lugar de apilarse en capas gruesas. Los cálculos de los cambios energéticos mostraron que la adsorción implica tanto atracción física (por diferencias de carga) como enlace químico (por intercambio de electrones con el metal). Imágenes microscópicas respaldaron este panorama: el acero sin inhibidor en ácido desarrolló picaduras y grietas, mientras que el acero en ácido con inhibidor apareció mucho más liso, cubierto por una capa más uniforme. El análisis elemental y la espectroscopía infrarroja confirmaron que las moléculas orgánicas estaban presentes en la superficie y que sus grupos enlazantes habían interactuado con átomos de hierro.
Por qué la cadena más larga funciona mejor
Aunque ambas moléculas comparten la misma “cabeza” que se ancla al acero, sus “colas” se comportan de forma distinta. La cadena butilo más larga de Q‑C4 es más hidrofóbica que el grupo metilo corto de Q‑C1. Una vez que el grupo cabeza se fija al metal, esta cola ayuda a formar una película más gruesa y completa que mantiene la solución ácida a distancia. Simulaciones computacionales mediante teoría del funcional de la densidad apoyaron esta conclusión: se calculó que Q‑C4 tiene una ligera mayor capacidad para donar electrones y una estructura electrónica más blanda, lo que favorece una interacción más fuerte con el metal. En conjunto, estas propiedades permiten que Q‑C4 se empaquete más densamente y forme una barrera más eficaz, dejando menos puntos expuestos donde puede iniciarse la corrosión.
Qué significa esto para la protección del acero en el mundo real
En términos sencillos, el estudio muestra que moléculas orgánicas muy simples y de bajo coste pueden ofrecer una protección sustancial al acero al carbono en ambientes ácidos agresivos, y que modificar algo tan modesto como la longitud de una cadena de carbono puede marcar una diferencia notable. El inhibidor de cola más larga forma un recubrimiento más denso y resistente, reduciendo la corrosión mucho más que su homólogo de cola corta. Si bien la protección disminuye a temperaturas elevadas, el trabajo ofrece una hoja de ruta clara: ajustando la estructura molecular, en especial la longitud de la cadena, los ingenieros pueden diseñar inhibidores a medida que sean más sencillos de producir, eficaces a bajas dosis y adecuados para uso industrial a gran escala para mantener las estructuras de acero más seguras y duraderas.
Cita: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Palabras clave: corrosión del acero al carbono, inhibidores de corrosión, compuestos quinazolinona, ambientes ácidos, protección de superficies