Clear Sky Science · it
Effetto della lunghezza della catena alchilica sulle prestazioni inibitorie di corrosione dei derivati 2-tioxo-2,3-diidrochinazolin-4(1H)-one per acciaio al carbonio in soluzione HCl
Proteggere i metalli di uso quotidiano dai danni nascosti
Dai ponti e gli edifici alle automobili e agli elettrodomestici, l'acciaio al carbonio sostiene in silenzio gran parte della vita moderna. Tuttavia questo metallo ha una debolezza: in ambienti acidi, come quelli impiegati per pulire apparecchiature industriali o nei processi petroliferi, può dissolversi sorprendentemente in fretta. Questo studio esplora se due piccole molecole organiche, facili da sintetizzare, possono agire come scudi invisibili sull'acciaio, rallentando questo danno silenzioso e prolungando la vita delle infrastrutture vitali.
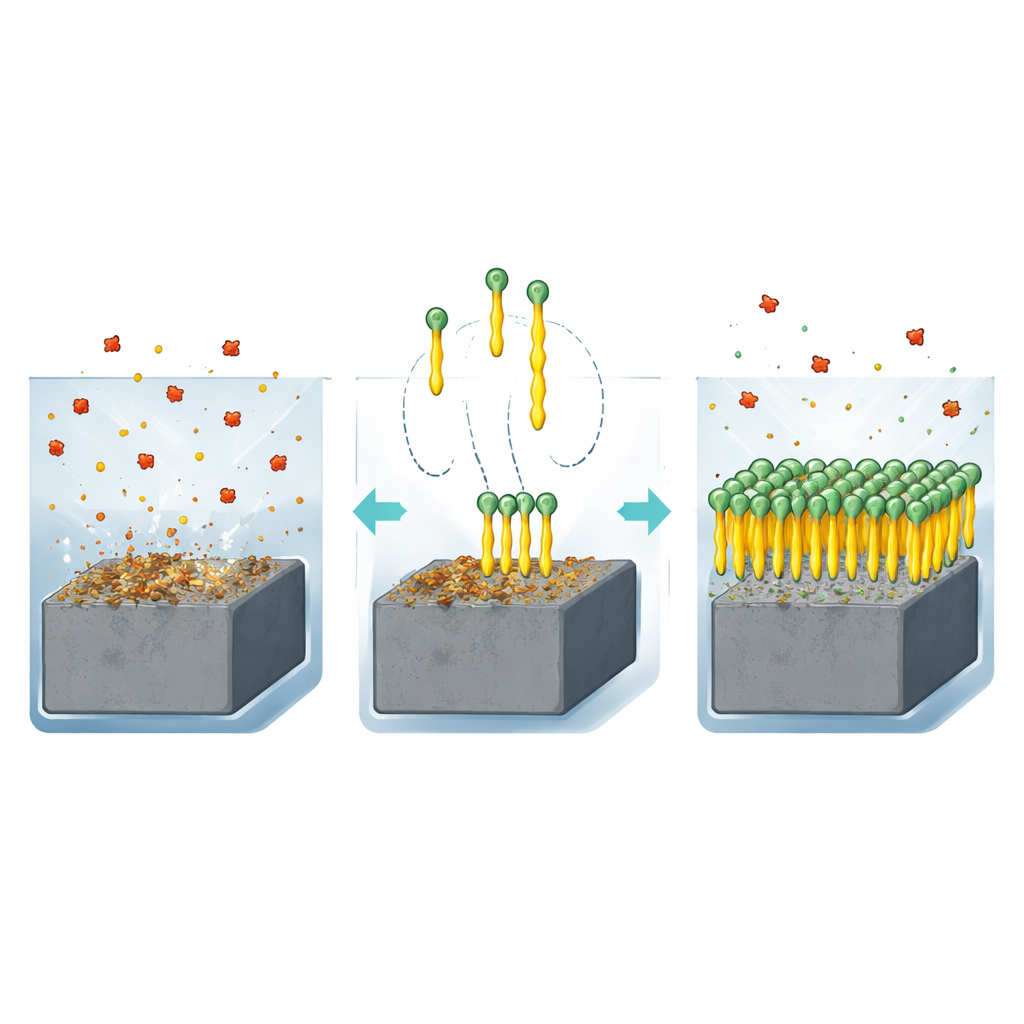
Perché l'acciaio ha bisogno di una guardia chimica
Quando l'acciaio al carbonio è immerso in un liquido acido come l'acido cloridrico, gli atomi sulla sua superficie reagiscono e si staccano nella soluzione. Col tempo, questa corrosione può assottigliare tubi, indebolire serbatoi e compromettere la sicurezza. Uno dei modi più pratici per contrastare questo processo è aggiungere piccole quantità di molecole speciali dette inibitori al liquido. Queste molecole si legano alla superficie dell'acciaio e formano un film protettivo che impedisce ulteriori attacchi. Gli autori si sono concentrati su una famiglia di composti noti come quinazolinoni, che contengono atomi di azoto, zolfo e ossigeno in grado di aderire saldamente al metallo. Hanno progettato due versioni molto semplici, identiche tranne che per la lunghezza di una singola catena carboniosa: un gruppo metile corto (Q‑C1) e un gruppo butile più lungo (Q‑C4).
Testare due piccole molecole come scudi per l'acciaio
Per valutare l'efficacia di questi composti, il team ha immerso campioni di acciaio al carbonio in acido cloridrico concentrato con e senza inibitori. Pesando con precisione i campioni prima e dopo l'esposizione, hanno potuto determinare quanto metallo si fosse dissolto. Hanno inoltre impiegato test elettrochimici, che misurano quanto facilmente la carica elettrica si trasferisce attraverso l'interfaccia acciaio–soluzione, fornendo una misura sensibile della velocità di corrosione. Su una gamma di concentrazioni, entrambe le molecole hanno ridotto sensibilmente la perdita di acciaio, con la Q‑C4 a catena più lunga che ha raggiunto quasi l'89% di protezione nelle condizioni migliori. Tuttavia, l'effetto protettivo si è indebolito a temperature più elevate, suggerendo che il film inibitore diventa meno stabile quando il calore favorisce il distacco delle molecole dalla superficie.
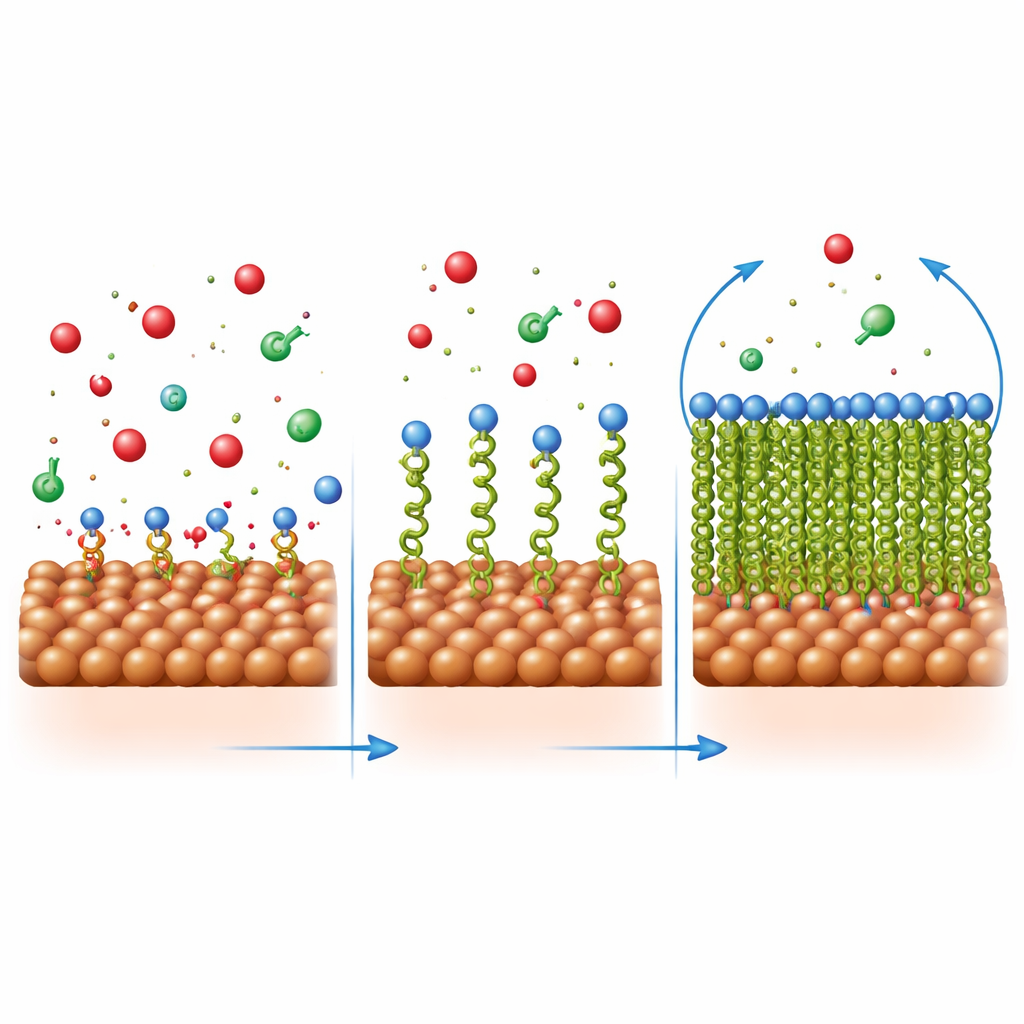
Come si forma e si mantiene il film protettivo
I ricercatori hanno esaminato il modo in cui queste molecole si dispongono sull'acciaio analizzando come la copertura varia con la concentrazione. Il comportamento seguito è stato quello di un semplice modello «a strato singolo», il che significa che ogni molecola inibitrice occupa un posto distinto sulla superficie piuttosto che impilarsi in strati spessi. I calcoli delle variazioni di energia hanno mostrato che l'adesione comporta sia attrazione fisica (attraverso differenze di carica) sia legami chimici (condivisione di elettroni con il metallo). Immagini microscopiche hanno supportato questo quadro: l'acciaio nudo in ambiente acido presentava crateri e fessure, mentre l'acciaio in acido contenente inibitori appariva molto più uniforme, ricoperto da uno strato regolare. L'analisi elementare e la spettroscopia infrarossa hanno confermato che le molecole organiche erano effettivamente presenti sulla superficie dell'acciaio e che i loro gruppi leganti avevano interagito con gli atomi di ferro.
Perché la catena più lunga funziona meglio
Pur condividendo la stessa «testa» che si ancora al metallo, le loro «code» si comportano in modo diverso. La catena butilica più lunga della Q‑C4 è più idrofobica rispetto al breve gruppo metile della Q‑C1. Una volta che il gruppo testa si ancora al metallo, questa coda contribuisce a formare un film più spesso e più completo che tiene la soluzione acida a distanza. Le simulazioni al calcolatore basate sulla teoria del funzionale della densità confermano questo risultato: per Q‑C4 è stata calcolata una capacità leggermente maggiore di donare elettroni e una struttura elettronica più «morbida», caratteristiche che favoriscono un'interazione più forte con il metallo. Insieme, questi tratti aiutano Q‑C4 a impaccarsi più strettamente e a formare una barriera più efficace, lasciando meno punti esposti dove può iniziare la corrosione.
Cosa significa per la protezione dell'acciaio nel mondo reale
In termini concreti, lo studio dimostra che molecole organiche molto semplici e a basso costo possono offrire all'acciaio al carbonio una protezione sostanziale in ambienti acidi aggressivi, e che modificare anche un elemento modesto come la lunghezza di una catena carboniosa può fare una differenza evidente. L'inibitore a coda più lunga forma un rivestimento più denso e resistente, riducendo la corrosione molto più del suo parente a catena corta. Sebbene la protezione diminuisca alle temperature più elevate, il lavoro offre una chiara strada da seguire: modulando la struttura molecolare, in particolare la lunghezza della catena, gli ingegneri possono progettare inibitori su misura, facili da produrre, efficaci a basse dosi e adatti a un impiego su larga scala nell'industria per mantenere le strutture in acciaio più sicure e durature.
Citazione: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Parole chiave: corrosione acciaio al carbonio, inibitori di corrosione, composti quinazolinonici, ambienti acidi, protezione delle superfici