Clear Sky Science · nl
Effect van lengte van de alkylketen op de corrosieremmende werking van 2-thioxo-2,3-dihydroquinazolin-4(1H)-on-derivaten voor koolstofstaal in HCl-oplossing
Dagelijks metaal beschermen tegen verborgen schade
Van bruggen en gebouwen tot auto’s en huishoudelijke apparaten: koolstofstaal draagt stilletjes veel van het moderne leven. Dit werkpaard heeft echter een zwakte: in zure omgevingen, zoals bij het reinigen van industriële apparatuur of bij olie- en gasverwerking, kan het verrassend snel oplossen. Deze studie onderzoekt of twee kleine, eenvoudig te maken organische moleculen als onzichtbare schilden op staal kunnen fungeren, dit sluipende verval kunnen vertragen en de levensduur van cruciale infrastructuur kunnen verlengen.
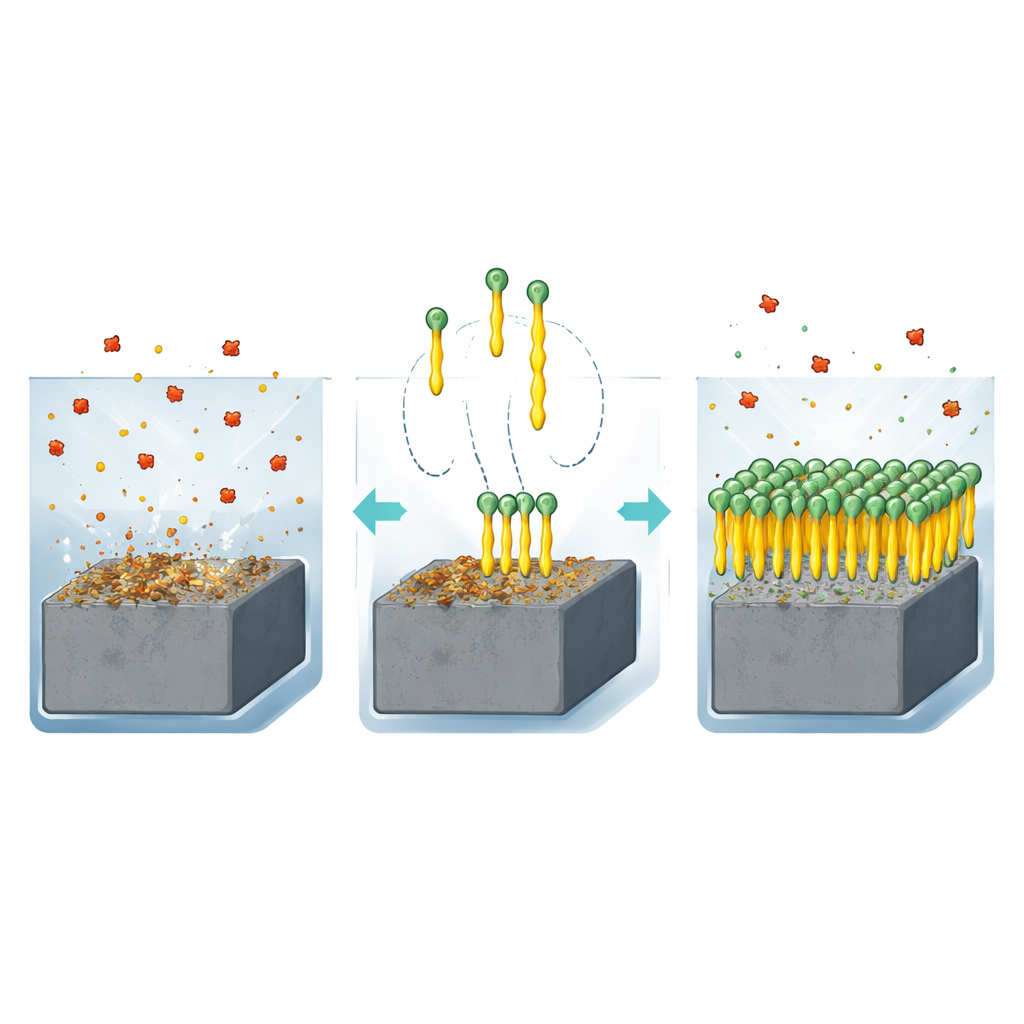
Waarom staal een chemische lijfwacht nodig heeft
Wanneer koolstofstaal in een zure vloeistof zoals zoutzuur staat, reageren atomen aan het oppervlak en laten ze los naar de oplossing. Na verloop van tijd kan deze corrosie pijpen dunner maken, tanks verzwakken en de veiligheid in gevaar brengen. Een van de meest praktische manieren om dit proces te bestrijden is het toevoegen van kleine hoeveelheden speciale moleculen, zogeheten remmers, aan de vloeistof. Deze moleculen hechten zich aan het staaloppervlak en vormen een beschermende film die verdere aantasting belemmert. De auteurs richten zich op een familie van verbindingen die bekendstaan als quinazolinonen, die stikstof-, zwavel- en zuurstofatomen bevatten die sterk aan metaal kunnen binden. Ze ontwierpen twee zeer eenvoudige varianten, identiek behalve in de lengte van één koolstofketen: een korte methylgroep (Q‑C1) en een langere butylgroep (Q‑C4).
Het testen van twee kleine moleculen als stalen schilden
Om te beoordelen hoe goed deze verbindingen staal verdedigen, dompelde het team koolstofstaalmonsters onder in sterk zoutzuur met en zonder de remmers. Door de monsters zorgvuldig te wegen voor en na blootstelling, konden ze bepalen hoeveel metaal was opgelost. Ze gebruikten ook elektrochemische tests, die volgen hoe gemakkelijk elektrische lading over het grensvlak staal–oplossing beweegt en zo een gevoelige maat geven voor de corrosiesnelheid. Over een reeks concentraties verminderden beide moleculen het staalverlies aanzienlijk, waarbij de langketenige Q‑C4 onder optimale condities bijna 89% bescherming bereikte. De beschermende werking verzwakte echter bij hogere temperaturen, wat erop wijst dat de remmende film minder stabiel wordt naarmate warmte de moleculen aanmoedigt om van het oppervlak los te laten.
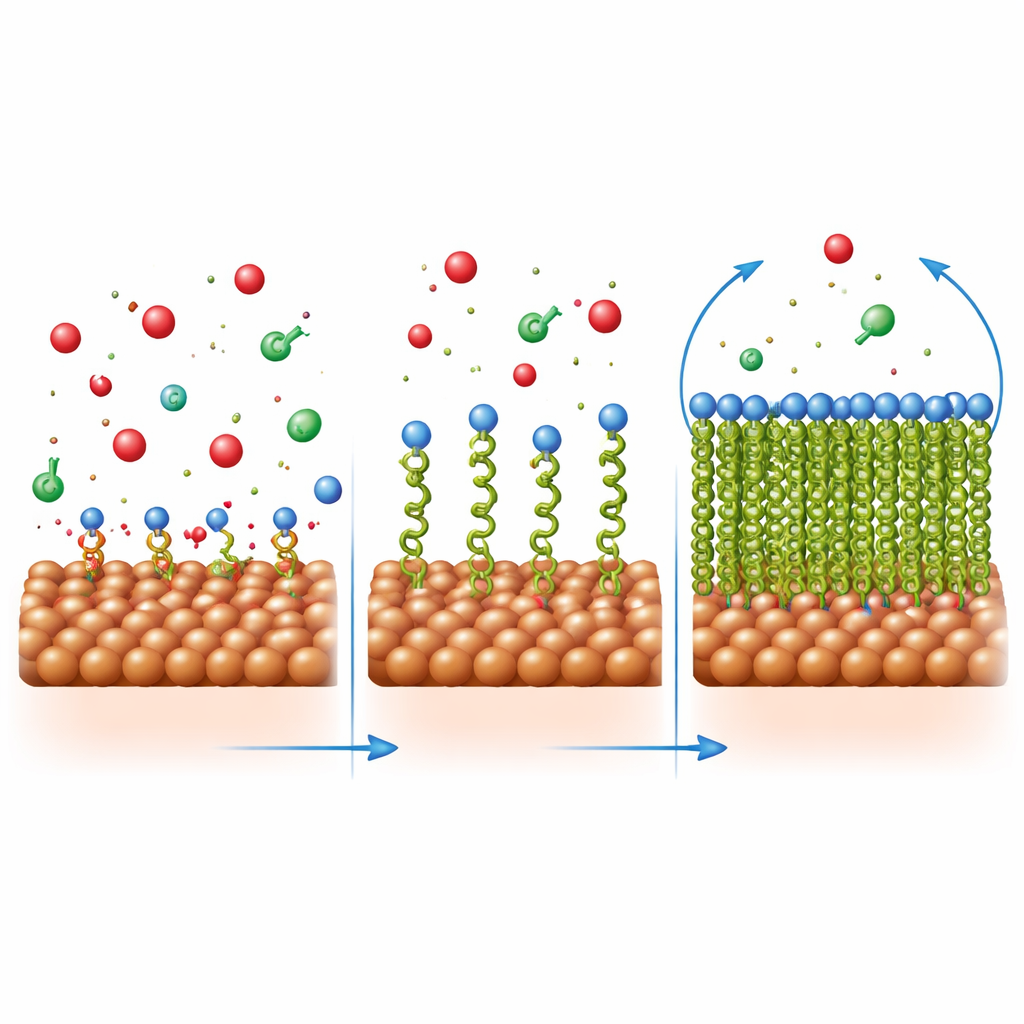
Hoe de beschermende film zich vormt en intact blijft
De onderzoekers onderzochten hoe deze moleculen zich op staal plaatsen door te analyseren hoe de bedekking verandert met concentratie. Het patroon volgde een eenvoudig “éénlaag”-model, wat betekent dat elk remmingsmolecuul een afzonderlijke plaats op het oppervlak inneemt in plaats van stapels te vormen. Berekeningen van energieveranderingen lieten zien dat de hechting zowel fysieke aantrekking (via ladingsverschillen) als chemische binding (door elektronen te delen met het metaal) omvat. Microscopische beelden ondersteunden dit beeld: bloot staal in zuur ontwikkelde putten en scheurtjes, terwijl staal in geïnhibeerd zuur er veel gladder uitzag, bedekt door een gelijkmatiger laag. Elementanalyse en infraroodspectroscopie bevestigden dat de organische moleculen inderdaad aanwezig waren op het staaloppervlak en dat hun bindingsgroepen interactie hadden gehad met ijzeratomen.
Waarom de langere keten beter werkt
Hoewel beide moleculen dezelfde “kop” delen die het staal vastgrijpt, gedragen hun “staarten” zich anders. De langere butylketen in Q‑C4 is minder wateraantrekkend dan de korte methylketen in Q‑C1. Zodra de kopgroep zich aan het metaal verankert, helpt deze staart een dichtere, meer complete film op te bouwen die de zure oplossing op afstand houdt. Computersimulaties met dichtheidsfunctionaaltheorie ondersteunden dit: Q‑C4 bleek iets sterker in staat te zijn elektronen te doneren en had een zachtere elektronische structuur, wat sterkere interactie met het metaal bevordert. Samen helpen deze eigenschappen Q‑C4 strakker te pakken en een effectievere barrière te vormen, waardoor er minder blootliggende plekken overblijven waar corrosie kan beginnen.
Wat dit betekent voor bescherming van staal in de praktijk
Kort gezegd laat de studie zien dat zeer eenvoudige, goedkope organische moleculen koolstofstaal substantiële bescherming kunnen bieden in agressieve zure omgevingen, en dat het aanpassen van iets schijnbaar gerings als de lengte van een koolstofketen een merkbaar verschil kan maken. De langstaartige remmer vormt een dichtere, beter bestand laag en vermindert corrosie veel meer dan zijn kortere verwant. Hoewel de bescherming afneemt bij hogere temperaturen, biedt het werk een duidelijk stappenplan: door de moleculaire structuur, en met name de ketenlengte, aan te passen, kunnen ingenieurs op maat gemaakte remmers ontwerpen die makkelijker te produceren zijn, effectief bij lage doses en geschikt voor grootschalig industrieel gebruik om stalen constructies veiliger en langer houdbaar te maken.
Bronvermelding: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Trefwoorden: corrosie van koolstofstaal, corrosieremmers, quinazolinonverbindingen, zure omgevingen, oppervlaktebescherming