Clear Sky Science · de
Einfluss der Länge der Alkylkette auf die Korrosionsinhibitionsleistung von 2‑thioxo‑2,3‑dihydroquinazolin‑4(1H)‑on‑Derivaten für Kohlenstoffstahl in HCl‑Lösung
Alltagsmetalle vor verdeckten Schäden schützen
Von Brücken und Gebäuden bis hin zu Autos und Haushaltsgeräten stützt Kohlenstoffstahl einen Großteil des modernen Lebens. Dieses Arbeitstier hat jedoch eine Schwäche: In sauren Umgebungen, wie sie etwa bei der Reinigung industrieller Anlagen oder in der Öl‑ und Gasverarbeitung vorkommen, kann er überraschend schnell aufgelöst werden. Diese Studie untersucht, ob zwei kleine, einfach herstellbare organische Moleküle wie unsichtbare Schutzschilde auf Stahl wirken können, die diesen stillen Schaden verlangsamen und die Lebensdauer wichtiger Infrastruktur verlängern.
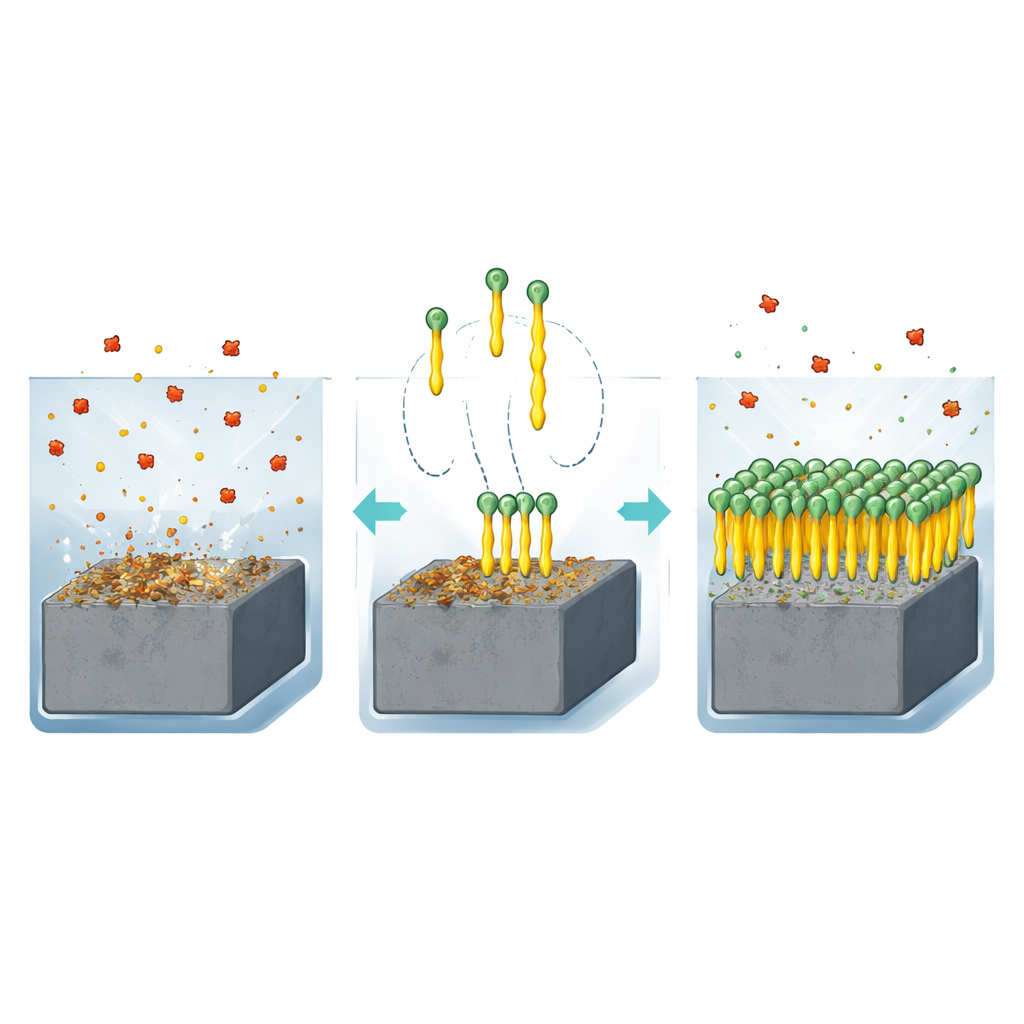
Warum Stahl einen chemischen Bodyguard braucht
Wenn Kohlenstoffstahl in einer sauren Lösung wie Salzsäure liegt, reagieren Atome an seiner Oberfläche und lösen sich in die Lösung. Im Laufe der Zeit kann diese Korrosion Rohre ausdünnen, Tanks schwächen und die Sicherheit beeinträchtigen. Eine der praktischsten Methoden, diesem Prozess entgegenzuwirken, besteht darin, der Lösung geringe Mengen spezieller Moleküle — sogenannter Inhibitoren — beizugeben. Diese Moleküle heften sich an die Stahloberfläche und bilden einen Schutzfilm, der weiteren Angriff blockiert. Die Autoren konzentrierten sich auf eine Familie von Verbindungen, die als Quinazolinone bekannt sind und Stickstoff-, Schwefel‑ und Sauerstoffatome enthalten, die stark am Metall haften können. Sie entwarfen zwei sehr einfache Varianten, die sich nur in der Länge einer Kohlenstoffkette unterscheiden: eine kurze Methylgruppe (Q‑C1) und eine längere Butylgruppe (Q‑C4).
Zwei kleine Moleküle als Stahlschutz testen
Um zu prüfen, wie gut diese Verbindungen Stahl schützen, tauchte das Team Kohlenstoffstahlproben in konzentrierte Salzsäure mit und ohne Inhibitoren. Durch sorgfältiges Wiegen der Proben vor und nach der Exposition konnten sie ermitteln, wie viel Metall sich gelöst hatte. Sie nutzten außerdem elektrochemische Tests, die verfolgen, wie leicht elektrische Ladung über die Stahl‑Lösungs‑Grenzfläche wandert und so eine empfindliche Messgröße für die Korrosionsrate liefern. Über einen Bereich von Konzentrationen verringerten beide Moleküle den Metallverlust deutlich, wobei das längerkettige Q‑C4 unter besten Bedingungen nahezu 89 % Schutz erreichte. Die Schutzwirkung schwächte sich jedoch bei höheren Temperaturen ab, was darauf hindeutet, dass der Inhibitorfilm weniger stabil wird, wenn Wärme das Ablösen der Moleküle von der Oberfläche begünstigt.
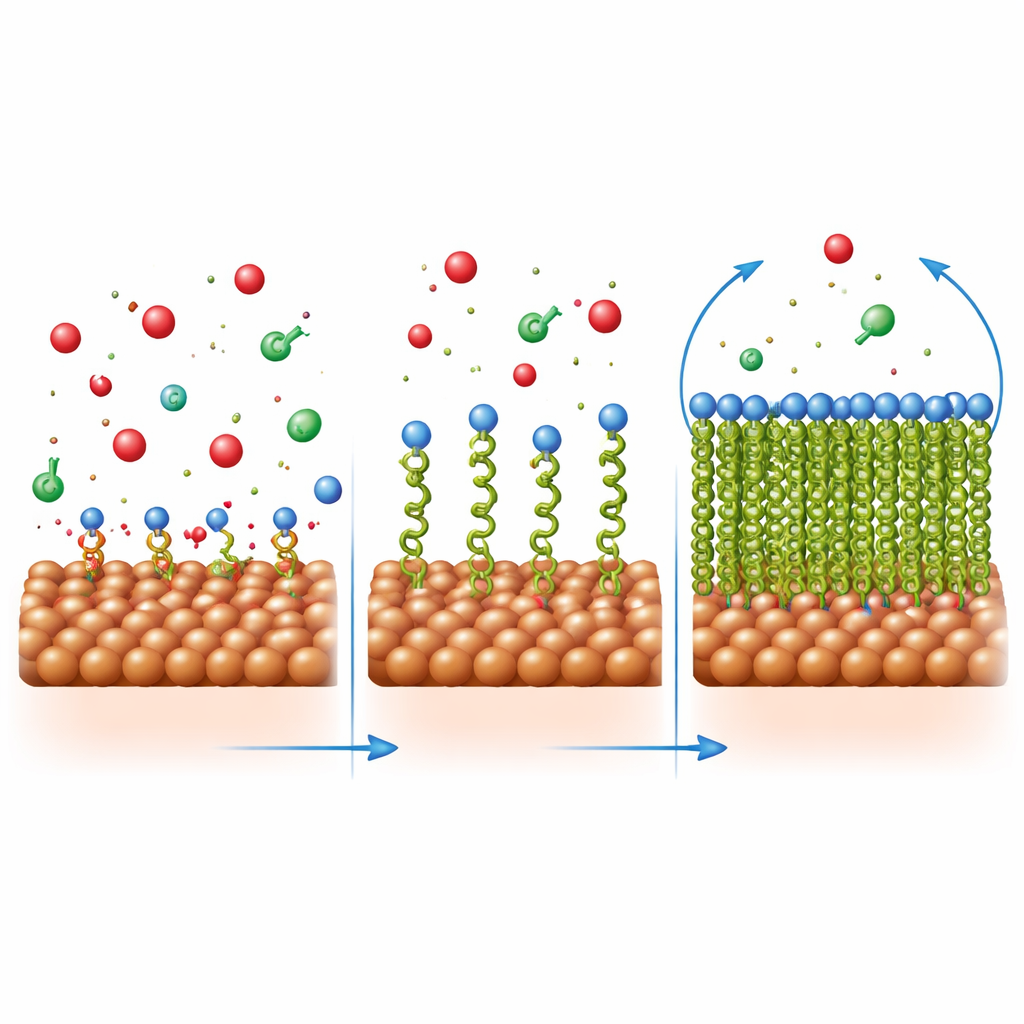
Wie der Schutzfilm entsteht und zusammenhält
Die Forschenden untersuchten, wie diese Moleküle auf dem Stahl anordnen, indem sie analysierten, wie die Bedeckung mit der Konzentration variiert. Das Muster folgte einem einfachen „Einlagenmodell“, was bedeutet, dass jedes Inhibitormolekül einen eigenen Platz auf der Oberfläche einnimmt, anstatt sich zu dicken Schichten aufzubauen. Berechnungen der Energieänderungen zeigten, dass die Anlagerung sowohl physikalische Attraktion (über Ladungsunterschiede) als auch chemische Bindung (durch Elektronenpaarübertragung mit dem Metall) umfasst. Mikroskopische Aufnahmen bestätigten dieses Bild: Unbehandelter Stahl in Säure zeigte Gruben und Risse, während Stahl in inhibierter Säure deutlich glatter aussah und von einer gleichmäßigeren Schicht bedeckt war. Elementanalysen und Infrarotspektroskopie bestätigten, dass die organischen Moleküle tatsächlich auf der Stahloberfläche vorhanden waren und dass ihre Bindungsgruppen mit den Eisenatomen interagiert hatten.
Warum die längere Kette besser wirkt
Obwohl beide Moleküle denselben „Kopf“ besitzen, der am Stahl anhaftet, verhalten sich ihre „Schwänze“ unterschiedlich. Die längere Butylkette in Q‑C4 ist wasserabweisender als die kurze Methylkette in Q‑C1. Sobald die Kopfgruppe am Metall verankert ist, hilft dieser Schwanz, einen dichteren, kompletteren Film aufzubauen, der die saure Lösung fernhält. Computersimulationen auf Basis der Dichtefunktionaltheorie stützten dies: Für Q‑C4 wurde eine etwas stärkere Elektronendonationsfähigkeit und eine weichere elektronische Struktur berechnet, was stärkere Wechselwirkungen mit dem Metall fördert. Zusammengenommen ermöglichen diese Eigenschaften, dass sich Q‑C4 dichter verpackt und eine effektivere Barriere bildet, sodass weniger freie Stellen verbleiben, an denen Korrosion einsetzen kann.
Was das für den praktischen Stahlschutz bedeutet
Einfach gesagt zeigt die Studie, dass sehr einfache, kostengünstige organische Moleküle Kohlenstoffstahl in aggressiven sauren Umgebungen deutlich schützen können und dass die Veränderung etwas so Unscheinbarem wie der Länge einer Kohlenstoffkette einen spürbaren Unterschied machen kann. Der länger geschwänzte Inhibitor bildet eine dichtere, widerstandsfähigere Beschichtung und reduziert die Korrosion deutlich stärker als sein kurzschwänziger Verwandter. Zwar nimmt der Schutz bei höheren Temperaturen ab, doch die Arbeit liefert eine klare Handlungsanweisung: Durch Anpassung der Molekülstruktur, insbesondere der Kettenlänge, können Ingenieure maßgeschneiderte Inhibitoren entwickeln, die sich leicht herstellen lassen, bei geringen Dosierungen wirksam sind und sich für den großtechnischen Einsatz eignen, um Stahlstrukturen sicherer und langlebiger zu machen.
Zitation: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Schlüsselwörter: Korrosion von Kohlenstoffstahl, Korrosionsinhibitoren, Quinazolinon‑Verbindungen, saure Umgebungen, Oberflächenschutz