Clear Sky Science · pt
Efeito do comprimento da cadeia alcila na performance de inibição de corrosão de derivados de 2-tioxo-2,3-dihidroquinazolin-4(1H)-ona para aço carbono em solução de HCl
Protegendo metais do dia a dia contra danos ocultos
De pontes e edifícios a automóveis e eletrodomésticos, o aço carbono sustenta discretamente grande parte da vida moderna. No entanto, esse metal tão utilizado tem uma vulnerabilidade: em ambientes ácidos, como os empregados na limpeza de equipamentos industriais ou no processamento de petróleo e gás, ele pode se dissolver surpreendentemente rápido. Este estudo investiga se duas pequenas moléculas orgânicas fáceis de produzir podem atuar como escudos invisíveis no aço, retardando esse dano silencioso e prolongando a vida útil de infraestruturas essenciais.
Por que o aço precisa de um guarda-costas químico
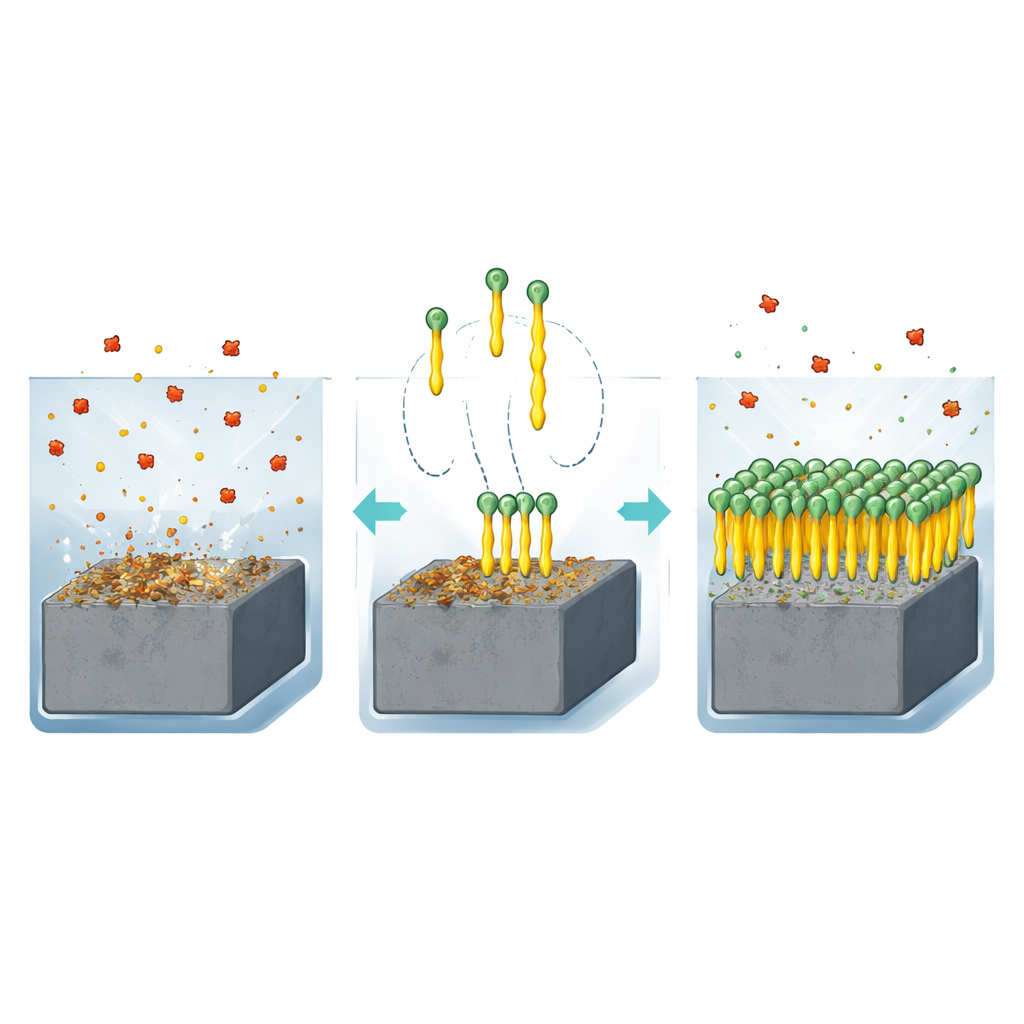
Quando o aço carbono fica imerso em um líquido ácido como o ácido clorídrico, os átomos em sua superfície reagem e se desprendem para a solução. Com o tempo, essa corrosão pode afinar tubos, enfraquecer tanques e comprometer a segurança. Uma das formas mais práticas de combater esse processo é adicionar pequenas quantidades de moléculas especiais chamadas inibidores ao líquido. Essas moléculas se ligam à superfície do aço e formam uma película protetora que bloqueia novos ataques. Os autores focaram em uma família de compostos conhecida como quinazolinonas, que contêm nitrogênio, enxofre e oxigênio — átomos capazes de aderir fortemente ao metal. Eles projetaram duas versões muito simples, idênticas exceto pelo comprimento de uma única cadeia carbônica: um grupo metila curto (Q‑C1) e um grupo butila mais longo (Q‑C4).
Testando duas pequenas moléculas como escudos para o aço
Para avaliar quão bem esses compostos defendem o aço, a equipe imergiu amostras de aço carbono em ácido clorídrico concentrado com e sem os inibidores. Pesando cuidadosamente as amostras antes e depois da exposição, foi possível determinar quanto metal se dissolveu. Também foram realizados testes eletroquímicos, que acompanham com que facilidade a carga elétrica atravessa a interface aço–solução, fornecendo uma medida sensível da taxa de corrosão. Em várias faixas de concentração, ambas as moléculas reduziram significativamente a perda de aço, com o Q‑C4 de cadeia mais longa atingindo quase 89% de proteção nas melhores condições. Entretanto, o efeito protetor enfraqueceu em temperaturas mais altas, sugerindo que a película inibidora se torna menos estável à medida que o calor favorece o desprendimento das moléculas da superfície.
Como a película protetora se forma e se mantém
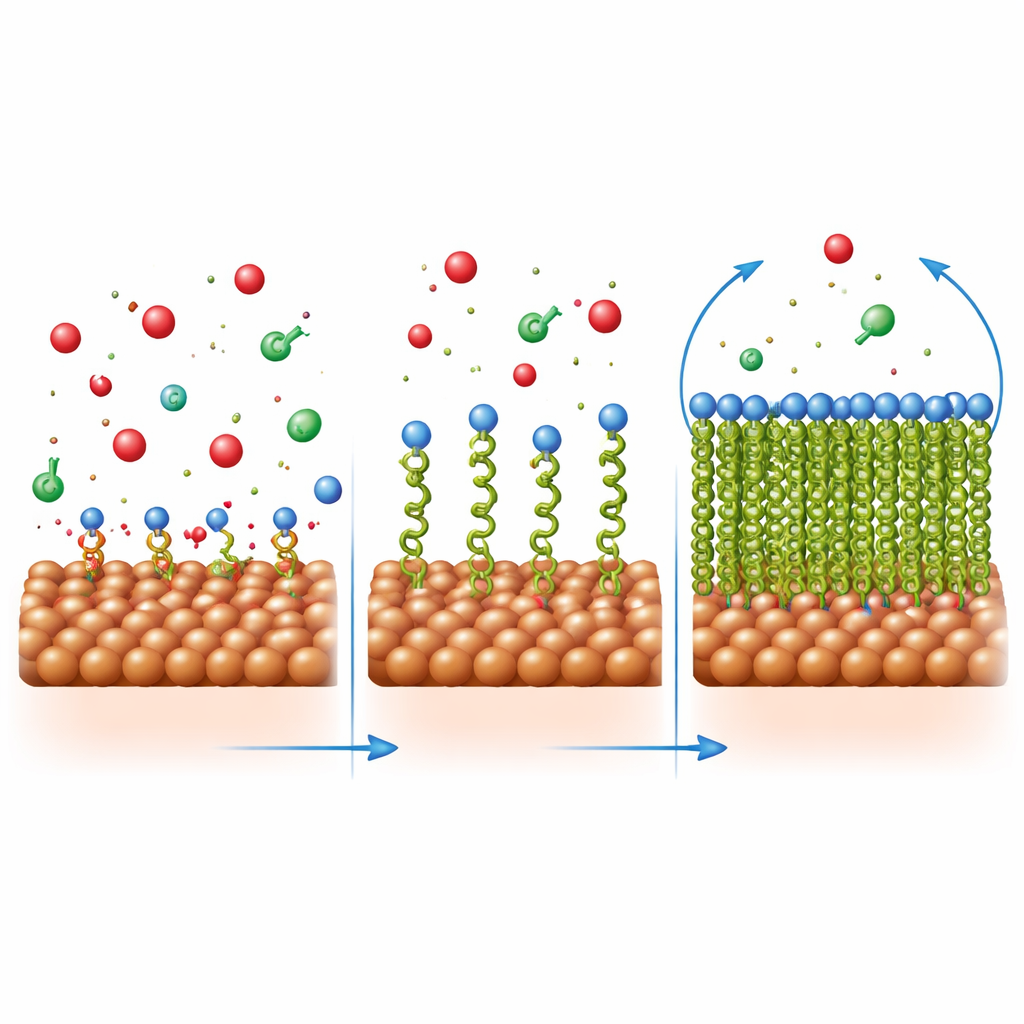
Os pesquisadores investigaram como essas moléculas se acomodam no aço analisando como a cobertura varia com a concentração. O padrão seguiu um modelo simples de “uma camada”, o que significa que cada molécula inibidora ocupa um ponto distinto na superfície em vez de empilhar-se em camadas espessas. Cálculos das variações de energia mostraram que a fixação envolve tanto atração física (por diferenças de carga) quanto ligação química (por compartilhamento de elétrons com o metal). Imagens microscópicas corroboraram esse quadro: o aço nu em ácido desenvolveu cavidades e trincas, enquanto o aço em ácido com inibidor parecia bem mais liso, coberto por uma camada mais uniforme. Análises elementares e espectroscopia no infravermelho confirmaram que as moléculas orgânicas estavam de fato presentes na superfície do aço e que seus grupos de ligação interagiram com átomos de ferro.
Por que a cadeia mais longa funciona melhor
Embora ambas as moléculas compartilhem a mesma “cabeça” que se agarra ao aço, suas “caudas” se comportam de modo diferente. A cadeia butila mais longa do Q‑C4 é mais hidrofóbica do que a curta cadeia metila do Q‑C1. Uma vez que o grupo cabeça ancora-se ao metal, essa cauda ajuda a construir uma película mais espessa e mais completa que mantém a solução ácida à distância. Simulações computacionais usando teoria do funcional da densidade apoiaram essa conclusão: foi calculado que o Q‑C4 tem uma capacidade ligeiramente maior de doar elétrons e uma estrutura eletrônica mais “suave”, o que favorece uma interação mais forte com o metal. Em conjunto, essas características ajudam o Q‑C4 a se empacotar com mais firmeza e formar uma barreira mais eficaz, deixando menos pontos expostos onde a corrosão pode começar.
O que isso significa para a proteção do aço no mundo real
Em termos práticos, o estudo mostra que moléculas orgânicas muito simples e de baixo custo podem oferecer proteção substancial ao aço carbono em ambientes ácidos severos, e que ajustar algo tão modesto quanto o comprimento de uma cadeia carbônica pode fazer diferença perceptível. O inibidor de cauda mais longa forma um revestimento mais denso e resistente, reduzindo a corrosão muito mais do que seu homólogo de cauda curta. Embora a proteção diminua em temperaturas elevadas, o trabalho oferece um roteiro claro: ao ajustar a estrutura molecular, especialmente o comprimento da cadeia, engenheiros podem projetar inibidores sob medida que sejam fáceis de produzir, eficazes em baixas concentrações e adequados para uso em grande escala na indústria, mantendo estruturas de aço mais seguras e duradouras.
Citação: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Palavras-chave: corrosão de aço carbono, inibidores de corrosão, compostos quinazolinona, ambientes ácidos, proteção de superfícies