Clear Sky Science · pl
Wpływ długości łańcucha alkilowego na skuteczność inhibitorów korozji pochodnych 2-tiokso-2,3-dihydrochinazolin-4(1H)-onu dla stali węglowej w roztworze HCl
Ochrona codziennych metali przed ukrytymi uszkodzeniami
Od mostów i budynków po samochody i sprzęt domowy — stal węglowa cicho podtrzymuje znaczną część współczesnego życia. Jednak ten niezawodny metal ma słabość: w środowiskach kwaśnych, takich jak te używane do czyszczenia urządzeń przemysłowych czy w przetwórstwie ropy i gazu, może ulegać szybkiemu rozpuszczaniu. W tym badaniu sprawdzono, czy dwa małe, łatwe do syntezy cząsteczki organiczne mogą działać jak niewidzialne tarcze na stali, spowalniając ten cichy proces niszczenia i wydłużając żywotność istotnej infrastruktury.
Dlaczego stal potrzebuje chemicznego ochroniarza
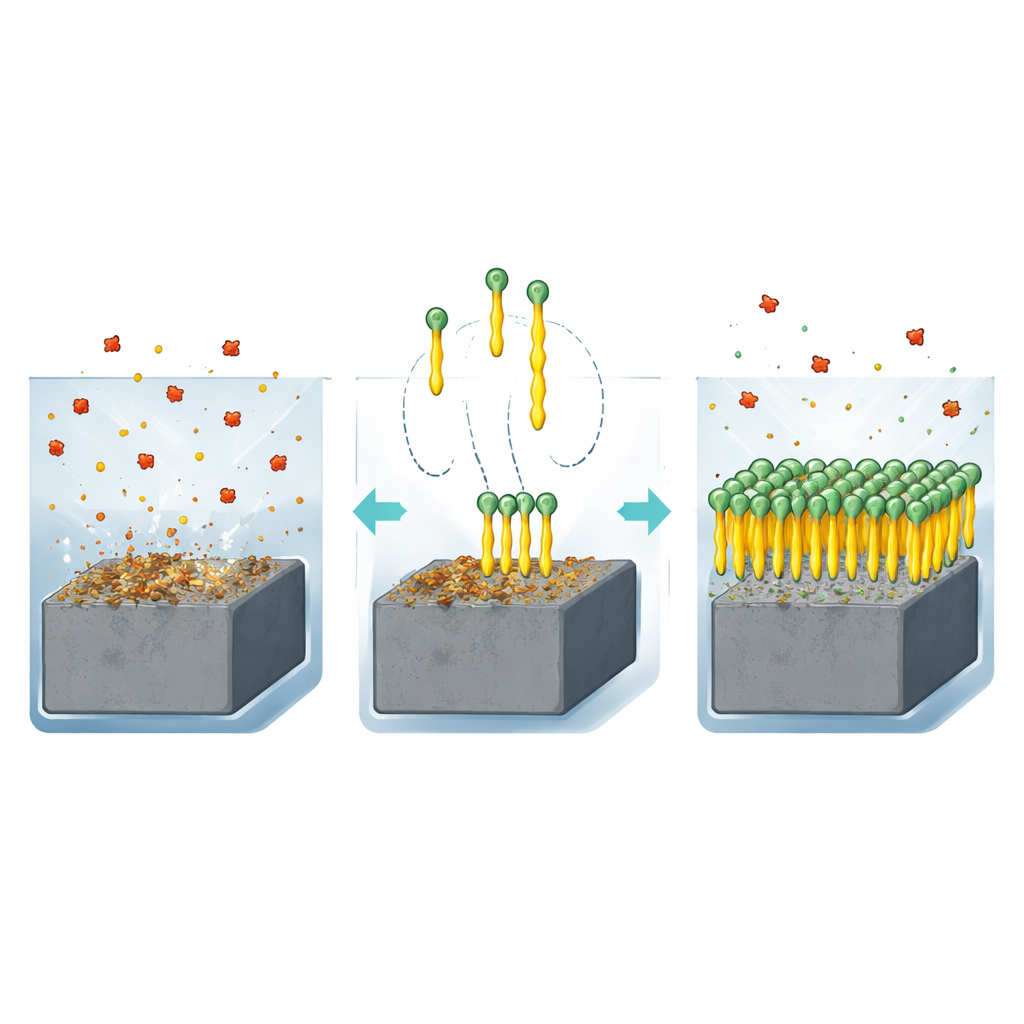
Gdy stal węglowa przebywa w kwaśnym roztworze, np. kwasu solnego, atomy na jej powierzchni reagują i odrywają się do roztworu. Z czasem korozja może przerzedzić rury, osłabić zbiorniki i zagrozić bezpieczeństwu. Jednym z najbardziej praktycznych sposobów walki z tym procesem jest dodanie niewielkich ilości specjalnych cząsteczek zwanych inhibitorami do roztworu. Cząsteczki te przyczepiają się do powierzchni stali i tworzą warstwę ochronną, która blokuje dalsze ataki. Autorzy skupili się na rodzinie związków znanych jako chinazolinony, które zawierają atomy azotu, siarki i tlenu i mogą silnie przylegać do metalu. Zaprojektowali dwie bardzo proste wersje, identyczne z wyjątkiem długości pojedynczego łańcucha węglowego: krótka grupa metylowa (Q‑C1) oraz dłuższa grupa butylowa (Q‑C4).
Testowanie dwóch małych cząsteczek jako tarcz dla stali
Aby ocenić, jak dobrze te związki chronią stal, zespół zanurzył próbki stali węglowej w silnym kwasie solnym z inhibitorami i bez nich. Dokładne ważenie próbek przed i po ekspozycji pozwoliło określić, ile materiału się rozpuściło. Wykorzystano także testy elektrochemiczne, które śledzą, jak łatwo ładunek elektryczny przemieszcza się na granicy stal–roztwór, dając czułe miary szybkości korozji. W szerokim zakresie stężeń obie cząsteczki znacząco zmniejszały utratę stali, przy czym dłuższy łańcuch Q‑C4 osiągnął niemal 89% ochrony w optymalnych warunkach. Jednak efekt ochronny słabł w wyższych temperaturach, co sugeruje, że warstwa inhibitora staje się mniej stabilna, gdy ciepło ułatwia odłączanie się cząsteczek od powierzchni.
Jak tworzy się i utrzymuje warstwa ochronna
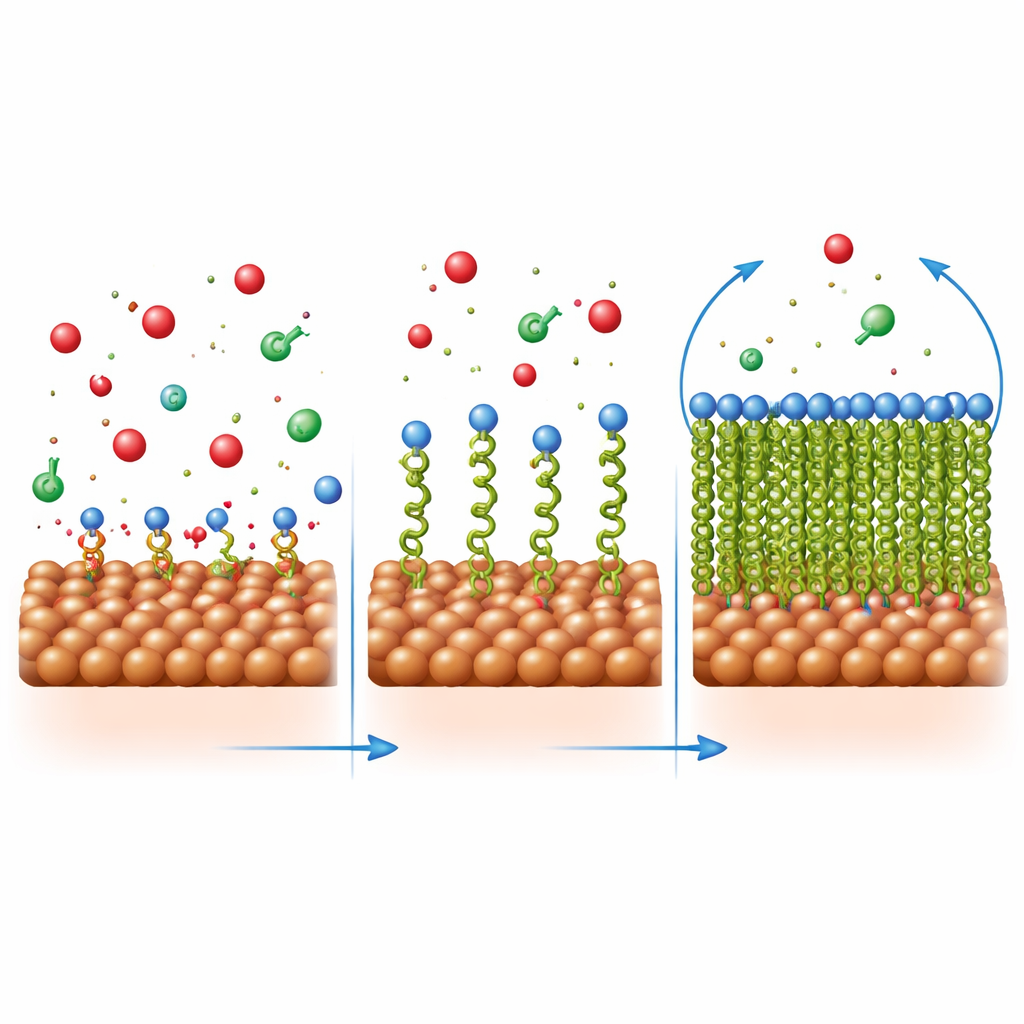
Naukowcy zbadali, w jaki sposób te cząsteczki układają się na stali, analizując, jak zmianie ulega pokrycie wraz ze stężeniem. Wzorzec odpowiadał prostemu modelowi „jednej warstwy”, co oznacza, że każda cząsteczka inhibitora zajmuje odrębne miejsce na powierzchni, zamiast układać się w grube stosy. Obliczenia zmian energii wykazały, że przyczepność obejmuje zarówno oddziaływania fizyczne (przez różnice ładunków), jak i wiązania chemiczne (przez dzielenie się elektronami z metalem). Obrazy mikroskopowe potwierdziły ten obraz: niechroniona stal w kwasie rozwijała dziury i pęknięcia, podczas gdy stal w roztworze z inhibitorem była znacznie gładsza, pokryta bardziej jednolitą warstwą. Analiza pierwiastkowa i spektroskopia w podczerwieni potwierdziły, że związki organiczne rzeczywiście były obecne na powierzchni stali i że ich grupy wiążące wchodziły w interakcje z atomami żelaza.
Dlaczego dłuższy łańcuch działa lepiej
Chociaż obie cząsteczki mają tę samą „głowę” chwytającą stal, ich „ogona” zachowują się inaczej. Dłuższy łańcuch butylowy w Q‑C4 jest bardziej hydrofobowy niż krótki łańcuch metylowy w Q‑C1. Gdy grupa głowy zakotwiczy się do metalu, ogon pomaga zbudować grubszą, bardziej ciągłą warstwę, która trzyma kwaśny roztwór na dystans. Symulacje komputerowe oparte na teorii funkcjonału gęstości potwierdziły to: dla Q‑C4 obliczono nieco silniejszą zdolność do oddawania elektronów i bardziej miękką strukturę elektroniczną, co sprzyja silniejszej interakcji z metalem. Te cechy razem pomagają Q‑C4 lepiej się upakować i tworzyć skuteczniejszą barierę, pozostawiając mniej odsłoniętych miejsc, gdzie może rozpocząć się korozja.
Co to znaczy dla ochrony stali w praktyce
Mówiąc prosto, badanie pokazuje, że bardzo proste, niskokosztowe cząsteczki organiczne mogą zapewnić stali węglowej istotną ochronę w agresywnych środowiskach kwaśnych, a modyfikacja tak pozornie drobnej cechy jak długość łańcucha węglowego może przynieść zauważalną różnicę. Inhibitor o dłuższym ogonie tworzy gęściejszą, bardziej odporną powłokę, znacznie zmniejszając korozję w porównaniu z krótszym krewnym. Choć ochrona maleje w wyższych temperaturach, praca ta dostarcza jasnego wskazania: poprzez dostosowanie struktury cząsteczkowej, zwłaszcza długości łańcucha, inżynierowie mogą projektować dopasowane inhibitory, które są łatwiejsze do wytworzenia, skuteczne w niskich dawkach i odpowiednie do szerokiego zastosowania przemysłowego, by utrzymać konstrukcje stalowe bezpieczniejsze i trwalsze.
Cytowanie: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Słowa kluczowe: korozja stali węglowej, inhibitory korozji, związki chinazolinonowe, środowiska kwaśne, ochrona powierzchni