Clear Sky Science · fr
Effet de la longueur de la chaîne alkyle sur la performance d'inhibition de la corrosion des dérivés de 2‑thioxo‑2,3‑dihydroquinazolin‑4(1H)‑one pour l'acier au carbone en solution HCl
Protéger les métaux du quotidien contre les dommages invisibles
Des ponts et des bâtiments aux voitures et aux appareils ménagers, l'acier au carbone soutient discrètement une grande partie de la vie moderne. Mais ce métal robuste a une faiblesse : dans les milieux acides, comme ceux utilisés pour nettoyer des équipements industriels ou pour traiter le pétrole et le gaz, il peut se dissoudre étonnamment vite. Cette étude examine si deux petites molécules organiques faciles à synthétiser peuvent agir comme des boucliers invisibles sur l'acier, ralentissant ce dommage silencieux et prolongeant la durée de vie des infrastructures essentielles.
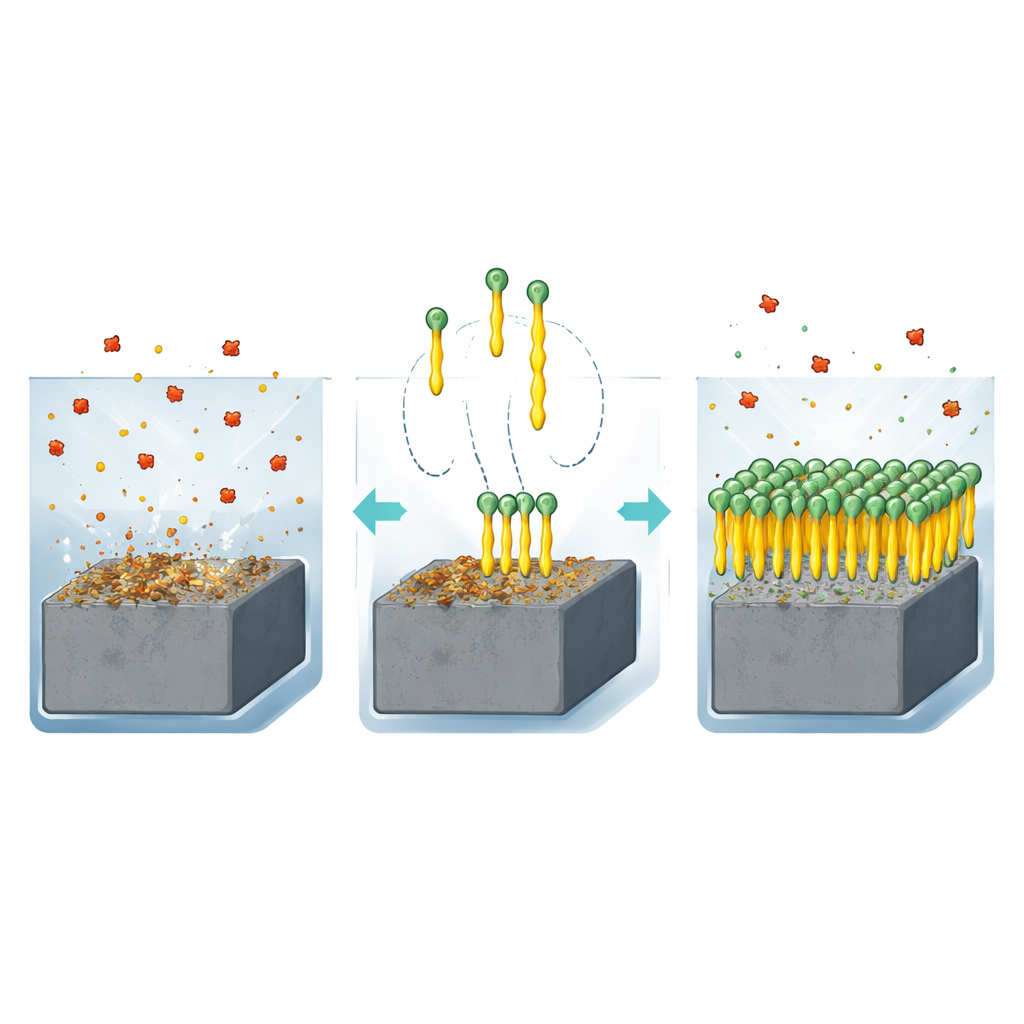
Pourquoi l'acier a besoin d'un garde du corps chimique
Quand l'acier au carbone est plongé dans un liquide acide tel que l'acide chlorhydrique, des atomes à sa surface réagissent et se détachent dans la solution. Avec le temps, cette corrosion peut amincir les tuyaux, affaiblir les réservoirs et compromettre la sécurité. L'une des méthodes les plus pratiques pour combattre ce processus consiste à ajouter de faibles quantités de molécules spéciales appelées inhibiteurs dans le liquide. Ces molécules se fixent à la surface de l'acier et forment un film protecteur qui empêche toute attaque supplémentaire. Les auteurs se sont concentrés sur une famille de composés connus sous le nom de quinazolinones, qui contiennent des atomes d'azote, de soufre et d'oxygène capables de s'accrocher fortement au métal. Ils ont conçu deux versions très simples, identiques sauf pour la longueur d'une seule chaîne carbonée : un groupe méthyle court (Q‑C1) et un groupe butyle plus long (Q‑C4).
Tester deux petites molécules comme boucliers pour l'acier
Pour évaluer l'efficacité de ces composés, l'équipe a immergé des échantillons d'acier au carbone dans de l'acide chlorhydrique concentré avec et sans inhibiteurs. En pesant soigneusement les échantillons avant et après l'exposition, ils ont pu déterminer la quantité de métal dissoute. Ils ont également utilisé des tests électrochimiques, qui suivent la facilité avec laquelle la charge électrique circule à l'interface acier‑solution, fournissant une mesure sensible du taux de corrosion. Sur une gamme de concentrations, les deux molécules ont considérablement réduit la perte d'acier, le composé à chaîne plus longue Q‑C4 atteignant près de 89 % de protection dans ses meilleures conditions. Cependant, l'effet protecteur s'est affaibli à des températures plus élevées, ce qui suggère que le film inhibiteur devient moins stable lorsque la chaleur favorise le détachement des molécules de la surface.
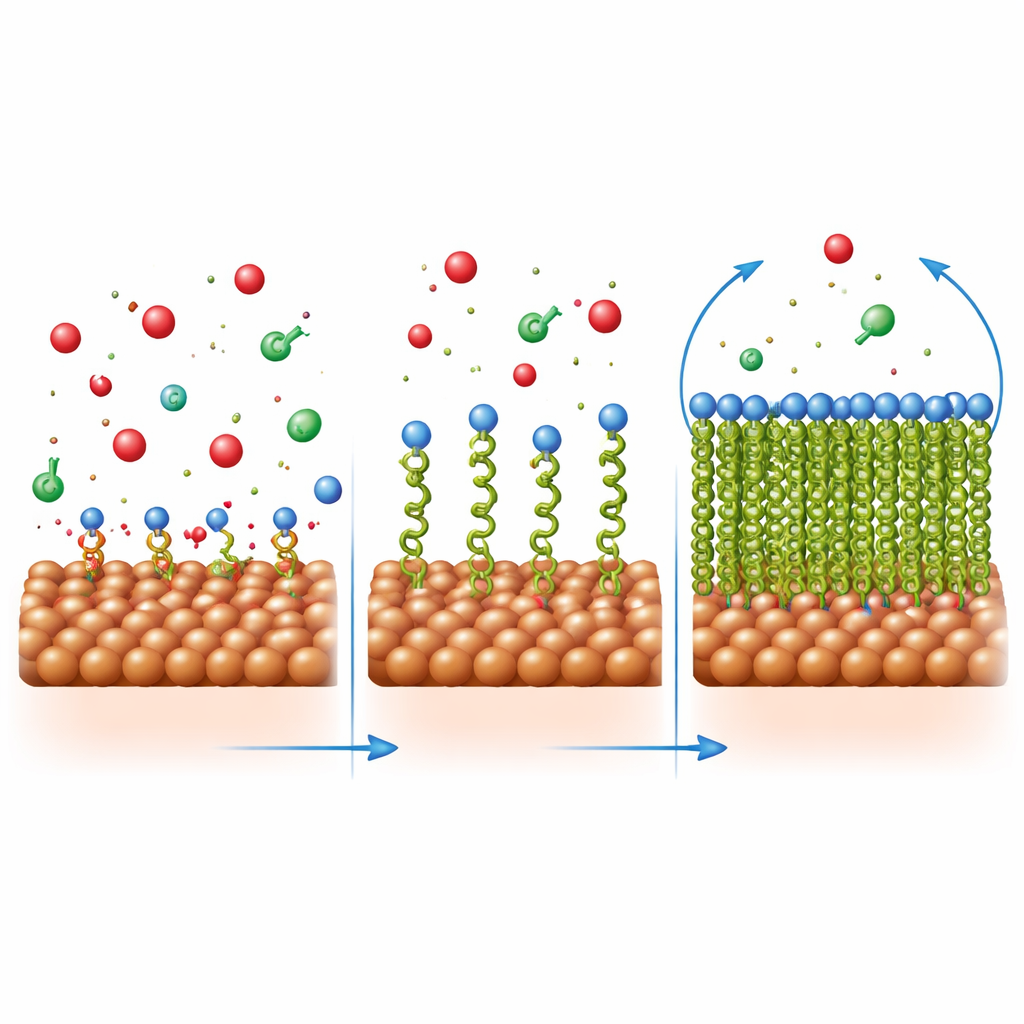
Comment le film protecteur se forme et se maintient
Les chercheurs ont sondé la manière dont ces molécules s'installent sur l'acier en analysant la variation de la couverture en fonction de la concentration. Le schéma a suivi un modèle simple de « couche unique », ce qui signifie que chaque molécule d'inhibiteur occupe un emplacement distinct sur la surface plutôt que de s'empiler en couches épaisses. Des calculs des variations d'énergie ont montré que la fixation implique à la fois une attraction physique (par différences de charge) et une liaison chimique (par partage d'électrons avec le métal). Des images microscopiques ont corroboré ce tableau : l'acier nu plongé dans l'acide présentait des piqûres et des fissures, tandis que l'acier dans l'acide contenant l'inhibiteur paraissait beaucoup plus lisse, couvert d'une couche plus uniforme. L'analyse élémentaire et la spectroscopie infrarouge ont confirmé que les molécules organiques étaient bien présentes à la surface de l'acier et que leurs groupes de liaison avaient interagi avec les atomes de fer.
Pourquoi la chaîne plus longue est plus efficace
Bien que les deux molécules partagent la même « tête » qui s'accroche à l'acier, leurs « queues » se comportent différemment. La longue chaîne butyle de Q‑C4 est plus hydrophobe que la courte chaîne méthyle de Q‑C1. Une fois le groupe tête ancré au métal, cette queue contribue à former un film plus épais et plus homogène qui maintient la solution acide à distance. Des simulations informatiques basées sur la théorie de la fonctionnelle de la densité ont confirmé cela : Q‑C4 a été calculé comme ayant une capacité légèrement supérieure à donner des électrons et une structure électronique plus molle, favorisant une interaction plus forte avec le métal. Ces caractéristiques aident Q‑C4 à se compacter davantage et à former une barrière plus efficace, laissant moins de zones exposées où la corrosion peut démarrer.
Ce que cela signifie pour la protection de l'acier en conditions réelles
En termes simples, l'étude montre que des molécules organiques très simples et peu coûteuses peuvent apporter une protection substantielle à l'acier au carbone dans des environnements acides sévères, et que modifier quelque chose d'aussi modeste que la longueur d'une chaîne carbonée peut faire une différence perceptible. L'inhibiteur à queue plus longue forme un revêtement plus dense et plus résistant, réduisant la corrosion bien davantage que son homologue plus court. Si la protection diminue à des températures élevées, ce travail fournit une feuille de route claire : en ajustant la structure moléculaire, en particulier la longueur de la chaîne, les ingénieurs peuvent concevoir des inhibiteurs sur mesure, plus faciles à produire, efficaces à faibles doses et adaptés à une utilisation à grande échelle dans l'industrie pour préserver les structures en acier plus longtemps et en meilleure sécurité.
Citation: El-Maksoud, S.A.A., Fathalla, W., Saleh, M.S. et al. Effect of alkyl chain length on the corrosion inhibition performance of 2-thioxo-2,3-dihydroquinazolin-4(1H)-one derivatives for carbon steel in HCl solution. Sci Rep 16, 10982 (2026). https://doi.org/10.1038/s41598-026-40197-z
Mots-clés: corrosion de l'acier au carbone, inhibiteurs de corrosion, composés quinazolinone, environnements acides, protection des surfaces