Clear Sky Science · ru
Дальнодействующая химическая сигнализация in vivo регулируется механическими сигналами
Как прикосновение формирует растущий мозг
Когда мозг принимает форму, миллиарды молодых нервных клеток должны пройти длинные и извилистые пути, чтобы найти своих правильных партнеров. На протяжении десятилетий учёным было известно, что эти путешествия направляются химическими сигналами, которые распространяются по ткани, как невидимые запахи. В этом исследовании выявлен неожиданный партнёр этих химических подсказок: физическая жёсткость самого мозга. Тщательно исследовав развивающиеся мозги лягушек, авторы показывают, что степень твёрдости или мягкости ткани может включать или выключать дальнодействующие химические сигналы, в конечном счёте направляя растущие нервные волокна по правильным маршрутам.
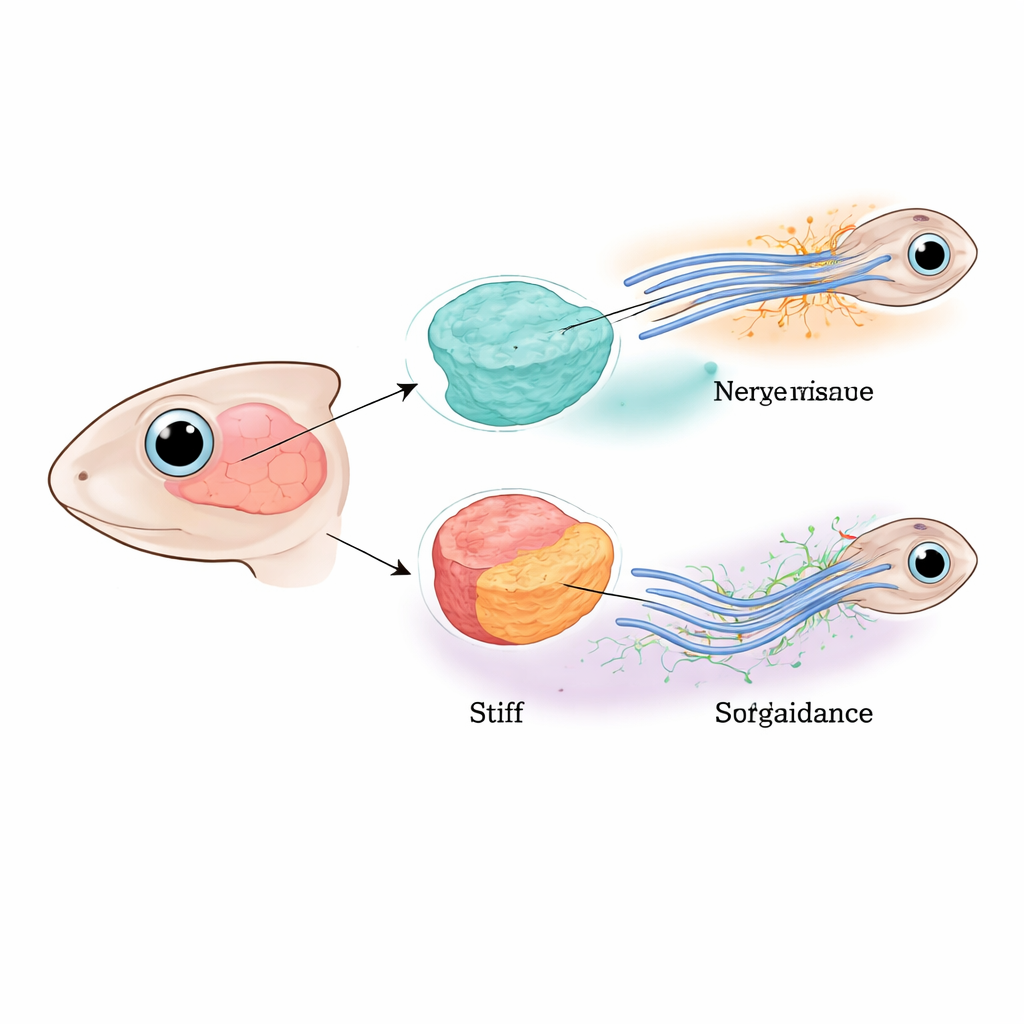
Направляя нервы через молодой мозг
Исследователи сосредоточились на оптическом пути у молодых африканских роговатых лягушек, где нервные волокна из глаза должны пересечь мозг и выполнить точный поворот перед достижением целевой области. Предыдущие работы показали, что эти волокна направляются как диффундирующими химическими репеллентами, так и постепенным изменением жёсткости ткани вдоль их пути. В этой работе команда разделила роли самих нейронов и окружающей мозговой ткани, выборочно уменьшая ключевой «датчик силы» — белок Piezo1 — либо в самих волокнах, либо в соседних клетках мозга, либо в обоих. Когда Piezo1 отсутствовал повсеместно, многие волокна задерживались, распадались или съезжали с курса, что подтверждает: корректное механическое ощущение необходимо для правильного формирования проводящих путей мозга.
Когда мозг размягчается, дальнодействующие сигналы ослабевают
Далее авторы спросили, как окружающая мозговая ткань способствует этой системе навигации. Когда они удаляли Piezo1 только из нервных волокон, жёсткость ткани оставалась нормальной, но ошибки в проводимости всё же возникали, указывая на то, что волокна больше не могли адекватно ощущать своё механическое окружение. Поразительно, что при удалении Piezo1 из самой мозговой ткани она становилась почти вдвое мягче, и ошибок в наведении становилось ещё больше — хотя в нервных волокнах Piezo1 всё ещё присутствовал. В этих размягчённых областях уровни двух известных дальнодействующих молекул навигации, Slit1 и Semaphorin3A, резко падали как на уровне РНК, так и на уровне белка. Это показало, что физическое состояние мозга не просто пассивно воспринимается клетками; оно активно контролирует, сколько этих диффундирующих химических подсказок производится.
Клеточная адгезия как скрытый механический рычаг
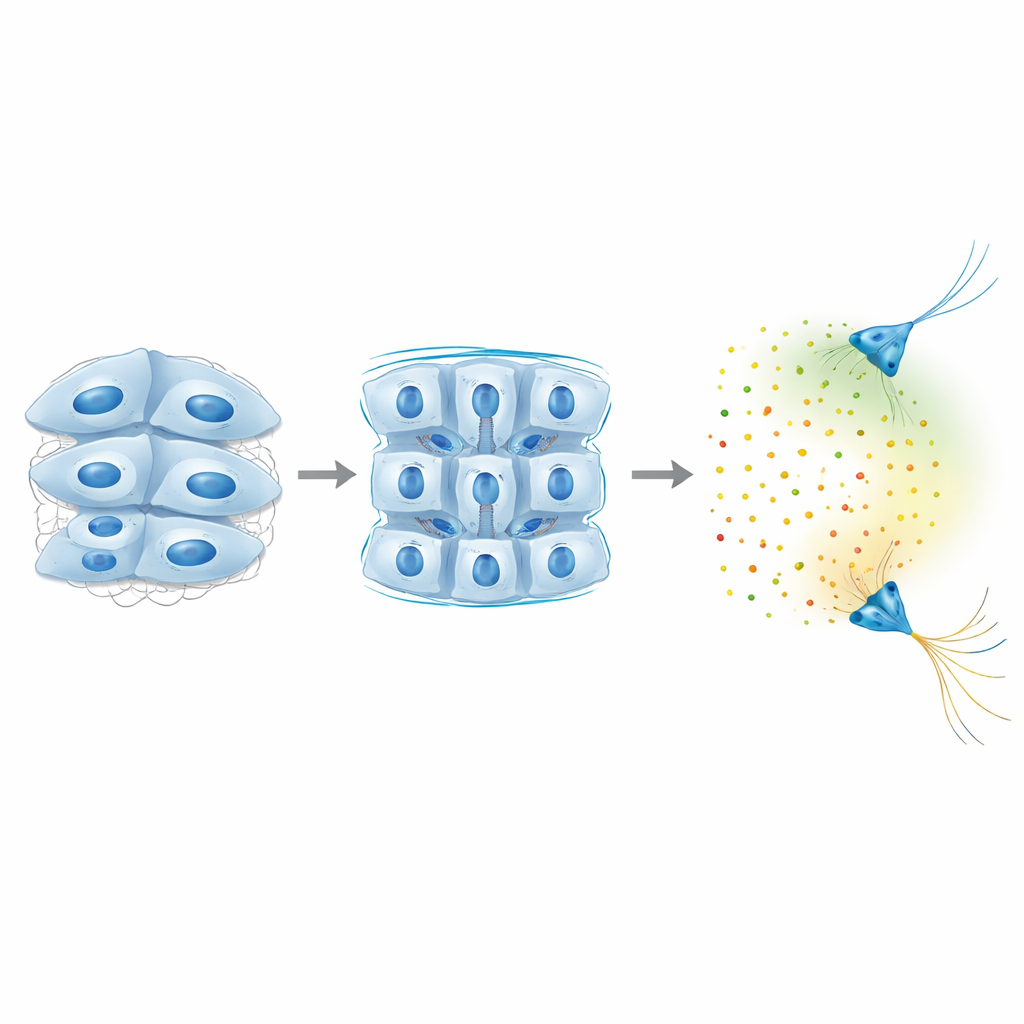
Почему ткань мозга становится мягче при дефиците Piezo1? Команда исключила простые объяснения, такие как уменьшение числа клеток или повышенная мягкость отдельных клеток. Вместо этого они обнаружили, что основные белки, скрепляющие соседние клетки мозга — NCAM1 и N-кадгерин — снижались при падении уровней Piezo1. Когда исследователи непосредственно уменьшали эти адгезионные белки, жёсткость ткани уменьшалась, а уровни Semaphorin3A тоже падали, хотя внутриклеточная механика оставалась без изменений. Это указывает на цепочку событий, в которой активность Piezo1 помогает поддерживать прочные клеточно-клеточные связи, что в свою очередь задаёт суммарную жёсткость ткани, а та затем определяет, в каком объёме ткань продуцирует определённые дальнодействующие химические сигналы.
Подкручивание механического регулятора
Чтобы проверить обратную сторону этой связи, авторы повысили жёсткость мозга несколькими способами. В лабораторных чашках они помещали небольшие кусочки мягкой мозговой ткани в 3D-гели различной жёсткости. В более жёстких гелях ткань сильнее тянула окружающую среду и начинала продуцировать гораздо большие уровни Slit1 и Semaphorin3A, даже в областях, которые обычно не вырабатывают эти сигналы. В целых головастиках они либо применяли препарат, усиливающий внутриклеточный контрактильный тонус, либо мягко сжимали отдельные участки мозга крошечным зондом. Обе подхода делали выбранные области жёстче и вызывали новую продукцию Semaphorin3A в регионах, обычно химически тихих. Однако этот механический «переключатель» не сработал у животных с пониженным уровнем Piezo1, что показывает: для трансляции повышенной жёсткости в усиленную химическую сигнализацию канал необходим.
Почему это важно для растущего и больного мозга
В целом исследование выявляет петлю обратной связи, в которой клетки мозга тянут и ощущают свое окружение через Piezo1, регулируют свои адгезионные связи, чтобы задать жёсткость ткани, и лишь при достижении пороговой жёсткости включают дальнодействующие химические сигналы, направляющие отдалённые нервные волокна. Механические и химические сигналы не действуют независимо друг от друга, а тесно переплетены: локальное изменение твёрдости ткани может изменить «химическую погоду» в отдалённых областях, влияя на то, куда растут аксоны и как формируются цепи. Этот вывод предполагает, что изменённая жёсткость ткани — наблюдаемая при травме мозга или нейродегенерации — может отозваться по всему развивающемуся или стареющему мозгу, меняя сами сигналы, которыми клетки обмениваются на больших расстояниях.
Цитирование: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Ключевые слова: механотрансдукция, направление аксонов, жесткость ткани, Piezo1, развитие мозга