Clear Sky Science · es
La señalización química a larga distancia in vivo está regulada por señales mecánicas
Cómo el tacto moldea los cerebros en crecimiento
Mientras un cerebro toma forma, miles de millones de neuronas jóvenes deben recorrer trayectos largos y sinuosos para encontrar a sus parejas correctas. Durante décadas, los científicos han sabido que estos desplazamientos están guiados por señales químicas que se dispersan como aromas invisibles a través del tejido. Este estudio revela un compañero sorprendente de esas señales químicas: la rigidez física del propio cerebro. Al sondear cuidadosamente cerebros de ranas en desarrollo, los autores muestran que cuán firme o blando es el tejido puede activar o desactivar señales químicas a distancia, dirigiendo en última instancia las fibras nerviosas en crecimiento por las rutas adecuadas.
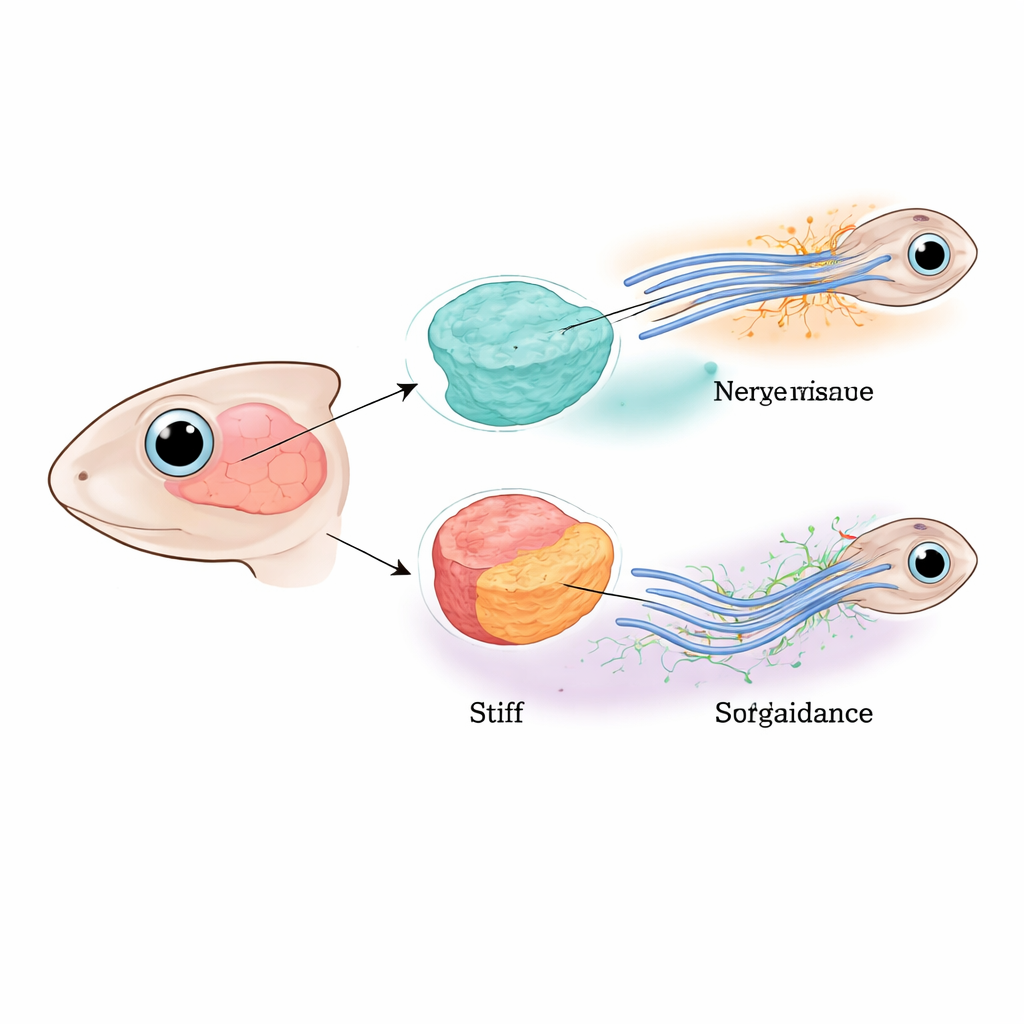
Guiando nervios a través del cerebro joven
Los investigadores se centraron en la vía óptica de renacuajos de la rana africana Xenopus, donde las fibras nerviosas procedentes del ojo deben cruzar el cerebro y ejecutar un giro preciso antes de alcanzar su región diana. Trabajos anteriores mostraron que estas fibras son dirigidas tanto por repelentes químicos en difusión como por un cambio gradual en la rigidez del tejido a lo largo de su trayecto. Aquí, el equipo separó los papeles de las propias neuronas y del tejido cerebral circundante reduciendo selectivamente una proteína sensor de fuerzas clave llamada Piezo1, ya fuera en las propias fibras nerviosas, en las células cerebrales vecinas o en ambas. Cuando Piezo1 faltaba por doquier, muchas fibras se detenían, se dividían o se desviaban de su curso, lo que confirma que la detección mecánica adecuada es esencial para cablear el cerebro.
Cuando el cerebro se ablanda, las señales a larga distancia se apagan
A continuación, los autores preguntaron cómo contribuye el tejido cerebral circundante a este sistema de guía. Cuando eliminaron Piezo1 solo de las fibras nerviosas, la rigidez del tejido permaneció normal, pero aun así ocurrieron errores de orientación, lo que indica que las fibras ya no podían percibir correctamente su entorno mecánico. De forma llamativa, cuando Piezo1 se eliminó del tejido cerebral, el tejido se volvió casi el doble de blando y los errores de guía aumentaron aún más, a pesar de que las fibras nerviosas todavía contenían Piezo1. En estas regiones ablandadas, los niveles de dos moléculas de guía de largo alcance conocidas, Slit1 y Semaphorin3A, cayeron drásticamente tanto a nivel de ARN como de proteína. Esto demostró que el estado físico del cerebro no era solo percibido pasivamente por las células; controlaba activamente cuánto de estas señales químicas difusibles se producía.
La adhesión celular como una palanca mecánica oculta
¿Qué hace que el tejido cerebral deficiente en Piezo1 sea más blando? El equipo descartó explicaciones simples como menos células o células individuales más flácidas. En su lugar, encontraron que proteínas importantes que cohesionan las células cerebrales vecinas —NCAM1 y N-cadherina— se reducían cuando descendían los niveles de Piezo1. Cuando los investigadores redujeron directamente estas proteínas de adhesión, la rigidez del tejido disminuyó y los niveles de Semaphorin3A también cayeron, aunque el interior de las células permaneciera mecánicamente inalterado. Esto apunta a una cadena de eventos en la que la actividad de Piezo1 ayuda a mantener fuertes conexiones célula–célula, que a su vez fijan la rigidez global del tejido y, posteriormente, gobiernan cuánto de ciertas señales químicas de largo alcance produce el tejido.
Subiendo el dial mecánico
Para probar la cara opuesta de esta relación, los autores aumentaron la rigidez cerebral de varias maneras. En placas de laboratorio, incrustaron pequeños trozos de tejido cerebral blando en geles 3D blandos o rígidos. En geles más rígidos, el tejido tiró con más fuerza de su entorno y empezó a producir niveles mucho más altos de Slit1 y Semaphorin3A, incluso en regiones que normalmente no sintetizan estas señales. En renacuajos intactos, aplicaron ya sea un fármaco que potencia las fuerzas contráctiles internas o comprimieron suavemente regiones cerebrales específicas con una pequeña sonda. Ambos enfoques endurecieron las zonas elegidas y dispararon la producción de nueva Semaphorin3A en áreas que habitualmente son químicamente silenciosas. Sin embargo, este “interruptor” mecánico falló en animales donde Piezo1 había sido reducido, mostrando que este canal es necesario para traducir la mayor rigidez en mayor señalización química.
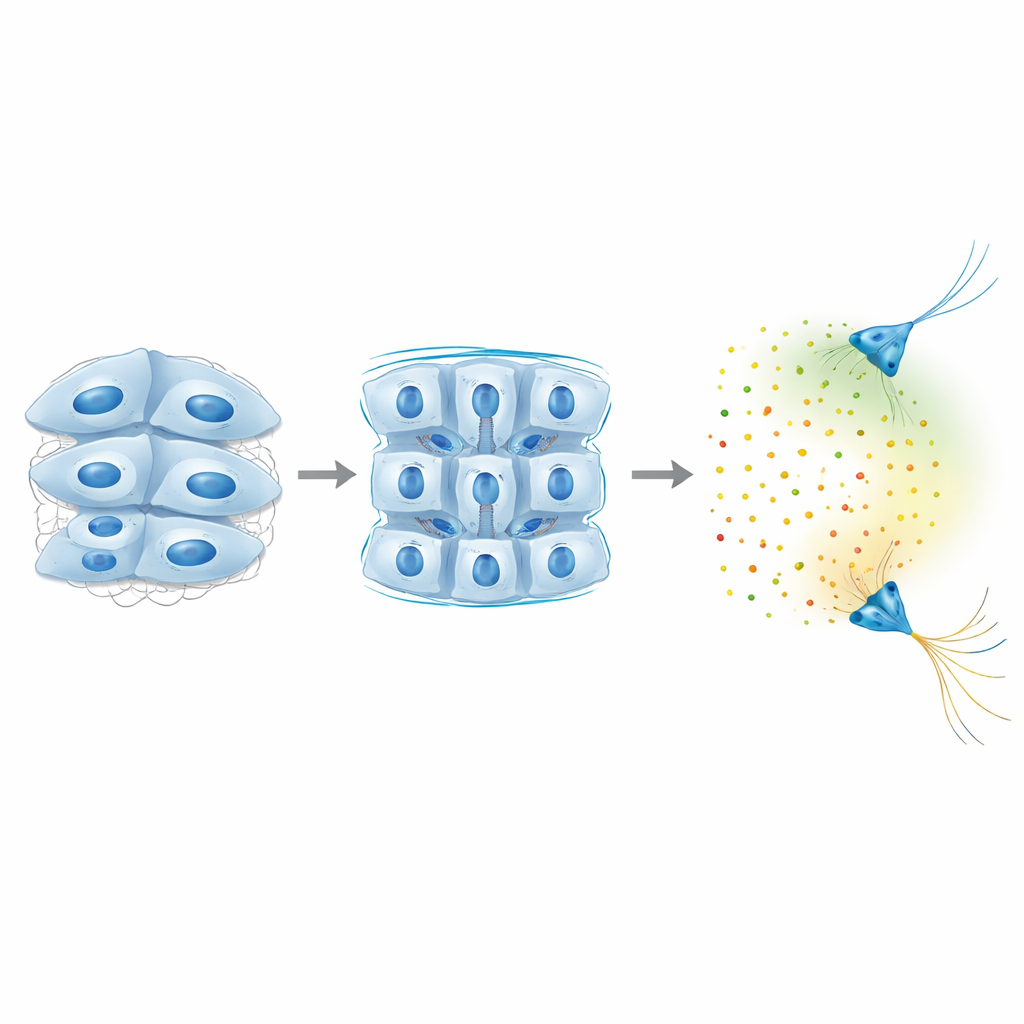
Por qué esto importa para cerebros en crecimiento y enfermos
En conjunto, el estudio revela un bucle de realimentación en el que las células cerebrales tiran y sienten su entorno a través de Piezo1, ajustan sus conexiones adhesivas para fijar la rigidez del tejido y, solo cuando se alcanza un umbral de rigidez, activan señales químicas de largo alcance que guían fibras nerviosas distantes. En lugar de actuar de forma independiente, las señales mecánicas y químicas están estrechamente entrelazadas: un cambio local en la firmeza del tejido puede remodelar el “clima químico” a distancia, influyendo en dónde crecen los axones y cómo se forman los circuitos. Esta idea sugiere que la rigidez tisular alterada —observada en condiciones que van desde lesiones cerebrales hasta neurodegeneración— podría repercutir en cerebros en desarrollo o envejecientes al cambiar las mismas señales que las células usan para comunicarse a larga distancia.
Cita: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Palabras clave: mecanotransducción, guía de axones, rigidez tisular, Piezo1, desarrollo cerebral