Clear Sky Science · fr
La signalisation chimique à longue portée in vivo est régulée par des signaux mécaniques
Comment le toucher façonne les cerveaux en croissance
Lorsque le cerveau prend forme, des milliards de jeunes neurones doivent parcourir des trajets longs et sinueux pour trouver leurs partenaires corrects. Depuis des décennies, les scientifiques savent que ces voyages sont guidés par des signaux chimiques qui se diffusent comme des parfums invisibles dans le tissu. Cette étude révèle un partenaire surprenant de ces indices chimiques : la rigidité physique du cerveau lui‑même. En sondant soigneusement des cerveaux de grenouilles en développement, les auteurs montrent que la fermeté ou la souplesse du tissu peut activer ou désactiver des signaux chimiques distants, orientant finalement les fibres nerveuses en croissance le long des voies appropriées.
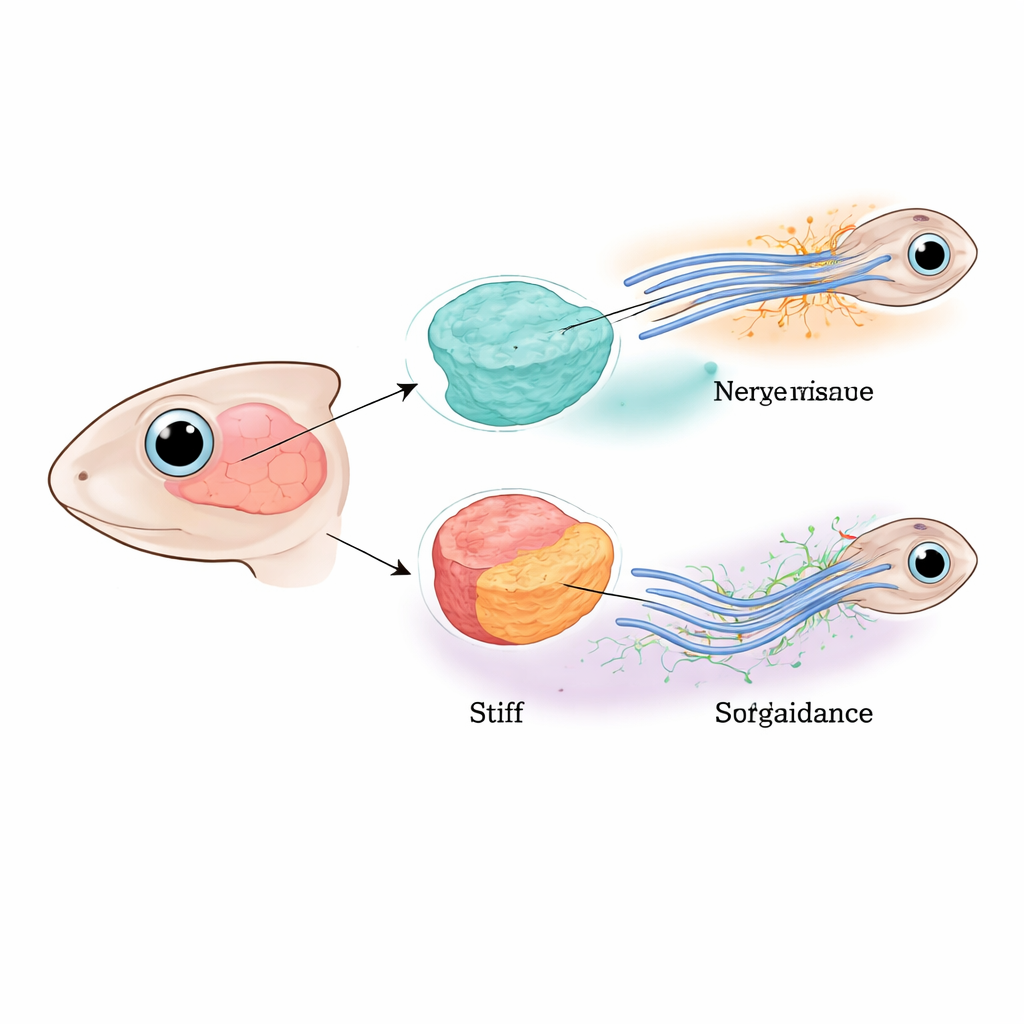
Guider les nerfs à travers le jeune cerveau
Les chercheurs se sont concentrés sur la voie optique de jeunes Xenopus, où les fibres nerveuses issues de l’œil doivent traverser le cerveau et effectuer un virage précis avant d’atteindre leur région cible. Des travaux antérieurs montraient que ces fibres sont dirigées à la fois par des répulsifs chimiques diffusifs et par un gradient progressif de raideur tissulaire le long de leur trajet. Ici, l’équipe a démêlé les rôles des neurones eux‑mêmes et du tissu cérébral environnant en réduisant sélectivement une protéine clé de “capteur de force” appelée Piezo1 soit dans les fibres nerveuses, soit dans les cellules cérébrales voisines, soit dans les deux. Lorsque Piezo1 manquait partout, de nombreuses fibres s’arrêtaient, se divisaient ou déviaient de leur trajectoire, confirmant que la détection mécanique correcte est essentielle pour câbler le cerveau.
Quand le cerveau s’assouplit, les signaux à longue distance s’estompent
Ensuite, les auteurs ont cherché à savoir comment le tissu cérébral environnant contribue à ce système de guidage. Lorsque Piezo1 a été retiré uniquement des fibres nerveuses, la raideur du tissu est restée normale, mais des erreurs de guidage sont apparues, indiquant que les fibres ne pouvaient plus percevoir correctement leur environnement mécanique. De manière frappante, lorsque Piezo1 a été supprimé dans le tissu cérébral, celui‑ci est devenu presque deux fois plus souple, et les erreurs de guidage sont devenues encore plus fréquentes—même si les fibres nerveuses contenaient toujours Piezo1. Dans ces régions assouplies, les niveaux de deux molécules de guidage à longue portée connues, Slit1 et Semaphorine3A, ont chuté fortement tant au niveau de l’ARN que de la protéine. Cela montre que l’état physique du cerveau n’était pas seulement perçu passivement par les cellules ; il contrôlait activement la quantité de ces indices chimiques diffusifs produite.
L’adhésion cellulaire comme levier mécanique caché
Qu’est‑ce qui rend le tissu cérébral déficient en Piezo1 plus souple ? L’équipe a écarté des explications simples comme un nombre réduit de cellules ou des cellules individuelles plus molles. À la place, ils ont constaté que des protéines majeures qui collent les cellules cérébrales voisines entre elles—NCAM1 et N‑cadherine—étaient diminuées lorsque les niveaux de Piezo1 baissaient. Lorsque les chercheurs ont abaissé directement ces protéines d’adhésion, la raideur tissulaire a diminué et les niveaux de Semaphorine3A ont également chuté, même si l’intérieur des cellules restait mécaniquement inchangé. Cela pointe vers une chaîne d’événements dans laquelle l’activité de Piezo1 aide à maintenir des connexions cellule–cellule fortes, qui à leur tour déterminent la rigidité globale du tissu, laquelle gouverne ensuite la production de certains signaux chimiques à longue portée.
Monter le cadran mécanique
Pour tester l’autre face de cette relation, les auteurs ont augmenté la raideur cérébrale de plusieurs façons. en culture, ils ont incorporé de petits morceaux de tissu cérébral mou soit dans des gels 3D mous soit dans des gels rigides. Sur des gels plus rigides, le tissu tirait plus fort sur son environnement et a commencé à produire des niveaux bien plus élevés de Slit1 et de Semaphorine3A, même dans des régions qui ne fabriquent normalement pas ces indices. Chez des têtards intacts, ils ont soit appliqué un médicament qui renforce les forces contractiles internes, soit comprimé doucement des régions cérébrales spécifiques avec une minuscule sonde. Les deux approches ont rigidifié les régions choisies et déclenché une nouvelle production de Semaphorine3A dans des zones habituellement chimiquement silencieuses. Toutefois, cet « interrupteur » mécanique a échoué chez les animaux où Piezo1 avait été réduit, montrant que ce canal est nécessaire pour traduire une raideur accrue en signalisation chimique accrue.
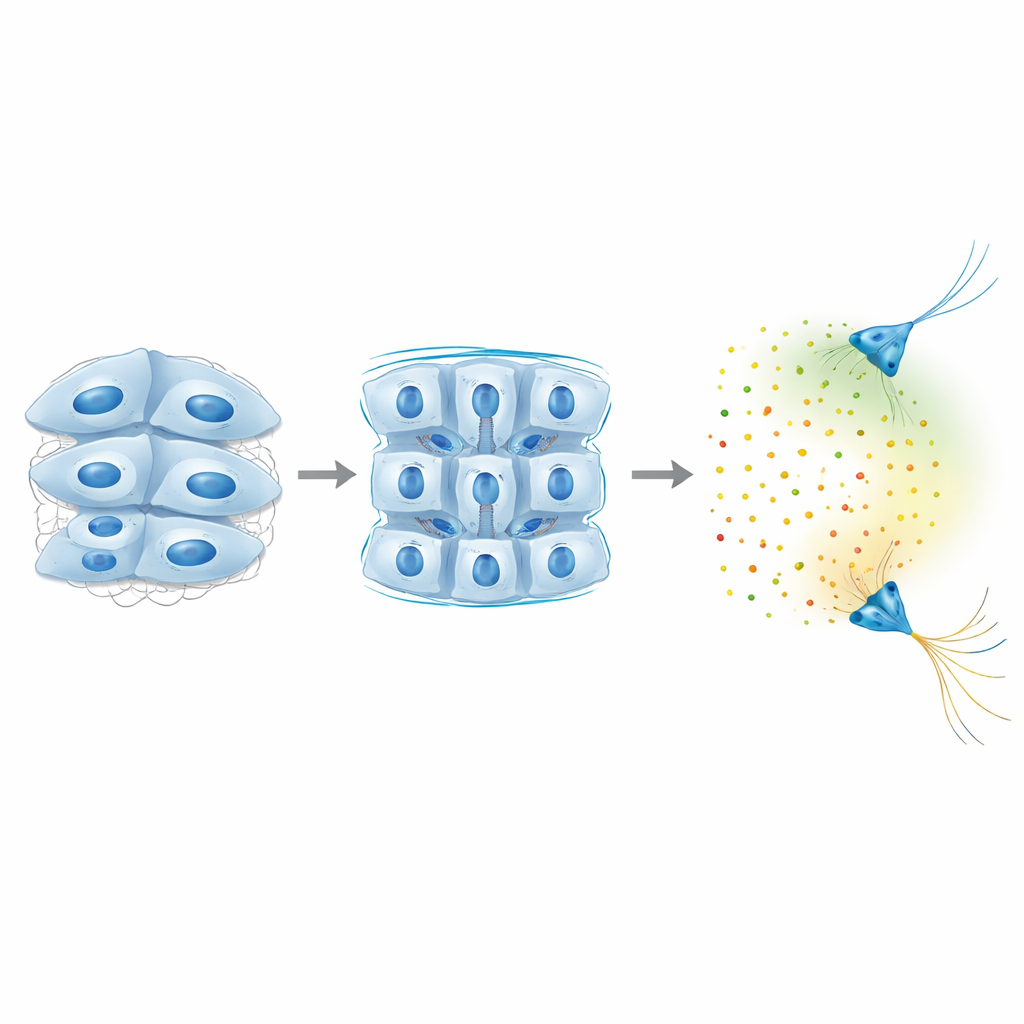
Pourquoi cela compte pour les cerveaux en croissance et malades
Au total, l’étude révèle une boucle de rétroaction dans laquelle les cellules cérébrales tirent sur et sentent leur environnement via Piezo1, ajustent leurs connexions adhésives pour définir la raideur du tissu, et, une fois qu’un seuil de rigidité est atteint, activent des indices chimiques à longue portée qui dirigent des fibres nerveuses distantes. Plutôt que d’agir de manière indépendante, les signaux mécaniques et chimiques sont étroitement imbriqués : un changement local de fermeté tissulaire peut remodeler le « climat chimique » à distance, influençant où les axones poussent et comment les circuits se forment. Cette connaissance suggère que des altérations de la raideur tissulaire—observées dans des états allant des blessures cérébrales à la neurodégénérescence—pourraient résonner à travers les cerveaux en développement ou vieillissants en modifiant les signaux mêmes que les cellules utilisent pour communiquer sur de longues distances.
Citation: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Mots-clés: mécanotransduction, guidage des axones, raideur tissulaire, Piezo1, développement cérébral