Clear Sky Science · it
La segnalazione chimica a lunga distanza in vivo è regolata da segnali meccanici
Come il tatto modella i cervelli in crescita
Man mano che un cervello prende forma, miliardi di giovani neuroni devono percorrere traiettorie lunghe e tortuose per trovare i partner corretti. Per decenni, gli scienziati hanno saputo che questi viaggi sono guidati da segnali chimici che si diffondono come odori invisibili attraverso il tessuto. Questo studio rivela un partner sorprendente per quei segnali chimici: la rigidità fisica del cervello stesso. Attraverso attente misure sui cervelli in sviluppo delle rane, gli autori mostrano che la maggiore o minore fermezza del tessuto può attivare o disattivare segnali chimici distanti, indirizzando infine le fibre nervose in crescita lungo le rotte corrette.
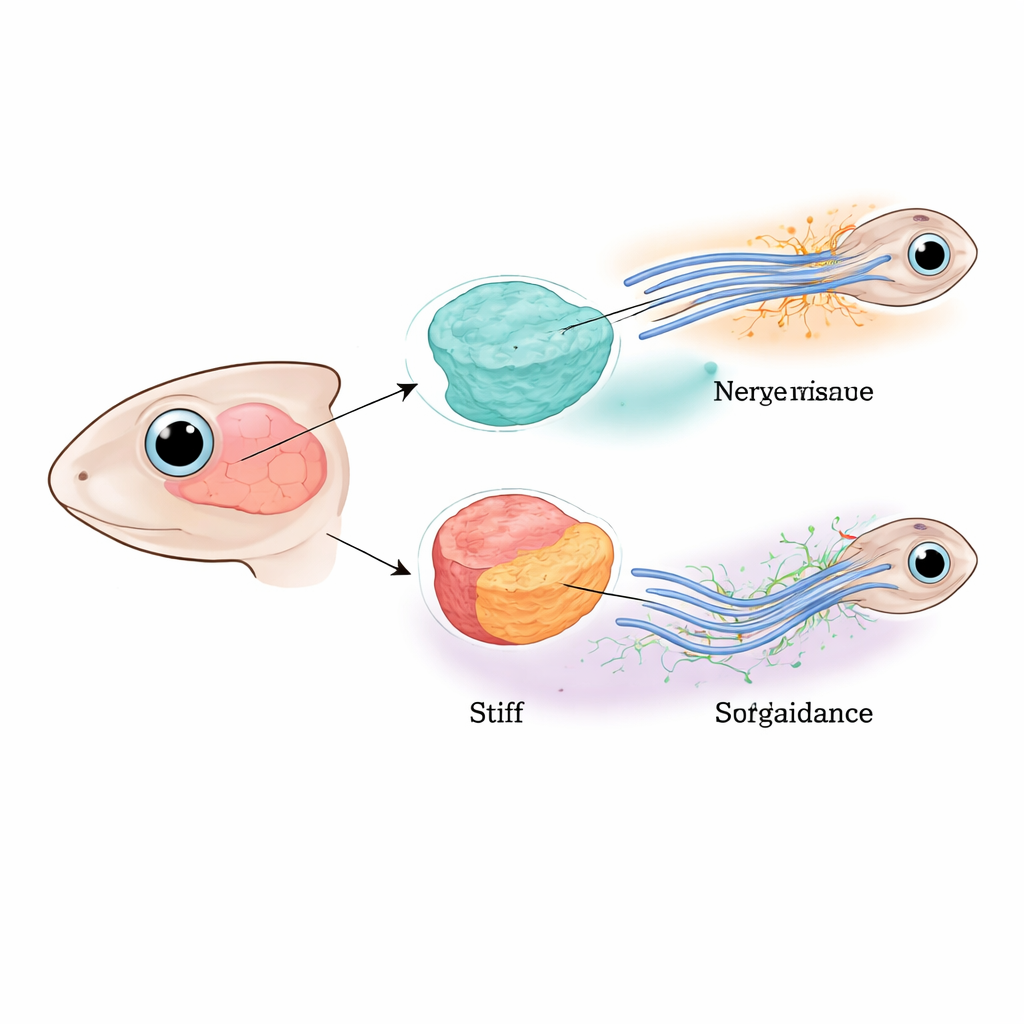
Guidare i nervi attraverso il cervello giovane
I ricercatori si sono concentrati sulla via ottica dei giovani Xenopus (rane dagli artigli africane), dove le fibre nervose dall'occhio devono attraversare il cervello ed effettuare una svolta precisa prima di raggiungere la regione bersaglio. Studi precedenti avevano mostrato che queste fibre vengono indirizzate sia da repellenti chimici diffusi sia da un gradiente di rigidità del tessuto lungo il loro percorso. Qui, il gruppo ha separato i ruoli dei neuroni stessi e del tessuto cerebrale circostante riducendo selettivamente una proteina sensore di forza chiave chiamata Piezo1 nelle sole fibre nervose, nelle cellule cerebrali vicine, o in entrambe. Quando Piezo1 mancava ovunque, molte fibre si bloccavano, si dividevano o deviavano dal percorso, confermando che il corretto senso meccanico è essenziale per il cablaggio del cervello.
Quando il cervello si ammorbida, i segnali a lunga distanza svaniscono
Successivamente, gli autori hanno indagato come il tessuto cerebrale circostante contribuisca a questo sistema di guida. Quando hanno rimosso Piezo1 solo dalle fibre nervose, la rigidità del tessuto rimaneva normale, ma gli errori di percorso continuavano a verificarsi, indicando che le fibre non riuscivano più a percepire correttamente il loro ambiente meccanico. Sorprendentemente, quando Piezo1 è stato rimosso invece dal tessuto cerebrale, il tessuto è diventato quasi il doppio più morbido e gli errori di guida sono aumentati ulteriormente—even se le fibre nervose contenevano ancora Piezo1. In queste regioni ammorbidite, i livelli di due note molecole guida a lunga distanza, Slit1 e Semaphorin3A, sono diminuiti drasticamente sia a livello di RNA sia di proteina. Questo dimostra che lo stato fisico del cervello non era semplicemente percepito dalle cellule in modo passivo; controllava attivamente quanto di questi segnali chimici diffusivi veniva prodotto.
La adesione cellulare come leva meccanica nascosta
Cosa rende il tessuto cerebrale carente di Piezo1 più morbido? Il gruppo ha escluso spiegazioni semplici come meno cellule o singole cellule più flosce. Invece, hanno scoperto che proteine principali che incollano insieme le cellule cerebrali vicine—NCAM1 e N-caderina—erano ridotte quando i livelli di Piezo1 calavano. Quando i ricercatori hanno ridotto direttamente queste proteine di adesione, la rigidità del tessuto è diminuita e anche i livelli di Semaphorin3A sono scesi, nonostante l'interno delle cellule non fosse cambiato meccanicamente. Questo indica una catena di eventi in cui l'attività di Piezo1 contribuisce a mantenere forti connessioni cellula–cellula, che a loro volta determinano la rigidità complessiva del tessuto, la quale regola quanto di certe molecole chimiche a lunga distanza il tessuto produce.
Alzare la manopola meccanica
Per testare l'altro lato di questa relazione, gli autori hanno aumentato la rigidità cerebrale in vari modi. In coltura, hanno immerso piccoli pezzi di tessuto cerebrale morbido in gel 3D morbidi o rigidi. Nei gel più rigidi, il tessuto tirava con maggiore forza sul suo intorno e ha iniziato a produrre livelli molto più alti di Slit1 e Semaphorin3A, anche in regioni che normalmente non producono questi segnali. Nei girini intatti, hanno applicato un farmaco che aumenta le forze contrattile interne o hanno compresso delicatamente regioni cerebrali specifiche con una minuscola sonda. Entrambi gli approcci hanno irrigidito le regioni scelte e innescato la nuova produzione di Semaphorin3A in aree che di solito sono chimicamente silenti. Tuttavia, questo “interruttore” meccanico non ha funzionato negli animali in cui Piezo1 era stato ridotto, mostrando che il canale è necessario per tradurre un aumento di rigidità in un aumento della segnalazione chimica.
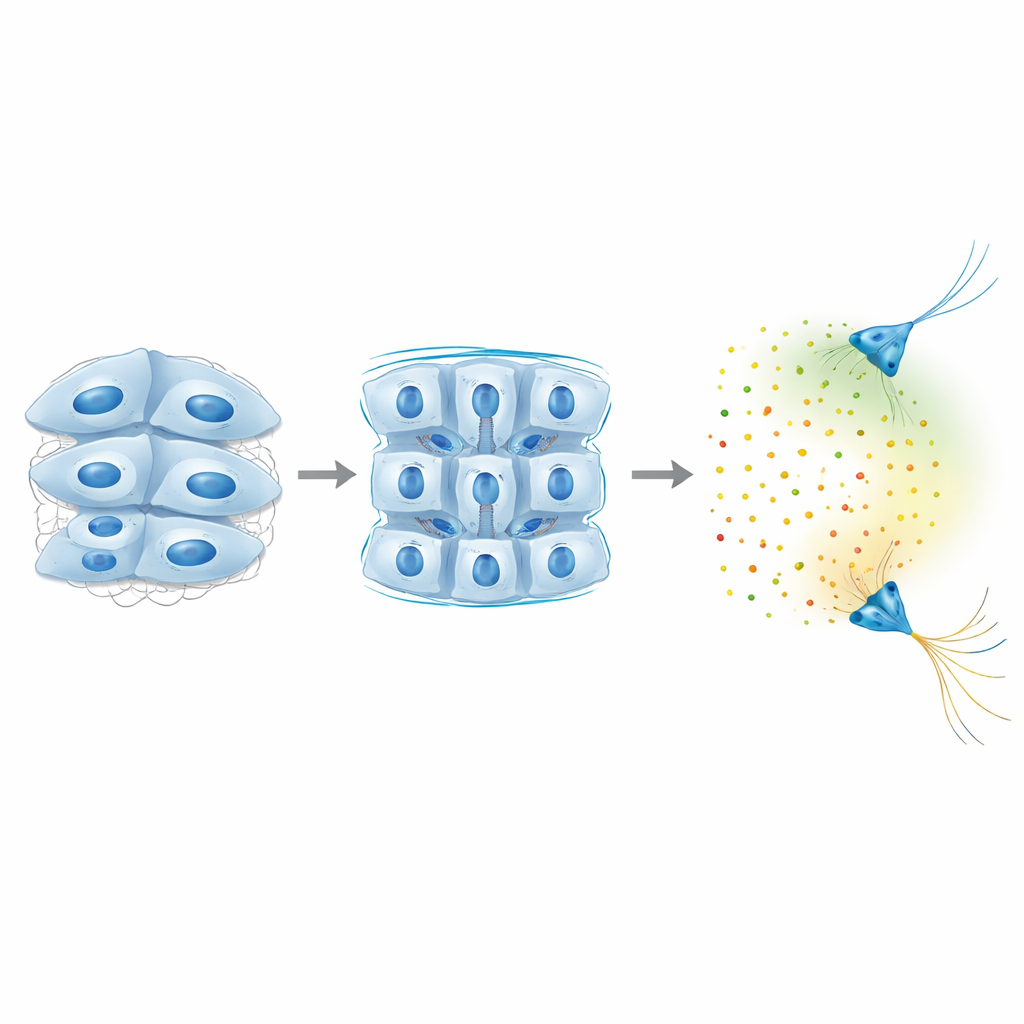
Perché questo conta per cervelli in crescita e malati
Complessivamente, lo studio rivela un circuito di retroazione in cui le cellule cerebrali tirano e percepiscono l'ambiente tramite Piezo1, regolano le loro connessioni adesive per impostare quanto è rigido il tessuto e, solo una volta raggiunta una soglia di rigidità, attivano segnali chimici a lunga distanza che guidano fibre nervose lontane. Piuttosto che agire in modo indipendente, segnali meccanici e chimici sono strettamente intrecciati: un cambiamento locale nella fermezza del tessuto può rimodellare il “clima chimico” lontano, influenzando dove gli assoni crescono e come si formano i circuiti. Questa intuizione suggerisce che una rigidità tissutale alterata—osservata in condizioni che vanno da lesioni cerebrali a neurodegenerazione—potrebbe riverberare attraverso cervelli in sviluppo o invecchiamento modificando i segnali che le cellule usano per comunicare a lunga distanza.
Citazione: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Parole chiave: meccanotrasduzione, indirizzamento degli assoni, rigidità dei tessuti, Piezo1, sviluppo cerebrale