Clear Sky Science · pl
Długodystansowe sygnalizowanie chemiczne in vivo jest regulowane przez sygnały mechaniczne
Jak dotyk kształtuje rosnące mózgi
W miarę formowania się mózgu miliardy młodych komórek nerwowych muszą przebyć długie, kręte trasy, aby odnaleźć właściwych partnerów. Od dziesięcioleci naukowcy wiedzą, że te wędrówki kierowane są przez sygnały chemiczne rozprzestrzeniające się w tkance niczym niewidzialne wonie. Badanie to ujawnia zaskakującego współtowarzysza tych chemicznych wskazówek: fizyczną sztywność samego mózgu. Poprzez precyzyjne sondowanie rozwijających się mózgów żab autorzy pokazują, że to, czy tkanka jest bardziej jędrna czy miękka, może przełączać zdalne sygnały chemiczne — włączać je lub wyłączać — i ostatecznie kierować rosnącymi włóknami nerwowymi na właściwe trasy.
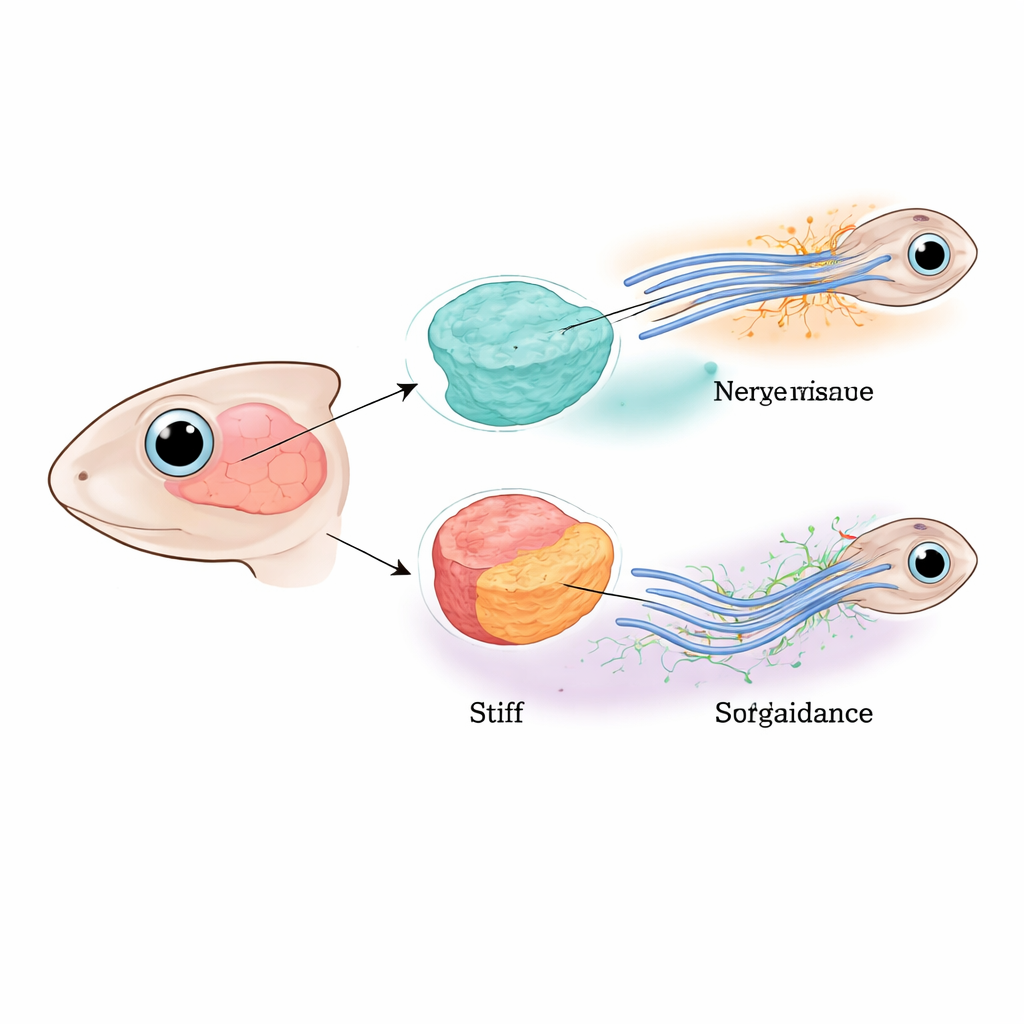
Prowadzenie nerwów przez młody mózg
Badacze skupili się na drodze wzrokowej młodych afrykańskich żab ościstych (Xenopus), gdzie włókna nerwowe z oka muszą przekroczyć mózg i wykonać precyzyjny skręt, zanim dotrą do obszaru docelowego. Wcześniejsze prace wykazały, że te włókna kierowane są zarówno przez dyfundujące chemiczne odpychacze, jak i przez stopniową zmianę sztywności tkanki wzdłuż ich trasy. W tej pracy zespół rozdzielił role samych neuronów i otaczającej tkanki mózgowej, selektywnie zmniejszając poziom kluczowego „czujnika siły” — białka Piezo1 — albo w samych włóknach nerwowych, albo w sąsiednich komórkach mózgu, albo w obu miejscach. Gdy Piezo1 był nieobecny wszędzie, wiele włókien zatrzymywało się, rozdwajało lub zbaczało z kursu, co potwierdziło, że właściwe wyczuwanie mechaniczne jest niezbędne do okablowania mózgu.
Gdy mózg zmiękcza się, sygnały dalekiego zasięgu gasną
Następnie autorzy zapytali, jak otaczająca tkanka mózgowa przyczynia się do tego systemu prowadzenia. Gdy usunęli Piezo1 tylko z włókien nerwowych, sztywność tkanki pozostała normalna, lecz nadal pojawiały się błędy w wytyczaniu dróg, co wskazuje, że włókna nie potrafiły już prawidłowo wyczuwać swojego mechanicznego otoczenia. Co zaskakujące, gdy Piezo1 usunięto z tkanki mózgowej, sama tkanka stała się prawie dwukrotnie miększa, a błędy w prowadzeniu pojawiały się jeszcze częściej — mimo że włókna nerwowe nadal zawierały Piezo1. W tych zmiękczonych regionach poziomy dwóch znanych długodystansowych cząsteczek prowadzących, Slit1 i Semaphorin3A, gwałtownie spadły zarówno na poziomie RNA, jak i białka. To pokazało, że stan fizyczny mózgu nie był tylko biernie odbierany przez komórki; aktywnie kontrolował, ile tych dyfundujących chemicznych sygnałów jest produkowanych.
Przyleganie komórek jako ukryta dźwignia mechaniczna
Co powoduje, że tkanka mózgowa pozbawiona Piezo1 jest miększa? Zespół wykluczył proste wyjaśnienia, takie jak mniejsza liczba komórek czy bardziej wiotkie komórki pojedyncze. Zamiast tego odkryli, że główne białka sklejające sąsiednie komórki mózgu — NCAM1 i N-kadheryna — były zmniejszone, gdy poziomy Piezo1 spadały. Gdy badacze bezpośrednio obniżyli te białka adhezyjne, sztywność tkanki spadła, a poziomy Semaphorin3A również się zmniejszyły, mimo że wnętrza komórek pozostały mechanicznie niezmienione. Wskazuje to na łańcuch zdarzeń, w którym aktywność Piezo1 pomaga utrzymać silne połączenia międzykomórkowe, które z kolei ustawiają masową sztywność tkanki, a ta następnie reguluje, ile określonych długodystansowych sygnałów chemicznych tkanka produkuje.
Podkręcanie mechanicznego pokrętła
Aby przetestować odwrotną stronę tej relacji, autorzy zwiększyli sztywność mózgu na kilka sposobów. W naczyniach hodowlanych zatopili małe fragmenty miękkiej tkanki mózgowej w trójwymiarowych żelach o różnej sztywności. Na twardszych żelach tkanka mocniej ciągnęła za otoczenie i zaczęła produkować znacznie wyższe poziomy Slit1 i Semaphorin3A, nawet w regionach, które normalnie tych sygnałów nie wytwarzają. U nieuszkodzonych kijanek zastosowali albo lek zwiększający wewnętrzne siły kurczliwe, albo delikatnie skompresowali określone obszary mózgu małą sondą. Oba podejścia usztywniły wybrane regiony i wywołały nową produkcję Semaphorin3A w obszarach zwykle chemicznie cichych. Jednak ten mechaniczny „przełącznik” zawiódł u zwierząt, w których Piezo1 został zredukowany, co pokazuje, że kanał ten jest potrzebny do przetłumaczenia zwiększonej sztywności na zwiększoną sygnalizację chemiczną.
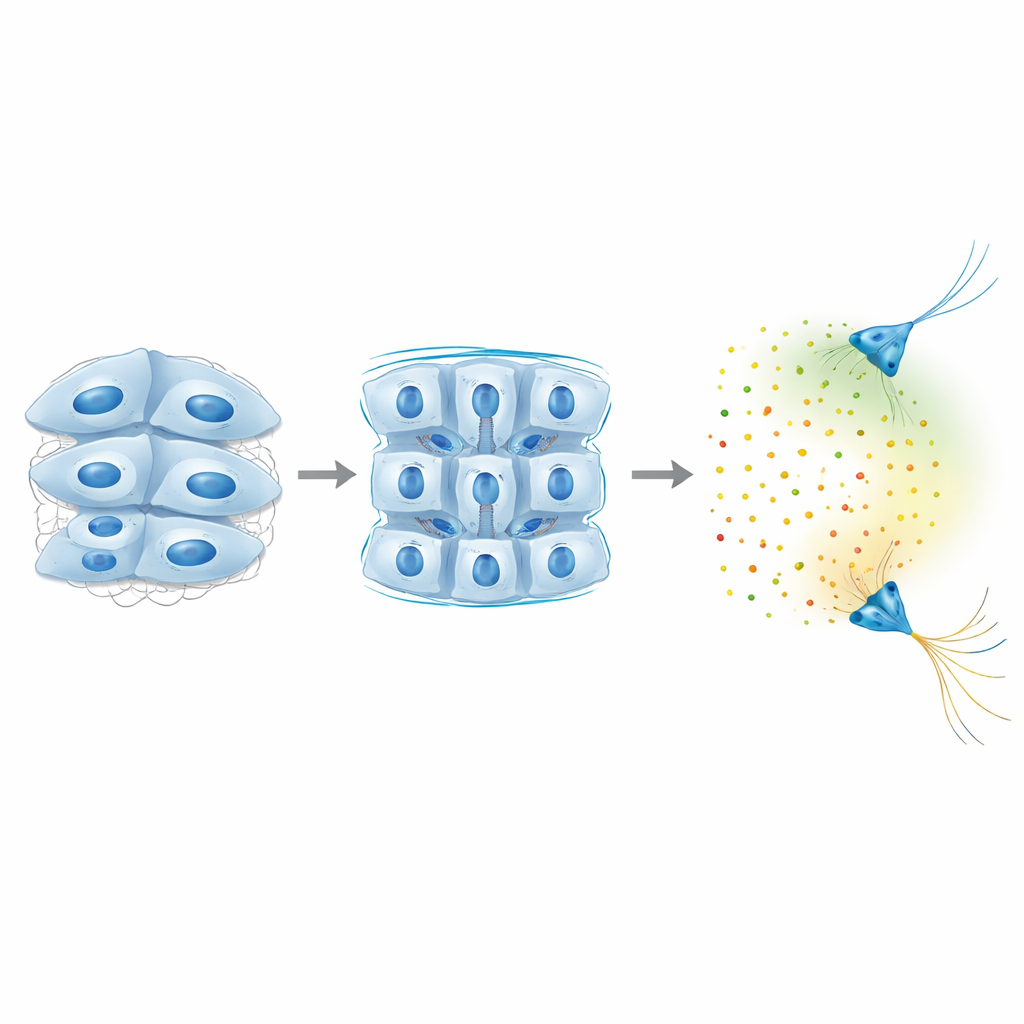
Dlaczego to ma znaczenie dla rozwijających się i chorych mózgów
Podsumowując, badanie ujawnia pętlę sprzężenia zwrotnego, w której komórki mózgowe napinają i odczuwają swoje otoczenie przez Piezo1, dostosowują swoje połączenia adhezyjne, aby ustawić sztywność tkanki, i dopiero po osiągnięciu progu sztywności włączają długodystansowe sygnały chemiczne, które kierują odległymi włóknami nerwowymi. Zamiast działać niezależnie, sygnały mechaniczne i chemiczne są ściśle splecione: lokalna zmiana jędrności tkanki może przekształcić „chemiczną pogodę” w odległych rejonach, wpływając na to, gdzie rosną aksony i jak formują się obwody. Ta obserwacja sugeruje, że zmieniona sztywność tkanki — występująca w warunkach od urazu mózgu po neurodegenerację — może rezonować w rozwijających się lub starzejących się mózgach, zmieniając same sygnały, których komórki używają do komunikacji na duże odległości.
Cytowanie: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Słowa kluczowe: mechanotransdukcja, nawigacja aksonalna, sztywność tkanki, Piezo1, rozwój mózgu