Clear Sky Science · de
Weitreichende chemische Signalübertragung in vivo wird durch mechanische Signale reguliert
Wie Berührung wachsende Gehirne formt
Während ein Gehirn Gestalt annimmt, müssen Milliarden junger Nervenzellen lange, verschlungene Wege zurücklegen, um ihre richtigen Partner zu finden. Seit Jahrzehnten ist bekannt, dass diese Reisen von chemischen Signalen geleitet werden, die wie unsichtbare Düfte durch das Gewebe diffundieren. Diese Studie zeigt einen überraschenden Partner dieser chemischen Hinweise: die physikalische Steifigkeit des Gehirns selbst. Durch sorgfältige Messungen an sich entwickelnden Froschhirnen zeigen die Autorinnen und Autoren, dass die Festigkeit oder Weichheit des Gewebes entfernte chemische Signale ein- oder ausschalten kann und so letztlich wachsende Nervenfasern auf die richtigen Bahnen lenkt.
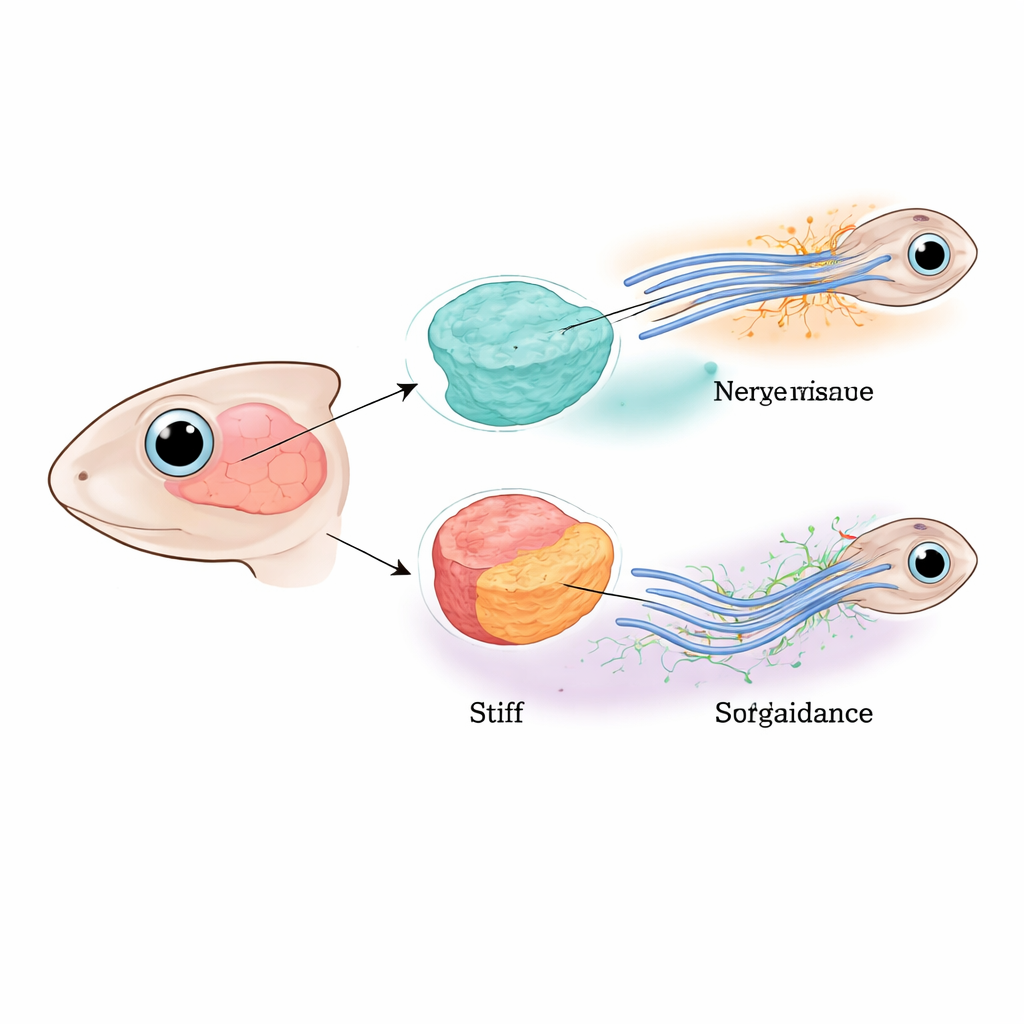
Nerven über das junge Gehirn leiten
Die Forschenden konzentrierten sich auf den optischen Leitungsweg junger Krallenfrösche (Xenopus), wo Nervenfasern aus dem Auge das Gehirn durchqueren und eine präzise Wendung ausführen müssen, bevor sie ihr Zielgebiet erreichen. Frühere Arbeiten zeigten, dass diese Fasern sowohl durch diffundierende chemische Replenten als auch durch einen allmählichen Wechsel der Gewebesteifigkeit entlang ihrer Route gesteuert werden. In der vorliegenden Arbeit trennten die Forschenden die Beiträge der Nervenfasern selbst und des umliegenden Hirngewebes, indem sie gezielt das wichtige „Kraftsensor“-Protein Piezo1 entweder in den Nervenfasern, in den benachbarten Hirnzellen oder in beiden reduzierten. Fehlt Piezo1 überall, stockten viele Fasern, spalteten sich oder drifteten vom Kurs ab, was bestätigt, dass korrektes mechanisches Erkennen für das Verdrahten des Gehirns essenziell ist.
Wenn das Gehirn weicher wird, schwinden Ferndsignale
Als Nächstes fragten die Autorinnen und Autoren, wie das umliegende Hirngewebe zu diesem Führungssystem beiträgt. Wurde Piezo1 nur aus den Nervenfasern entfernt, blieb die Gewebesteifigkeit normal, doch Pfadfindungsfehler traten weiterhin auf, was darauf hindeutet, dass die Fasern ihre mechanische Umgebung nicht mehr korrekt wahrnehmen konnten. Auffallend war, dass beim Entfernen von Piezo1 aus dem Hirngewebe das Gewebe nahezu doppelt so weich wurde und die Führungsfehler noch häufiger wurden — obwohl die Nervenfasern weiterhin Piezo1 enthielten. In diesen aufgeweichten Regionen sanken die Konzentrationen von zwei bekannten langreichweitigen Leitsubstanzen, Slit1 und Semaphorin3A, sowohl auf RNA- als auch auf Proteinebene deutlich. Das zeigt, dass der physikalische Zustand des Gehirns nicht nur passiv von Zellen wahrgenommen wird; er steuert aktiv, wie viel von diesen diffundierenden chemischen Signalen produziert wird.
Zelladhäsion als verborgener mechanischer Hebel
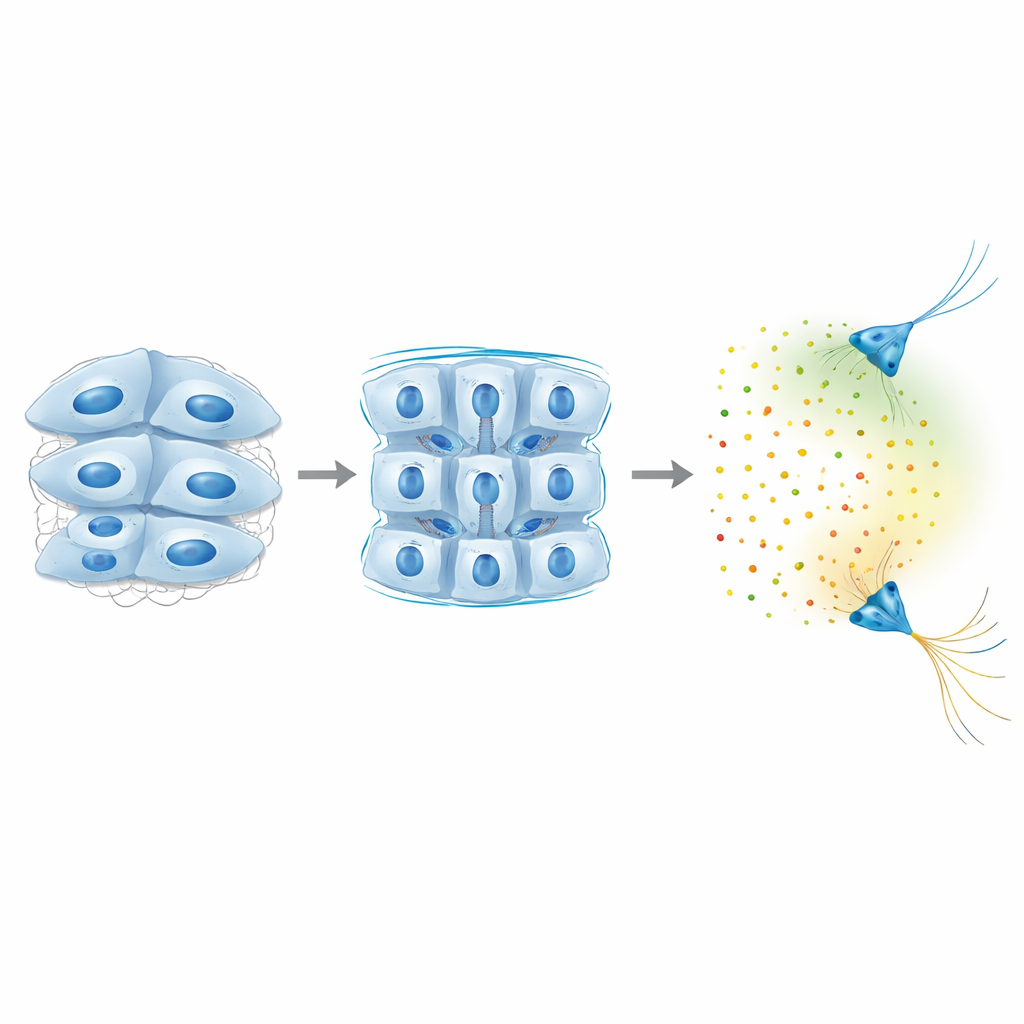
Wodurch wird Piezo1-defizientes Hirngewebe weicher? Das Team schloss einfache Erklärungen wie weniger Zellen oder weichere Einzelzellen aus. Stattdessen fanden sie, dass wichtige Proteine, die benachbarte Hirnzellen zusammenkleben — NCAM1 und N-Cadherin — reduziert waren, wenn Piezo1 abnahm. Wenn die Forschenden diese Adhäsionsproteine direkt verringerten, nahm die Gewebesteifigkeit ab und auch die Semaphorin3A-Werte fielen, obwohl das Innere der Zellen mechanisch unverändert blieb. Das deutet auf eine Ereigniskette hin, bei der Piezo1-Aktivität hilft, starke Zell–Zell-Verbindungen aufrechtzuerhalten, die wiederum die makroskopische Steifigkeit des Gewebes bestimmen und somit regeln, wie viel bestimmter langreichweitiger chemischer Signale das Gewebe produziert.
Den mechanischen Drehregler aufdrehen
Um die Gegenrichtung dieser Beziehung zu testen, erhöhten die Autorinnen und Autoren die Hirnsteifigkeit auf verschiedene Weise. In Zellkulturen betteten sie kleine Stücke weichen Hirngewebes in entweder weiche oder steife 3D-Gele ein. Auf steiferen Gelen zog das Gewebe kräftiger an seiner Umgebung und begann, deutlich höhere Mengen an Slit1 und Semaphorin3A zu produzieren, selbst in Regionen, die normalerweise diese Signale nicht herstellen. In intakten Kaulquappen verabreichten sie entweder ein Medikament, das die inneren kontraktilen Kräfte verstärkt, oder komprimierten bestimmte Hirnregionen sanft mit einer winzigen Sonde. Beide Ansätze verfestigten die ausgewählten Bereiche und lösten neue Semaphorin3A-Produktion in Gebieten aus, die üblicherweise chemisch ruhig sind. Dieses mechanische „Schaltverhalten“ versagte jedoch in Tieren, bei denen Piezo1 reduziert worden war, was zeigt, dass der Kanal nötig ist, um zusätzliche Steifigkeit in erhöhte chemische Signalgebung zu übersetzen.
Warum das für wachsende und erkrankte Gehirne wichtig ist
Insgesamt zeigt die Studie eine Rückkopplungsschleife, in der Gehirnzellen an ihrer Umgebung ziehen und diese über Piezo1 wahrnehmen, ihre adhäsiven Verbindungen anpassen, um die Gewebesteifigkeit festzulegen, und erst ab einer Schwellensteifigkeit langreichweitige chemische Hinweise einschalten, die entfernte Nervenfasern lenken. Mechanische und chemische Signale wirken demnach nicht unabhängig voneinander, sondern sind eng verflochten: Eine lokale Veränderung der Gewebefestigkeit kann das „chemische Wetter“ weit entfernt umgestalten, beeinflussen, wohin Axone wachsen und wie Schaltkreise sich formen. Diese Erkenntnis legt nahe, dass veränderte Gewebesteifigkeit — wie sie bei Verletzungen oder neurodegenerativen Erkrankungen auftritt — sich durch entwickelnde oder alternde Gehirne auswirken könnte, indem sie die Signale verändert, mit denen Zellen über große Entfernungen kommunizieren.
Zitation: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Schlüsselwörter: Mechanotransduktion, Axonführung, Gewebesteifigkeit, Piezo1, Gehirnentwicklung