Clear Sky Science · nl
Langafstands chemische signalering in vivo wordt gereguleerd door mechanische signalen
Hoe aanraking zich vormt in groeiende hersenen
Terwijl een brein vorm krijgt, moeten miljarden jonge zenuwcellen lange, kronkelige paden afleggen om hun juiste partners te vinden. Decennialang wisten wetenschappers dat deze reizen worden gestuurd door chemische signalen die zich als onzichtbare geuren door het weefsel verspreiden. Deze studie onthult een verrassende partner van die chemische aanwijzingen: de fysieke stijfheid van het brein zelf. Door ontwikkelende kikkervisjeshersenen nauwkeurig te onderzoeken, tonen de auteurs aan dat de mate van stevigheid of zachtheid van het weefsel verre chemische signalen aan of uit kan schakelen, en zo groeiende zenuwvezels uiteindelijk langs de juiste routes stuurt.
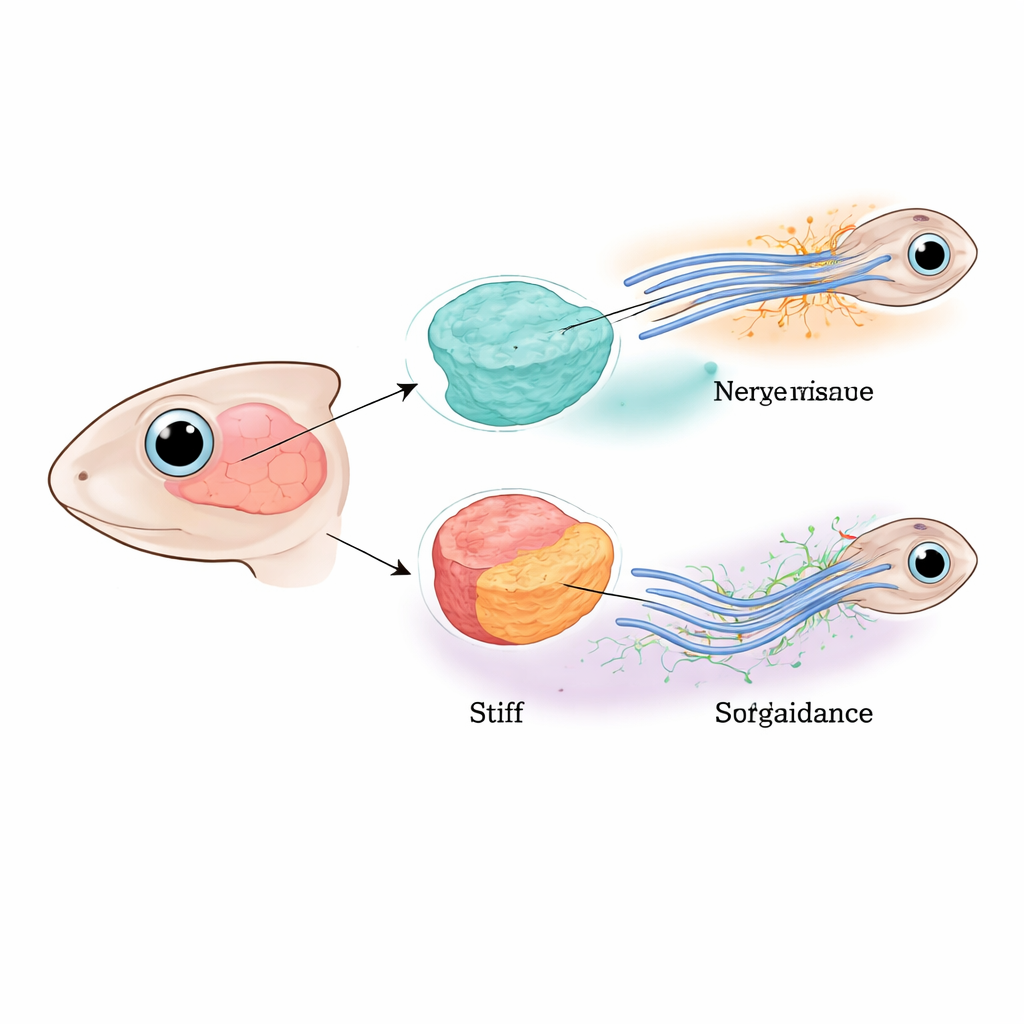
Geleiding van zenuwen door het jonge brein
De onderzoekers concentreerden zich op het optische pad van jonge Afrikaanse klauwkikkers, waar zenuwvezels vanuit het oog het brein moeten kruisen en een precieze bocht moeten maken voordat ze hun doelgebied bereiken. Eerder werk toonde aan dat deze vezels zowel door diffunderende chemische repellents als door een geleidelijke verandering in weefselstijfheid langs hun route gestuurd worden. Hier maakten de onderzoekers de rollen van de zenuwcellen zelf en het omringende breinweefsel uiteen door selectief een belangrijk "krachtsensor"-eiwit genaamd Piezo1 te verminderen in ofwel de zenuwvezels, de aangrenzende hersencellen, of beide. Wanneer Piezo1 overal ontbrak, bleven veel vezels steken, splitsten ze zich op of sloegen ze een verkeerde weg in, wat bevestigde dat juiste mechanische waarneming essentieel is voor het bedraden van het brein.
Wanneer het brein verzacht, vervagen langafstandssignalen
Vervolgens vroegen de auteurs hoe het omringende hersenweefsel bijdraagt aan dit geleidingssysteem. Wanneer zij Piezo1 alleen uit de zenuwvezels verwijderden, bleef de stijfheid van het weefsel normaal, maar traden er toch fouten in de padvinding op, wat aangeeft dat de vezels hun mechanische omgeving niet goed meer konden voelen. Opmerkelijk was dat wanneer Piezo1 in plaats daarvan uit het hersenweefsel werd verwijderd, het weefsel bijna twee keer zo zacht werd en geleidingsfouten nog frequenter voorkwamen — zelfs hoewel de zenuwvezels nog steeds Piezo1 bevatten. In deze verzachte regio’s daalden de niveaus van twee bekende langafstandsgleidingsmoleculen, Slit1 en Semaphorin3A, scherp zowel op RNA- als eiwitniveau. Dit toonde aan dat de fysieke staat van het brein niet alleen passief door cellen werd waargenomen; zij reguleerde actief hoeveel van deze diffunderende chemische signalen werden geproduceerd.
Celadhesie als een verborgen mechanische hefboom
Wat maakt Piezo1-deficiënt hersenweefsel zachter? Het team sloot eenvoudige verklaringen uit, zoals minder cellen of lossere individuele cellen. In plaats daarvan ontdekten ze dat belangrijke eiwitten die naburige hersencellen aan elkaar lijmen — NCAM1 en N-cadherine — werden verminderd wanneer Piezo1-niveaus daalden. Toen de onderzoekers deze adhesie-eiwitten direct verlaagden, daalde de weefselstijfheid en nam ook het niveau van Semaphorin3A af, hoewel de cellulaire inwendige mechanica ongewijzigd bleef. Dit wijst op een keten van gebeurtenissen waarbij Piezo1-activiteit helpt sterke cel–celverbindingen te behouden, die op hun beurt de bulkstijfheid van het weefsel bepalen, wat vervolgens regelt hoeveel van bepaalde langafstandige chemische signalen het weefsel produceert.
De mechanische draaiknop hoger zetten
Om het omgekeerde van deze relatie te testen, verhoogden de auteurs de hersenstijfheid op verschillende manieren. In petrischalen plaatsten ze kleine stukjes zacht hersenweefsel in 3D-gels die ofwel zacht ofwel stijf waren. In stijvere gels trok het weefsel harder aan zijn omgeving en begon het veel hogere niveaus van Slit1 en Semaphorin3A te produceren, zelfs in gebieden die normaal deze signalen niet maken. In intacte kikkervisjes gaven ze ofwel een geneesmiddel dat interne contractiele krachten versterkt, of ze comprimeerden voorzichtig specifieke hersengebieden met een klein probe. Beide benaderingen maakten de gekozen regio’s stijver en induceerden nieuwe productie van Semaphorin3A in gebieden die doorgaans chemisch stil zijn. Deze mechanische "schakelaar" faalde echter in dieren waarin Piezo1 was verminderd, wat aantoont dat het kanaal nodig is om extra stijfheid om te zetten in verhoogde chemische signalering.
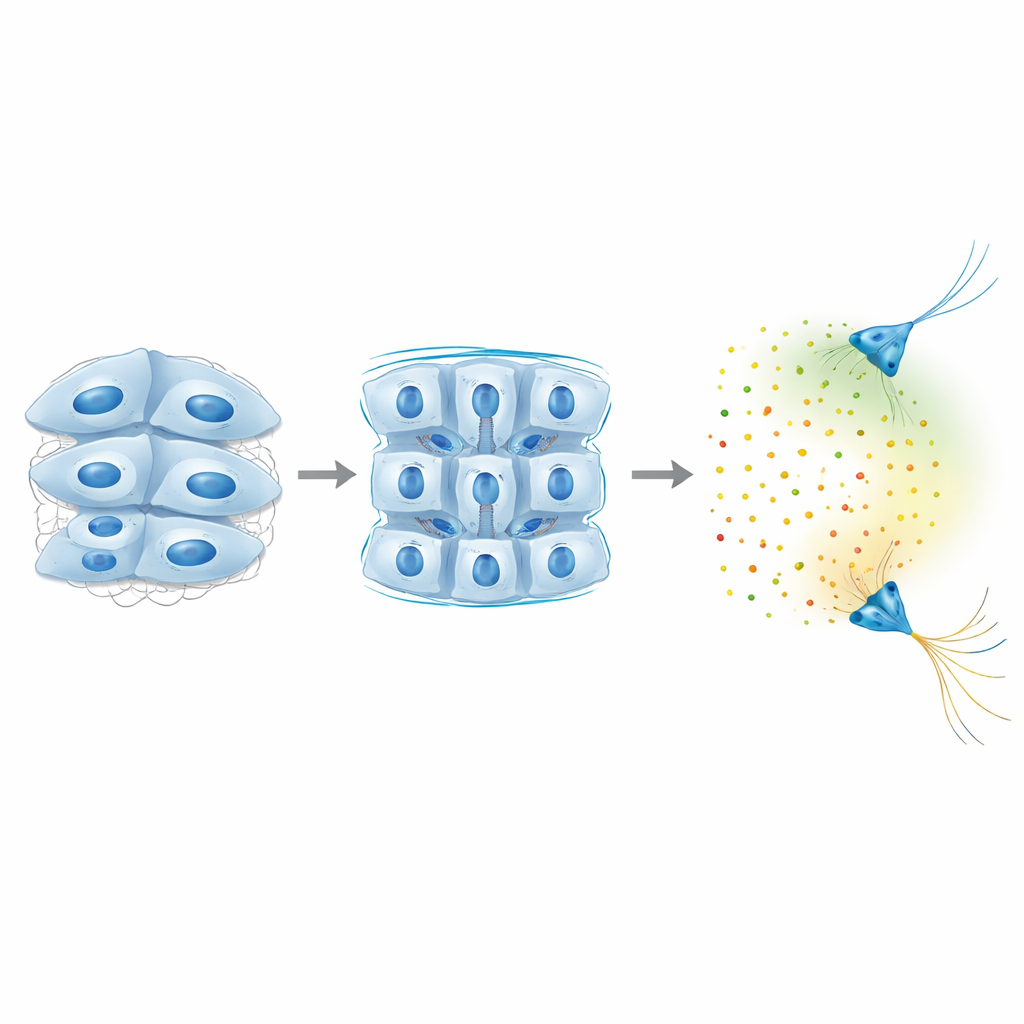
Waarom dit belangrijk is voor groeiende en zieke hersenen
Alles bij elkaar onthult de studie een terugkoppelingslus waarin hersencellen aan hun omgeving trekken en deze via Piezo1 waarnemen, hun adhesieve verbindingen aanpassen om te bepalen hoe stijf het weefsel is, en pas wanneer een drempelstijfheid is bereikt, langafstandige chemische aanwijzingen inschakelen die verre zenuwvezels sturen. In plaats van onafhankelijk te werken, zijn mechanische en chemische signalen nauw met elkaar verweven: een lokale verandering in de stevigheid van het weefsel kan het "chemische weer" op afstand hervormen, waardoor wordt beïnvloed waar axonen groeien en hoe netwerken zich vormen. Dit inzicht suggereert dat veranderde weefselstijfheid — waargenomen bij aandoeningen van hersenletsel tot neurodegeneratie — een echo kan veroorzaken door ontwikkelende of verouderende hersenen door de signalen die cellen gebruiken om over lange afstanden te communiceren te veranderen.
Bronvermelding: Pillai, E.K., Mukherjee, S., Gampl, N. et al. Long-range chemical signalling in vivo is regulated by mechanical signals. Nat. Mater. 25, 687–697 (2026). https://doi.org/10.1038/s41563-025-02463-9
Trefwoorden: mechanotransductie, axongeleiding, weefselstijfheid, Piezo1, hersenenontwikkeling