Clear Sky Science · ru
Функциональные подписи де-ново вариантов GABBR1 и GABBR2, ассоциированных с нейроразвивающими расстройствами
Почему крошечные изменения в химии мозга имеют значение
Многие дети с аутизмом, трудностями в обучении или нарушениями движений и внимания так и не получают ясного биологического объяснения своих симптомов. В этом исследовании рассматривается одна возможная причина: редкие генетические изменения, которые тонко искажают то, как клетки мозга реагируют на успокаивающее химическое вещество ГАМК. Проследив эти изменения от ДНК до отдельных рецепторов на нейронах, исследователи показывают, как маленькие молекулярные сбои могут нарушить баланс мозговой активности и указать путь к более точным, персонализированным методам лечения.
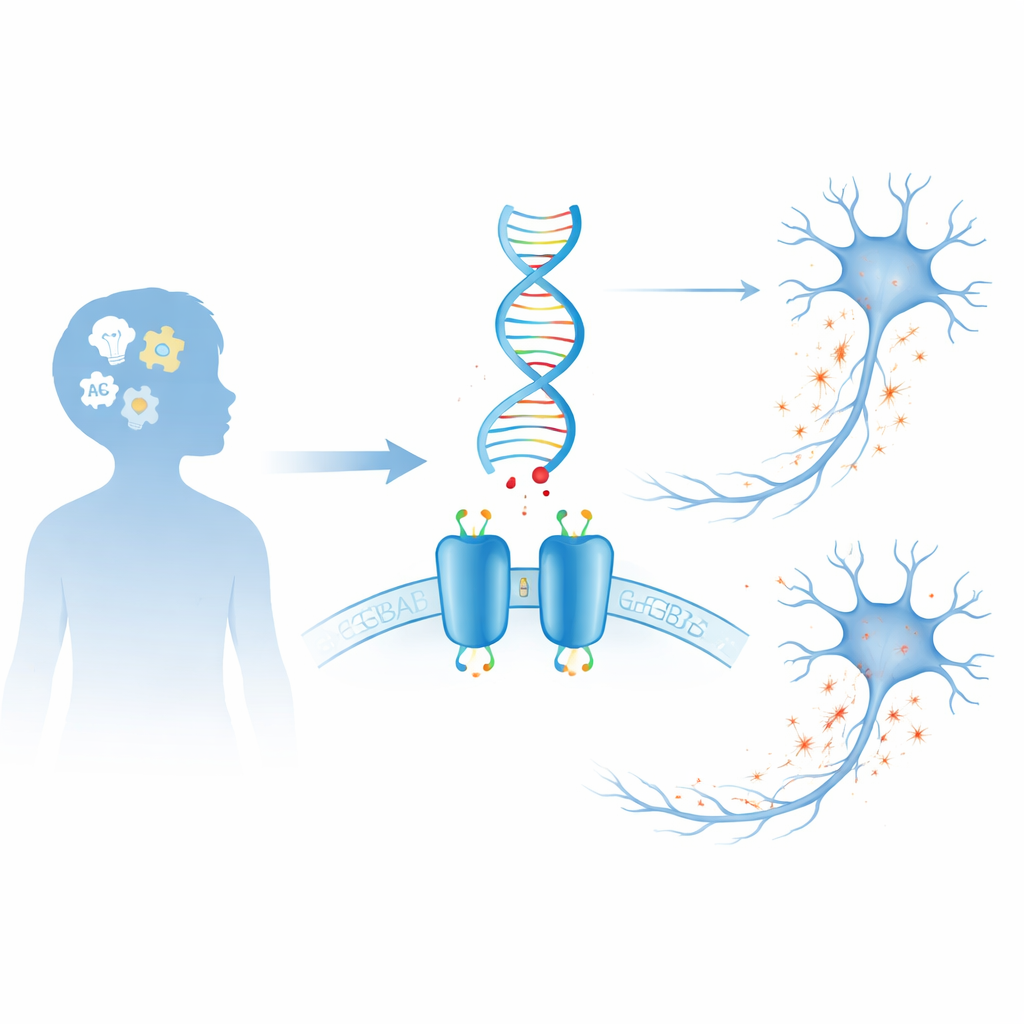
Тормозная система мозга
Наш мозг полагается на постоянную борьбу между сигналами, возбуждающими нейроны, и сигналами, которые их успокаивают. ГАМК — главное «тормозное» химическое вещество мозга. Один из ключевых инструментов, с помощью которого он действует, — GABAB-рецептор, состоящий из двух частей белок, расположенный на поверхности нейронов и некоторых клеток поддержки. Когда ГАМК связывается с рецептором, запускаются внутриклеточные изменения, снижающие активность клетки, что помогает предотвращать перегрузку, формировать ритмы мозга и тонко настраивать коммуникацию между клетками. Поскольку этот рецептор играет центральную роль в контроле возбудимости, даже незначительные изменения в его структуре могут иметь широкомасштабные эффекты на функцию мозга и поведение.
Семь редких генетических изменений под микроскопом
Исследователи сосредоточились на семи редких, спонтанных изменениях в ДНК — так называемых де-ново вариантах — в генах, кодирующих две половины GABAB-рецептора, GABBR1 и GABBR2. Каждый вариант был обнаружен у ребёнка с нейроразвивающими проблемами, такими как задержка речи и моторного развития, интеллектуальная недостаточность, черты аутистического спектра или трудности с вниманием; у некоторых также наблюдались судороги или нарушения движений. Компьютерные алгоритмы указывали на то, что эти варианты, вероятно, вредны, но такие предсказания не могут сказать, станет ли рецептор сверхактивным, недостаточно активным или неправильно локализованным. Чтобы ответить на эти вопросы, команда воспроизвела каждый вариант в человеческих клетках в лаборатории и измерила, как ведут себя изменённые рецепторы.
Когда тормоз мозга заедает или проскальзывает
Эксперименты показали, что семь вариантов проявляли себя по-разному. Некоторые ослабляли реакцию рецептора на ГАМК: для полного включения рецептора требовалось гораздо больше вещества, или меньшее число рецепторов достигало поверхности клетки. Эти изменения фактически снижали доступную тормозную силу в мозге. Другие варианты имели почти противоположный эффект, оставляя рецептор частично включённым даже при отсутствии ГАМК. Такая постоянная низкоуровневая активность повышала базовый уровень сигнализации, но парадоксально уменьшала запас для дальнейшей реакции при росте уровня ГАМК, притупляя влияние реальных ингибирующих сигналов в периоды интенсивной мозговой активности.
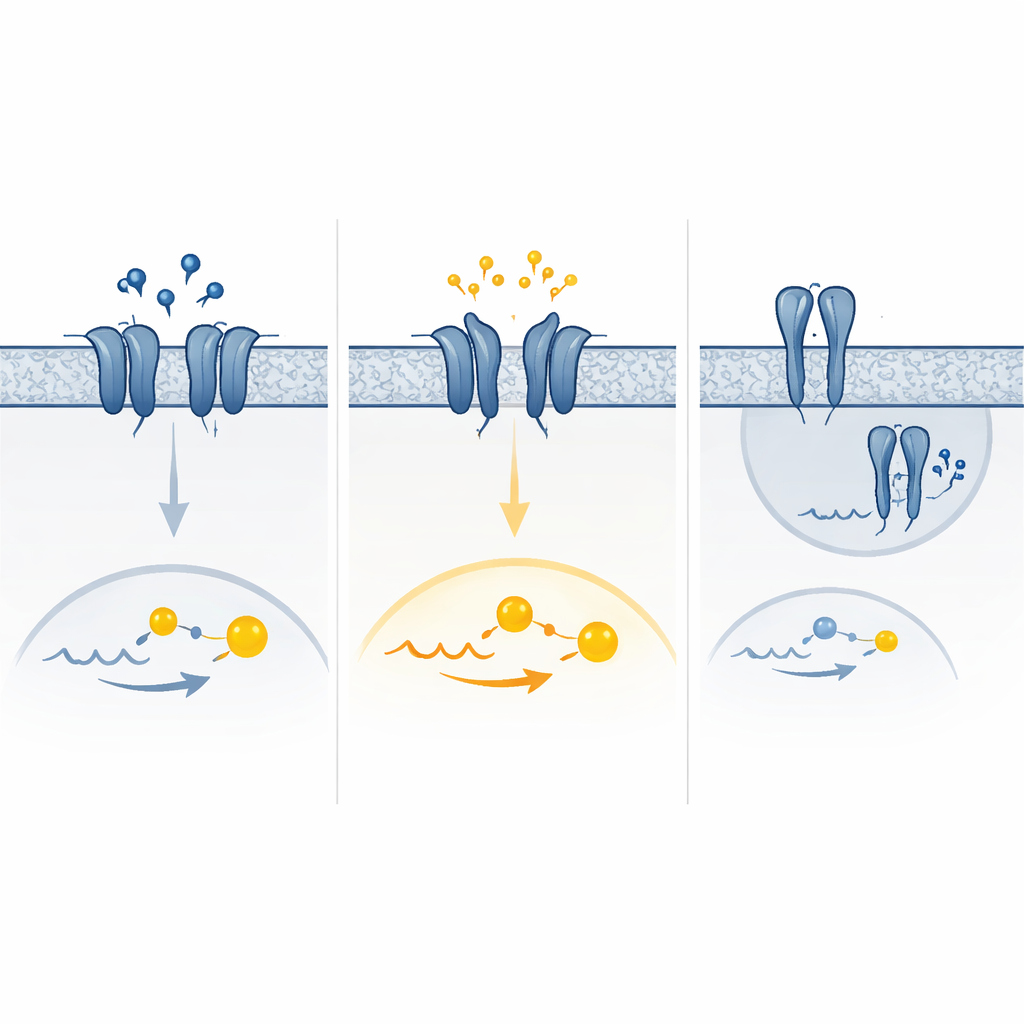
Смешение избыточного и недостаточного сигнала
Компьютерные моделирования движений рецептора помогли объяснить один яркий вариант, который демонстрировал сильную базовую активность и почти полное отсутствие реакции на ГАМК. В этом случае часть внешнего «зажима» рецептора имела тенденцию сама по себе закрываться и оставаться в активоподобной форме, имитируя то, что обычно происходит только при связывании ГАМК. Другие варианты, по-видимому, смещали равновесие в сторону активных конфигураций мембраносвязующих сегментов рецептора или изменяли то, как пары рецепторов собираются и достигают поверхности клетки. В результате возник спектр эффектов — чистая потеря функции, чистый прирост функции или комбинация обоих, в зависимости от уровня ГАМК и того, как клетки со временем адаптируются, удаляя или понижая активность чрезмерно активных рецепторов.
Последствия для персонализированного лечения
Хотя у детей были схожие симптомы, лежащие в основе проблемы с рецепторами оказались существенно разными. Это важно для терапии. Варианты, уменьшающие число рецепторов или их чувствительность, могут реагировать на препараты, усиливающие эффект ГАМК на оставшиеся нормальные рецепторы. Напротив, варианты, делающие рецепторы слишком активными, могут требовать иного подхода, и простая блокада рецептора может усугубить некоторые аспекты сигнализации. Исследование показывает, что полагаться только на компьютерные предсказания недостаточно: прямые функциональные тесты необходимы, чтобы различать эти сценарии. Точное картирование того, как каждый вариант GABAB-рецептора меняет сигнализацию, закладывает основу для более таргетированных стратегий лечения нейроразвивающих расстройств, в которых тормозная система мозга работает неверно.
Цитирование: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Ключевые слова: GABAB-рецептор, нейроразвивающие расстройства, генетические варианты, расстройства аутистического спектра, персонализированная медицина