Clear Sky Science · it
Firme funzionali di varianti de novo di GABBR1 e GABBR2 associate a disturbi del neurosviluppo
Perché piccole modifiche nella chimica cerebrale contano
Molti bambini con autismo, difficoltà di apprendimento o problemi di movimento e attenzione non ricevono mai una spiegazione biologica chiara per i loro sintomi. Questo studio esamina una possibile causa: cambiamenti genetici rari che alterano in modo sottile il modo in cui le cellule cerebrali rispondono a una sostanza chimica calmante chiamata GABA. Seguendo queste varianti dal DNA ai singoli recettori sui neuroni, i ricercatori mostrano come piccoli difetti molecolari possano spostare l’equilibrio dell’attività cerebrale e indicare la strada verso trattamenti più precisi e personalizzati.
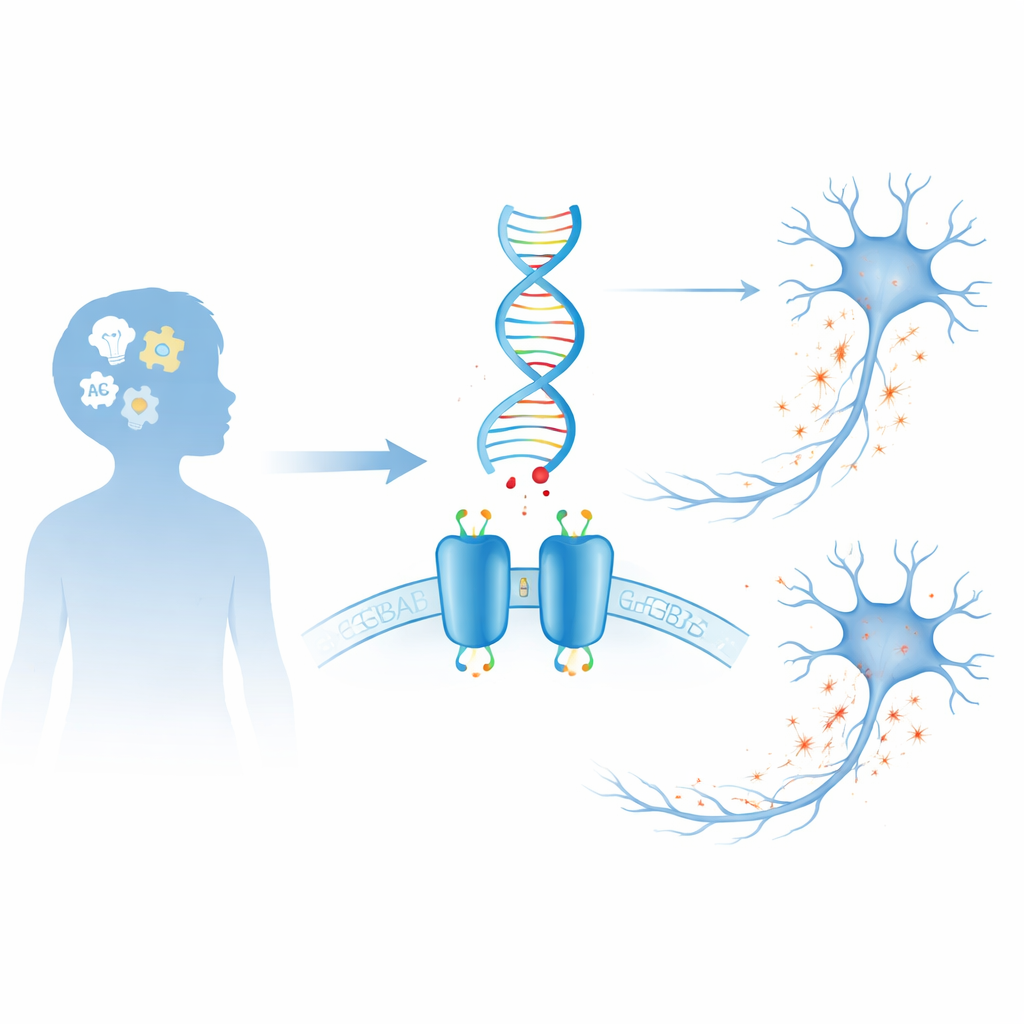
Il sistema frenante del cervello
I nostri cervelli si basano su una continua lotta tra segnali che eccitano i neuroni e segnali che li calmano. Il GABA è la principale sostanza «freno» del cervello. Uno dei dispositivi chiave che impiega è il recettore GABAB, una proteina in due parti che si trova sulla superficie dei neuroni e di alcune cellule di supporto. Quando il GABA si lega, il recettore innesca cambiamenti interni che abbassano l’attività cellulare, contribuendo a prevenire il sovraccarico, definire i ritmi cerebrali e affinare la comunicazione tra le cellule. Poiché questo recettore è così centrale nel controllo dell’eccitabilità, anche lievi variazioni nella sua struttura possono avere effetti estesi sulla funzione cerebrale e sul comportamento.
Sette varianti genetiche rare sotto la lente
I ricercatori si sono concentrati su sette cambiamenti del DNA rari e spontanei — chiamati varianti de novo — nei geni che codificano le due parti del recettore GABAB, GABBR1 e GABBR2. Ciascuna variante è stata trovata in un bambino con problemi del neurosviluppo come ritardo nel linguaggio e nelle abilità motorie, disabilità intellettiva, tratti dello spettro autistico o difficoltà di attenzione; alcuni avevano anche crisi epilettiche o anomalie del movimento. Gli algoritmi informatici suggerivano tutti che queste varianti erano probabilmente dannose, ma tali predizioni non possono dire se un recettore diventi iperattivo, ipoattivo o mal posizionato. Per rispondere a questa domanda, il gruppo ha ricreato ciascuna variante in cellule umane in laboratorio e ha misurato il comportamento dei recettori alterati.
Quando il freno del cervello si blocca o scivola
Gli esperimenti hanno rivelato che le sette varianti non agivano tutte allo stesso modo. Alcune indebolivano la risposta del recettore al GABA: era necessaria una quantità molto maggiore del neurotrasmettitore per attivare completamente il recettore, oppure un numero inferiore di recettori raggiungeva la superficie cellulare. Questi cambiamenti riducevano di fatto la potenza frenante disponibile nel cervello. Altre varianti avevano quasi l’effetto opposto, lasciando il recettore parzialmente attivato anche in assenza di GABA. Questa attività costante a bassa intensità aumentava la segnalazione basale ma paradossalmente lasciava meno margine per una risposta ulteriore quando i livelli di GABA aumentavano, attenuando l’impatto dei veri segnali inibitori durante l’attività cerebrale intensa.
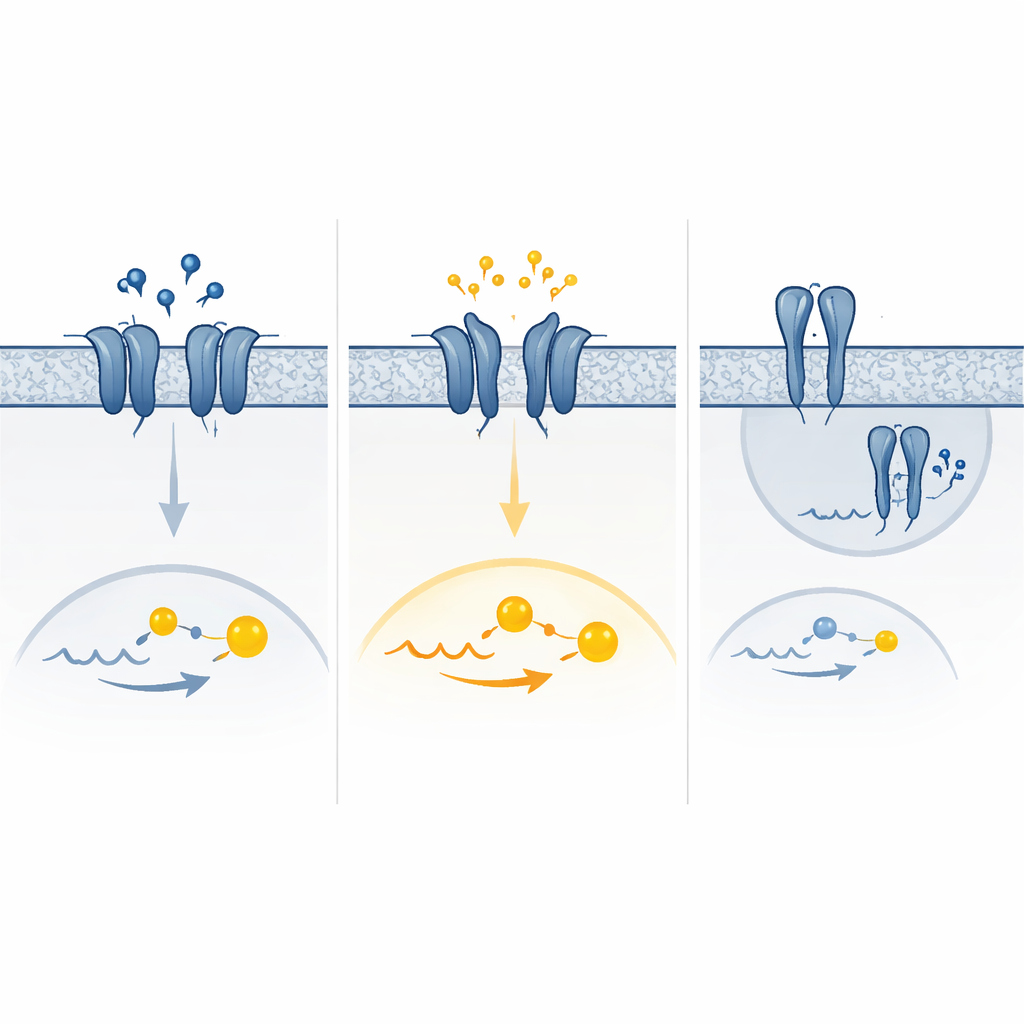
Un mix di segnale in eccesso e in difetto
Le simulazioni al computer del movimento dei recettori hanno aiutato a spiegare una variante sorprendente che mostrava forte attività basale e praticamente nessuna risposta al GABA. In questo caso, una parte del dominio esterno «morsetto» del recettore tendeva a chiudersi autonomamente e a rimanere in una conformazione simile a quella attiva, imitando quanto normalmente accade solo quando il GABA è legato. Altre varianti sembravano favorire disposizioni attive dei segmenti transmembrana del recettore o alterare il modo in cui le coppie di recettori si assemblano e raggiungono la superficie cellulare. Il risultato finale era uno spettro di effetti — perdita di funzione pura, aumento di funzione puro o una combinazione di entrambi a seconda dei livelli di GABA e di come le cellule si adattano nel tempo rimuovendo o regolando al ribasso i recettori iperattivi.
Implicazioni per trattamenti personalizzati
Nonostante i bambini condividessero sintomi sovrapposti, i problemi recettoriali sottostanti erano piuttosto diversi. Questa scoperta è importante per la terapia. Le varianti che riducono il numero o la sensibilità dei recettori potrebbero beneficiare di farmaci che potenziano l’effetto del GABA sui recettori normali rimasti. Al contrario, le varianti che rendono i recettori troppo attivi potrebbero rispondere in modo molto diverso, e il semplice blocco del recettore potrebbe peggiorare alcuni aspetti della segnalazione. Lo studio mostra che affidarsi solo alle predizioni informatiche non basta: i test funzionali diretti sono cruciali per distinguere questi scenari. Mappando esattamente come ciascuna variante del recettore GABAB modifica la segnalazione, questo lavoro pone le basi per strategie terapeutiche più mirate nei disturbi del neurosviluppo in cui il sistema frenante del cervello si altera.
Citazione: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Parole chiave: Recettore GABAB, disturbi del neurosviluppo, varianti genetiche, spettro autistico, medicina di precisione