Clear Sky Science · pt
Assinaturas funcionais de variantes de novo em GABBR1 e GABBR2 associadas a transtornos do neurodesenvolvimento
Por que pequenas mudanças na química cerebral são importantes
Muitas crianças com autismo, dificuldades de aprendizado ou problemas de movimento e atenção nunca recebem uma explicação biológica clara para seus sintomas. Este estudo investiga uma possível causa: alterações genéticas raras que distorcem sutilmente como as células cerebrais respondem a um químico calmante chamado GABA. Ao rastrear essas mudanças do DNA até receptores individuais nos neurônios, os pesquisadores mostram como pequenas falhas moleculares podem desequilibrar a atividade cerebral e indicar caminhos para tratamentos mais precisos e personalizados.
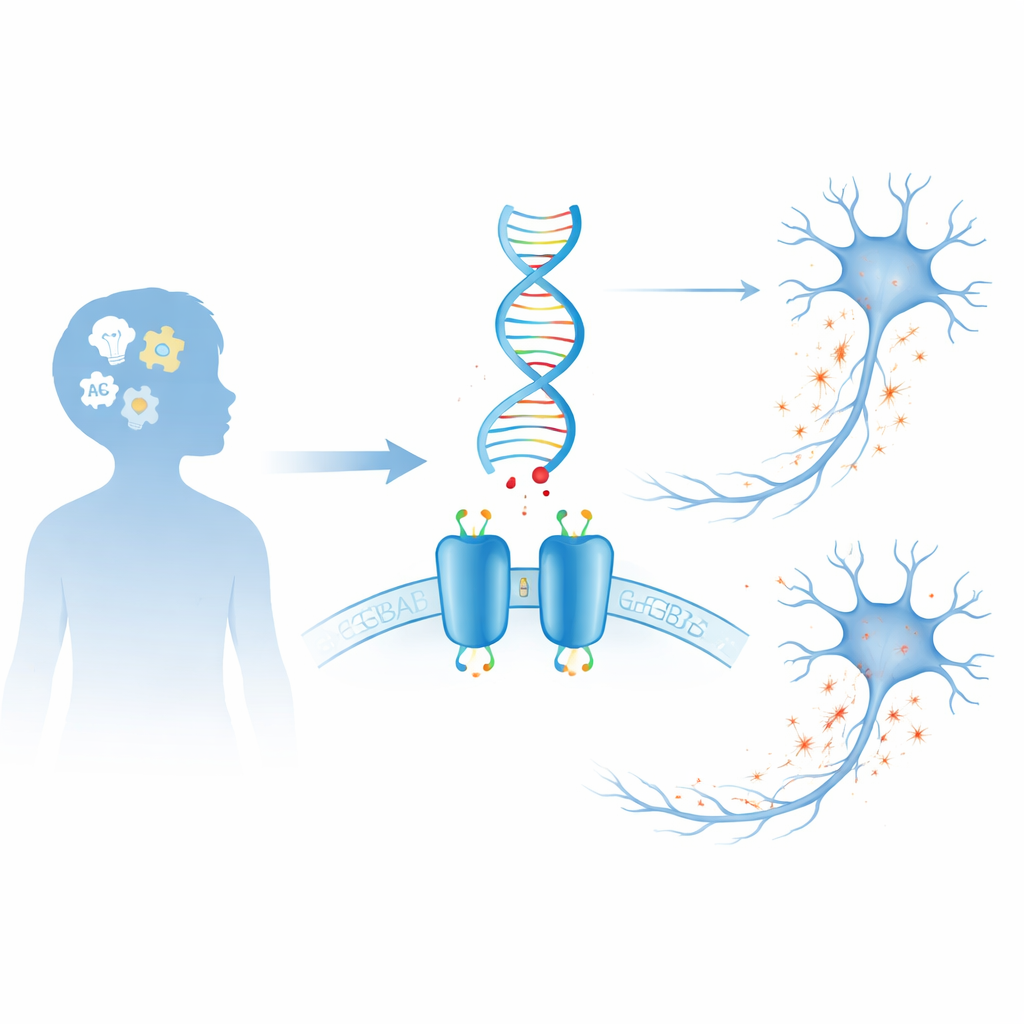
O sistema de freio do cérebro
Nossos cérebros dependem de um constante cabo-de-guerra entre sinais que excitam os neurônios e sinais que os acalmam. O GABA é o principal “freio” químico do cérebro. Um dos dispositivos-chave que ele usa é o receptor GABAB, uma proteína em duas partes que se localiza na superfície dos neurônios e de algumas células de suporte. Quando o GABA se liga, o receptor desencadeia mudanças internas que reduzem a atividade celular, ajudando a prevenir sobrecarga, a moldar ritmos cerebrais e a ajustar finamente a comunicação entre células. Como esse receptor é central no controle da excitabilidade, até mudanças leves em sua estrutura podem ter efeitos amplos sobre a função cerebral e o comportamento.
Sete alterações genéticas raras sob o microscópio
Os pesquisadores focaram em sete mudanças raras e espontâneas no DNA — chamadas variantes de novo — nos genes que codificam as duas metades do receptor GABAB, GABBR1 e GABBR2. Cada variante foi encontrada em uma criança com problemas do neurodesenvolvimento, como atraso da fala e das habilidades motoras, deficiência intelectual, características do espectro autista ou dificuldades de atenção; algumas também apresentavam convulsões ou anormalidades de movimento. Algoritmos computacionais sugeriram que essas variantes provavelmente eram prejudiciais, mas tais previsões não conseguem dizer se um receptor fica hiperativo, subativo ou mal localizado. Para responder a isso, a equipe recriou cada variante em células humanas no laboratório e mediu como os receptores alterados se comportavam.
Quando o freio do cérebro trava ou escorrega
Os experimentos revelaram que as sete variantes não atuavam da mesma forma. Algumas enfraqueceram a resposta do receptor ao GABA: era necessária muito mais substância para ativar totalmente o receptor, ou menos receptores chegavam à superfície celular. Essas mudanças reduziram efetivamente o poder de freio disponível no cérebro. Outras variantes tiveram quase o efeito oposto, deixando o receptor parcialmente ativado mesmo na ausência de GABA. Essa atividade constante em baixo nível aumentava a sinalização basal, mas paradoxalmente deixava menos espaço para resposta adicional quando os níveis de GABA aumentavam, atenuando o impacto dos sinais inibitórios reais durante períodos de intensa atividade cerebral.
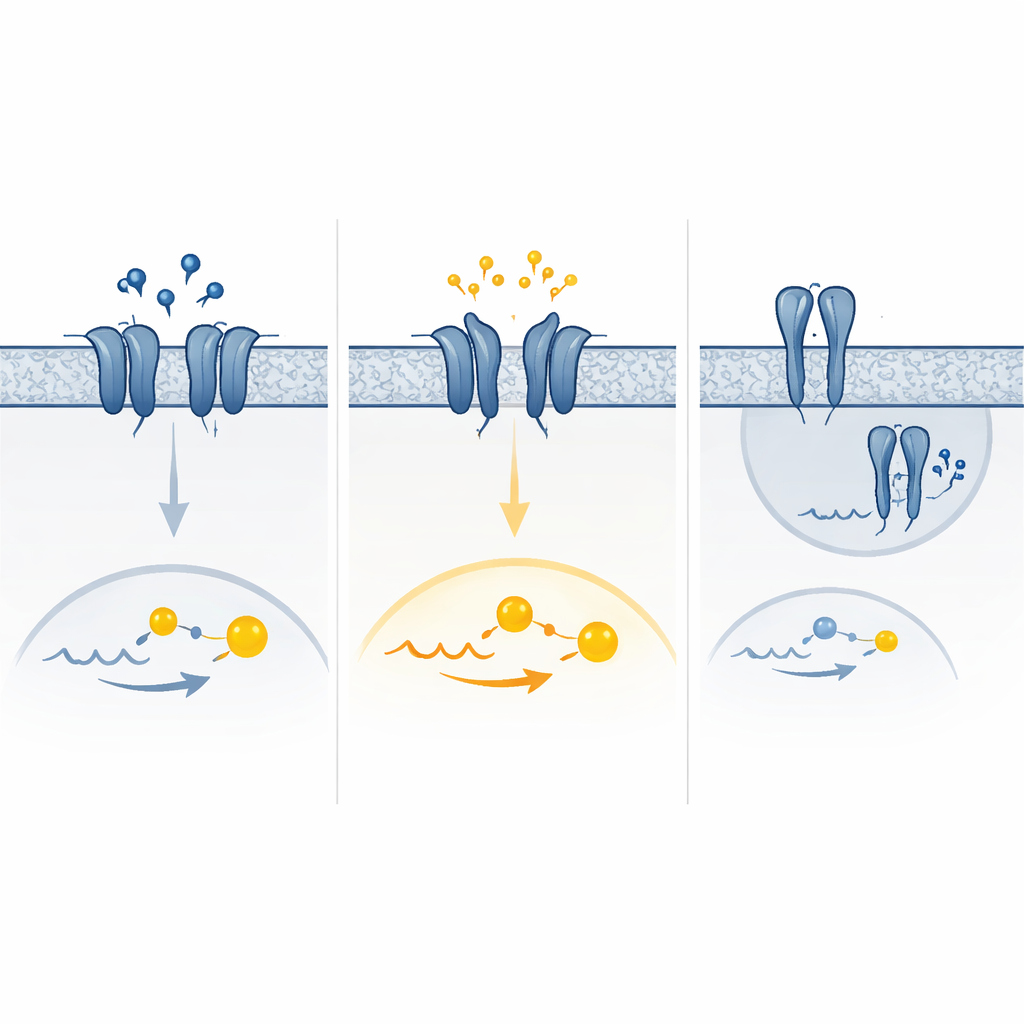
Uma mistura de sinal demais e de sinal de menos
Simulações computacionais do movimento do receptor ajudaram a explicar uma variante marcante que apresentava forte atividade basal e praticamente nenhuma resposta ao GABA. Nesse caso, parte do domínio externo em “braçadeira” do receptor tendia a se fechar sozinha e permanecer numa forma semelhante à ativa, imitando o que normalmente ocorre apenas quando o GABA está ligado. Outras variantes pareciam favorecer arranjos ativos dos segmentos transmembranares do receptor ou alteravam como os pares de receptores se montavam e alcançavam a superfície celular. O resultado final foi um espectro de efeitos — perda pura de função, ganho puro de função, ou uma combinação de ambos dependendo dos níveis de GABA e de como as células se adaptam ao longo do tempo removendo ou regulando para baixo receptores hiperativos.
Implicações para tratamentos personalizados
Embora as crianças compartilhassem sintomas sobrepostos, os problemas subjacentes nos receptores eram bastante diferentes. Essa constatação é relevante para a terapia. Variantes que reduzem o número ou a sensibilidade dos receptores podem ser beneficiadas por drogas que aumentem o efeito do GABA nos receptores normais restantes. Em contraste, variantes que tornam os receptores excessivamente ativos podem responder de forma muito diferente, e bloquear simplesmente o receptor pode piorar certos aspectos da sinalização. O estudo mostra que confiar apenas em previsões computacionais não é suficiente: testes funcionais diretos são cruciais para distinguir entre esses cenários. Ao mapear exatamente como cada variante do receptor GABAB altera a sinalização, este trabalho estabelece a base para estratégias de tratamento mais direcionadas em transtornos do neurodesenvolvimento nos quais o sistema de freio do cérebro funciona mal.
Citação: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Palavras-chave: receptor GABAB, transtornos do neurodesenvolvimento, variantes genéticas, transtorno do espectro autista, medicina de precisão