Clear Sky Science · ar
التواقيع الوظيفية لمتغيرات جديدة في GABBR1 و GABBR2 المرتبطة باضطرابات النمو العصبي
لماذا تهم التغيرات الصغيرة في كيمياء الدماغ
العديد من الأطفال الذين يعانون من توحد أو صعوبات تعلم أو مشاكل في الحركة والانتباه لا يحصلون أبدًا على تفسير بيولوجي واضح لأعراضهم. تبحث هذه الدراسة في سبب محتمل واحد: تغيّرات جينية نادرة تشوّه بشكل طفيف كيفية استجابة خلايا الدماغ لمادة مهدئة تُدعى GABA. من خلال تتبع هذه التغيّرات من الحمض النووي إلى مستقبلات مفردة على الخلايا العصبية، يظهر الباحثون كيف أن عيوبًا جزيئية صغيرة يمكن أن تُخل بتوازن نشاط الدماغ وتدل على سبل لعلاجات أكثر دقة وشخصانية.
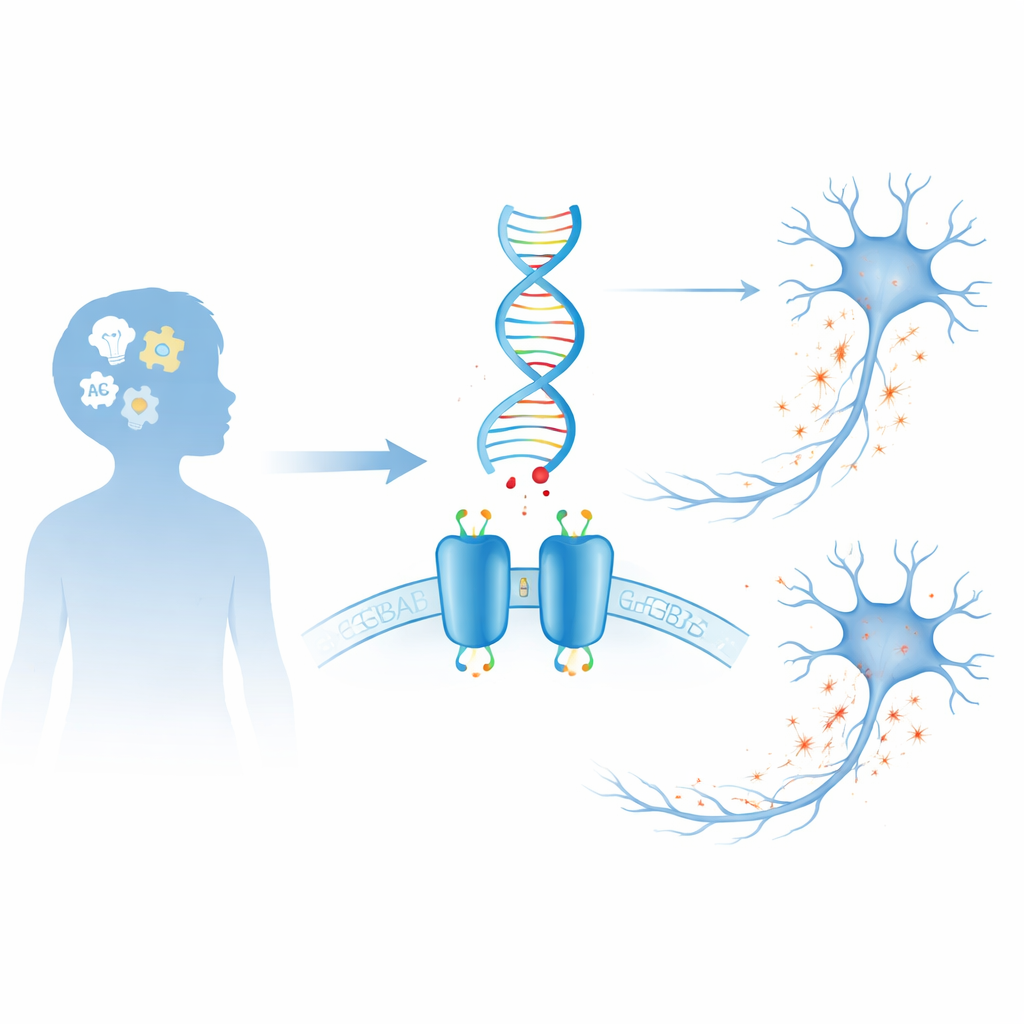
نظام الكبح في الدماغ
يعتمد دماغنا على صراع دائم بين الإشارات التي تُنشط الخلايا العصبية والإشارات التي تهدئها. GABA هو المركب «الفرامل» الرئيس في الدماغ. أحد الأجهزة الرئيسة التي يستخدمها هو مستقبل GABAB، وهو بروتين مكوّن من جزأين يجلس على سطح الخلايا العصبية وبعض الخلايا الداعمة. عند ارتباط GABA، يحفّز المستقبل تغيّرات داخلية تقلل من نشاط الخلايا، مما يساعد على منع التحميل الزائد، وتشكيل إيقاعات الدماغ، وضبط التواصل بين الخلايا بدقة. وبما أن هذا المستقبل محوري في التحكم في القابلية للتهيّج، فإن تغيّرًا طفيفًا في بنيته يمكن أن يكون له آثار واسعة على وظيفة الدماغ والسلوك.
سبعة تغيّرات جينية نادرة تحت المجهر
ركز الباحثون على سبعة تغيّرات نادرة وعفوية في الحمض النووي — تُسمى متغيرات نشأت حديثًا (de novo) — في الجينات التي تشفر نصفي مستقبل GABAB، وهما GABBR1 و GABBR2. وُجد كل متغير في طفل يعاني من مشاكل في التطور العصبي مثل تأخر النطق والمهارات الحركية، وتأخر ذهني، وسمات طيف التوحد، أو صعوبات في الانتباه؛ كما أن بعضهم عانى أيضًا نوبات أو اضطرابات حركية. أشارت خوارزميات الكمبيوتر جميعها إلى أن هذه المتغيرات من المرجح أن تكون ضارة، لكن هذه التنبؤات لا تكشف ما إذا كان المستقبل يصبح مفرط النشاط أو ناقص النشاط أو متغير الموضع داخل الخلية. للإجابة عن ذلك، أعاد الفريق إنشاء كل متغير في خلايا بشرية في المختبر وقيَّم كيف تصرفت المستقبلات المتغيّرة.
عندما تلتصق فرامل الدماغ أو تزلق
أظهرت التجارب أن السبعة متغيرات لم تتصرف جميعها بنفس الطريقة. فقد أضعف بعضها استجابة المستقبل لـ GABA: احتاجت كميات أكبر بكثير من المركب لتشغيل المستقبل بالكامل، أو أن عددًا أقل من المستقبلات وصل إلى سطح الخلية على الإطلاق. هذه التغيرات قللت فعليًا من قوة الكبح المتاحة في الدماغ. أما متغيرات أخرى فكان لها تقريبًا تأثير معاكس، إذ تركت المستقبل في حالة نشاط جزئي حتى عندما لم يكن هناك GABA حاضرًا. عزز هذا النشاط قاعدة الإشارة، لكن من المفارقات أنه ترك مجالًا أقل للاستجابة الإضافية عندما ارتفعت مستويات GABA، مما قلّل من تأثير الإشارات المثبطة الحقيقية أثناء نشاط الدماغ المكثف.
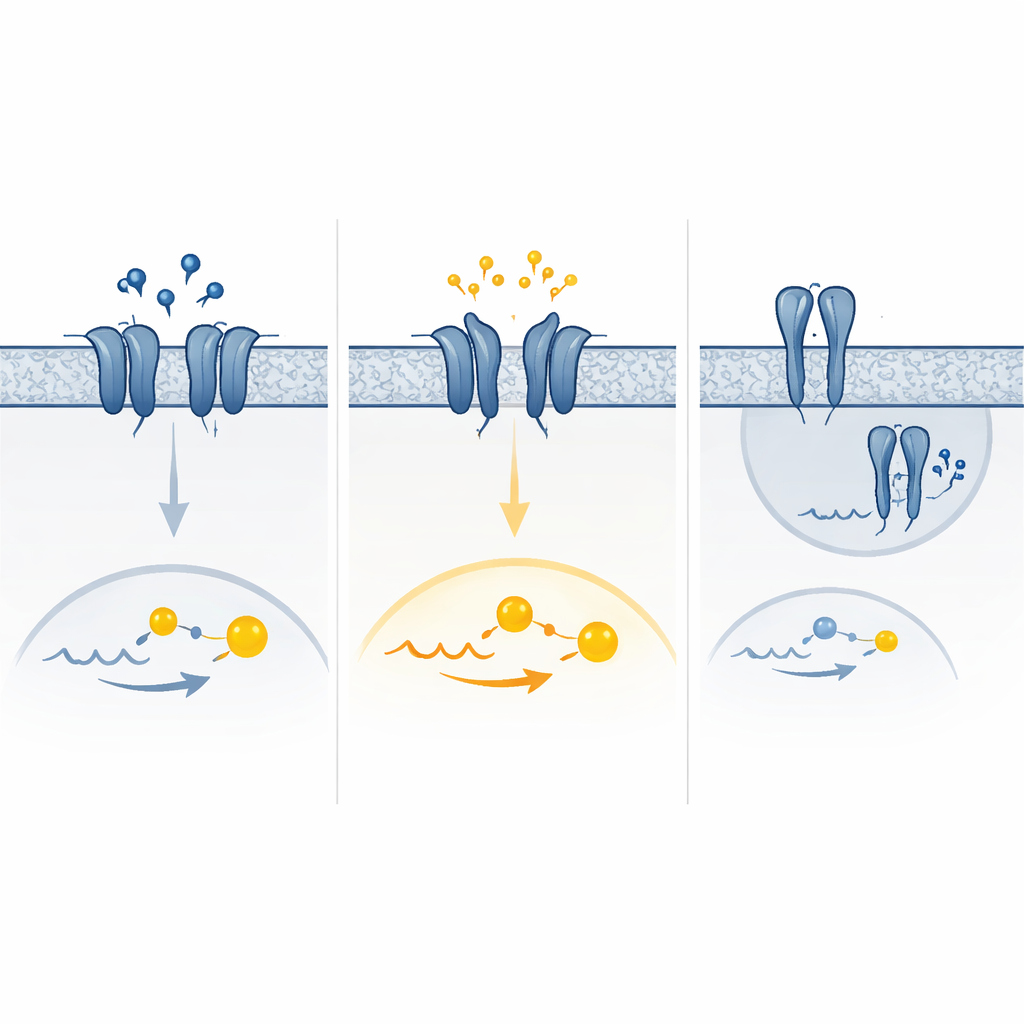
مزيج من فرط الإشارة ونقصها
ساعدت محاكيات حركة المستقبلات في الكمبيوتر على تفسير أحد المتغيرات اللافتة الذي أظهر نشاطًا قويًا على خط الأساس وتقريبًا عدم استجابة لـ GABA. في هذه الحالة، كان جزء من «مِلكَم» المستقبل الخارجي يميل إلى الانغلاق من تلقاء نفسه والبقاء في شكل شبيه بالنشط، مقلدًا ما يحدث عادةً فقط عند ارتباط GABA. بدا أن متغيرات أخرى تُفضّل ترتيبًا نشطًا لأجزاء المستقبل العابرة للغشاء أو تغيّر كيفية تجمّع أزواج المستقبلات ووصولها إلى سطح الخلية. والنتيجة النهائية كانت طيفًا من التأثيرات — فقدان كامل للوظيفة، أو كسب كامل للوظيفة، أو مزيج من الاثنين اعتمادًا على مستويات GABA وكيف تتكيف الخلايا مع مرور الوقت بإزالة أو خفض تنظيم المستقبلات المفرطة النشاط.
تداعيات للعلاج الشخصي
على الرغم من اشتراك الأطفال في أعراض متداخلة، كانت مشاكل المستقبلات الكامنة مختلفة إلى حد كبير. وهذه النتيجة مهمة للعلاج. قد تُستفاد المتغيرات التي تقلل عدد المستقبلات أو حساسيتها من أدوية تعزز تأثير GABA على المستقبلات السوية المتبقية. في المقابل، قد تستجيب المتغيرات التي تجعل المستقبلات مفرطة النشاط بطريقة مختلفة تمامًا، وقد يؤدي حجب المستقبل بشكل مباشر إلى تفاقم بعض جوانب الإشارة. تُظهر الدراسة أن الاعتماد على تنبؤات الحاسوب وحدها لا يكفي: فالاختبارات الوظيفية المباشرة حاسمة للتمييز بين هذه السيناريوهات. من خلال رسم خريطة دقيقة لكيفية تغيير كل متغير لمستقبل GABAB للإشارة، تمهّد هذه الدراسة الطريق لاستراتيجيات علاجية أكثر تفصيلًا في اضطرابات النمو العصبي حيث يختل نظام الكبح في الدماغ.
الاستشهاد: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
الكلمات المفتاحية: مستقبل GABAB, اضطرابات النمو العصبي, متغيرات جينية, طيف التوحد, الطب الدقيق