Clear Sky Science · pl
Funkcjonalne sygnatury nowych wariantów GABBR1 i GABBR2 powiązanych z zaburzeniami neurorozwojowymi
Dlaczego drobne zmiany w chemii mózgu mają znaczenie
Wielu dzieciom z autyzmem, trudnościami w uczeniu się albo zaburzeniami ruchu i uwagi nigdy nie udaje się postawić jasnego biologicznego wyjaśnienia ich objawów. Badanie to koncentruje się na jednej możliwej przyczynie: rzadkich zmian genetycznych, które subtelnie zaburzają sposób, w jaki komórki mózgu reagują na uspokajający związek chemiczny zwany GABA. Śledząc te zmiany od DNA aż po pojedyncze receptory na neuronach, autorzy pokazują, jak małe molekularne usterki mogą przechylić równowagę aktywności mózgu i wskazać drogę do bardziej precyzyjnych, spersonalizowanych terapii.
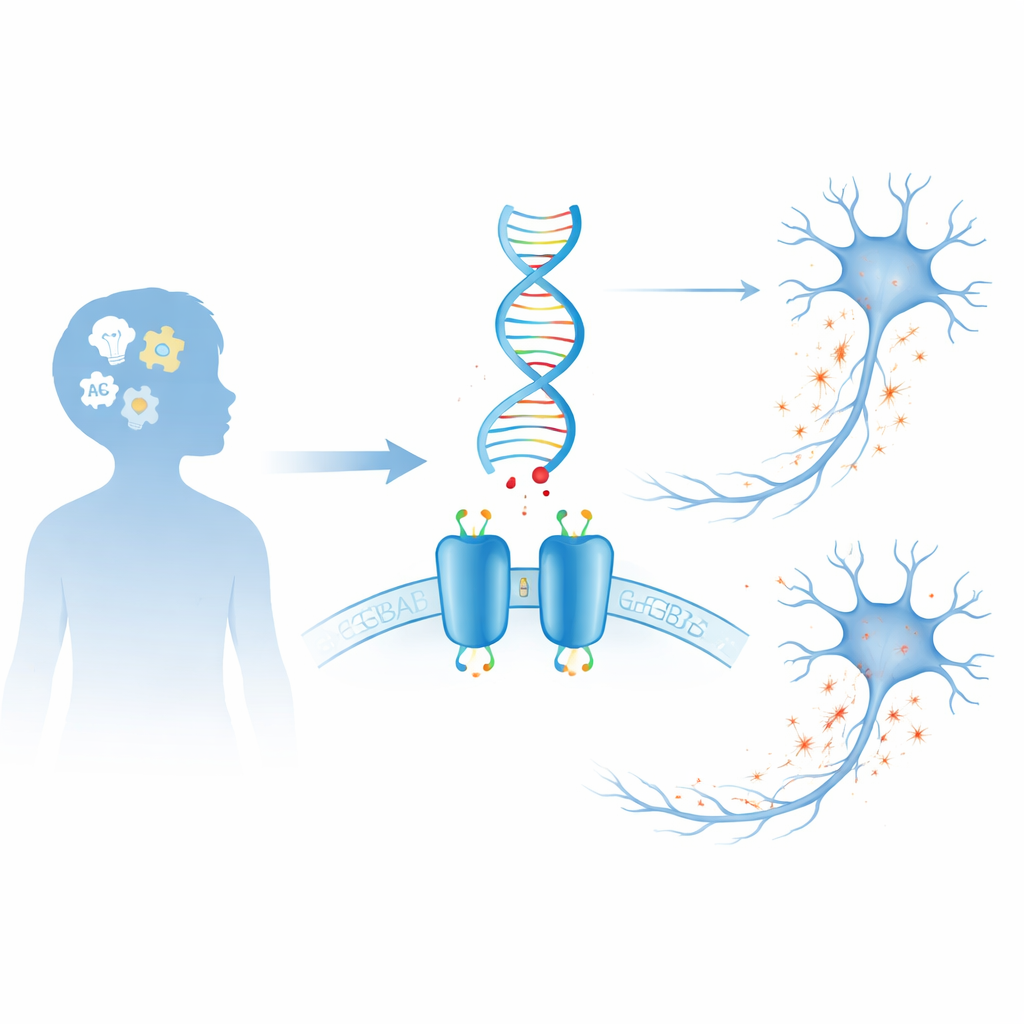
Hamulce mózgu
Nasz mózg opiera się na ciągłej walce między sygnałami pobudzającymi neurony a sygnałami je wyciszającymi. GABA jest głównym „hamulcem” mózgu. Jednym z kluczowych elementów tego systemu jest receptor GABAB, białko złożone z dwóch części, umieszczone na powierzchni neuronów i niektórych komórek podporowych. Gdy GABA wiąże się z receptorem, uruchamia on wewnątrzkomórkowe zmiany obniżające aktywność komórki, co pomaga zapobiegać przeciążeniu, kształtować rytmy mózgowe i dopracowywać komunikację między komórkami. Ponieważ receptor ten odgrywa centralną rolę w kontroli pobudliwości, nawet niewielkie zmiany jego struktury mogą mieć szerokie konsekwencje dla funkcji mózgu i zachowania.
Siedem rzadkich zmian pod lupą
Naukowcy skupili się na siedmiu rzadkich, spontanicznych zmianach w DNA — tzw. wariantach de novo — w genach kodujących dwie połowy receptora GABAB, GABBR1 i GABBR2. Każdy wariant znaleziono u dziecka z problemami neurorozwojowymi, takimi jak opóźnienie mowy i umiejętności motorycznych, niepełnosprawność intelektualna, cechy ze spektrum autyzmu lub trudności z uwagą; u niektórych występowały też napady drgawkowe lub nieprawidłowości ruchowe. Algorytmy komputerowe sugerowały, że warianty te prawdopodobnie są szkodliwe, ale takie prognozy nie mówią, czy receptor staje się nadaktywny, niedoczynny, czy też nieprawidłowo lokowany. Aby to ustalić, zespół odtworzył każdy wariant w komórkach ludzkich w laboratorium i zmierzył, jak zmienione receptory się zachowują.
Kiedy hamulec mózgu przykleja się lub ślizga
Eksperymenty wykazały, że siedem wariantów nie działało jednolicie. Niektóre osłabiały odpowiedź receptora na GABA: potrzebna była znacznie większa ilość związku, by w pełni włączyć receptor, albo mniej receptorów trafiało na powierzchnię komórki. Zmiany te skutecznie zmniejszały dostępne hamowanie w mózgu. Inne warianty miały niemal odwrotny efekt, pozostawiając receptor częściowo włączony nawet przy braku GABA. Ta stała, niskopoziomowa aktywność zwiększała sygnalizację bazową, ale paradoksalnie zmniejszała zdolność dalszej reakcji, gdy poziom GABA wzrastał, osłabiając wpływ prawdziwych sygnałów hamujących podczas intensywnej aktywności mózgowej.
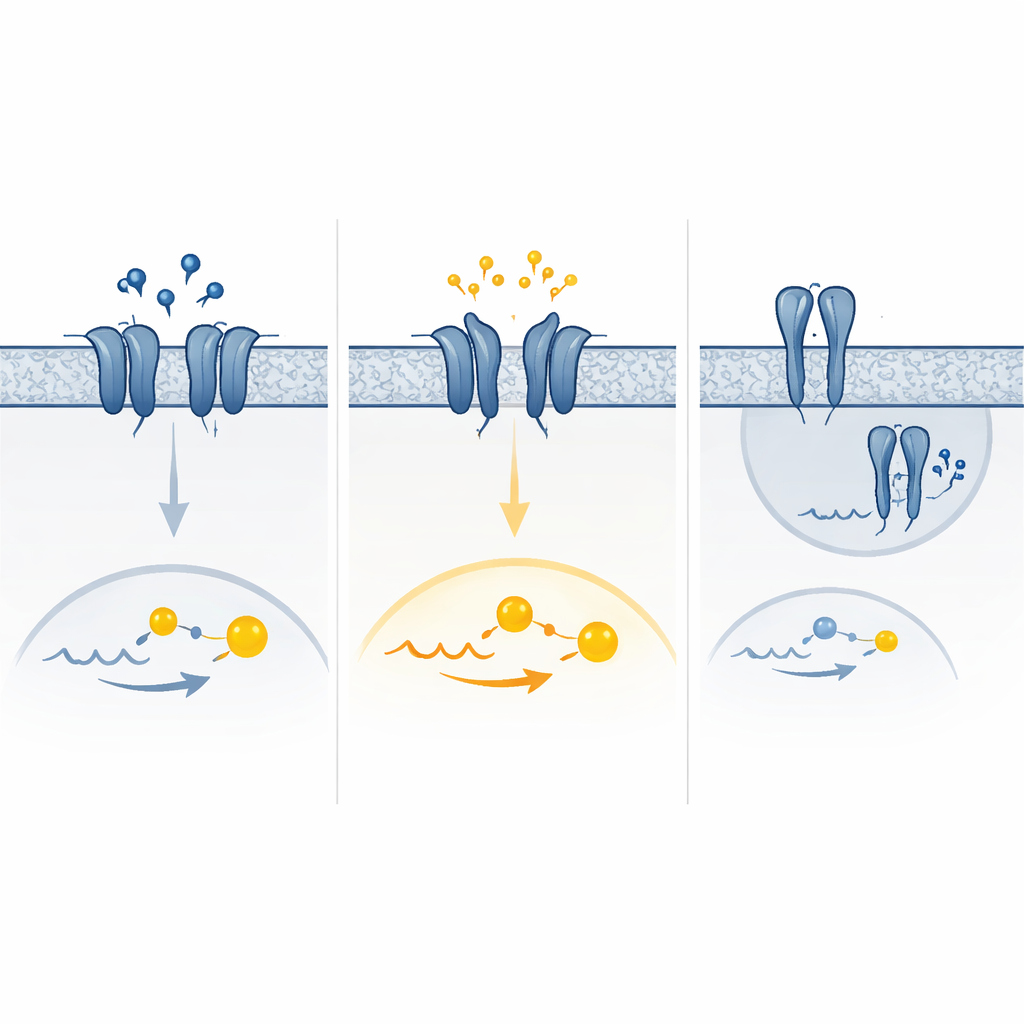
Mieszanka zbyt silnych i zbyt słabych sygnałów
Symulacje komputerowe ruchu receptora pomogły wyjaśnić jeden uderzający wariant, który wykazywał silną aktywność bazową i praktycznie brak odpowiedzi na GABA. W tym przypadku część zewnętrznej „klamry” receptora miała tendencję do samoczynnego zamykania się i utrzymywania kształtu przypominającego stan aktywny, naśladując to, co normalnie dzieje się tylko po związaniu GABA. Inne warianty wydawały się sprzyjać aktywnym układom segmentów przechodzących przez błonę albo zmieniać sposób, w jaki pary receptorów się składują i docierają na powierzchnię komórki. Efekt końcowy to spektrum zmian — czysta utrata funkcji, czysty zysk funkcji lub kombinacja obu, zależnie od poziomów GABA i tego, jak komórki z czasem adaptują się przez usuwanie lub obniżanie regulacji nadaktywowanych receptorów.
Implikacje dla leczenia spersonalizowanego
Choć dzieci miały nakładające się objawy, leżące u ich podstaw problemy z receptorami były bardzo różne. To odkrycie ma znaczenie dla terapii. Warianty zmniejszające liczbę lub czułość receptorów mogą być pomocne przy lekach wzmacniających efekt GABA na pozostałych, prawidłowych receptorach. Natomiast warianty powodujące nadmierną aktywność receptorów mogą reagować zupełnie inaczej, a proste blokowanie receptora może pogorszyć pewne aspekty sygnalizacji. Badanie pokazuje, że poleganie wyłącznie na przewidywaniach komputerowych nie wystarcza: konieczne są bezpośrednie testy funkcjonalne, aby odróżnić te scenariusze. Mapując dokładnie, jak każdy wariant receptora GABAB zmienia sygnalizację, praca ta tworzy podstawy do bardziej dopasowanych strategii leczenia w zaburzeniach neurorozwojowych, w których system hamowania mózgu działa nieprawidłowo.
Cytowanie: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Słowa kluczowe: receptor GABAB, zaburzenia neurorozwojowe, warianty genetyczne, spektrum autyzmu, medycyna precyzyjna