Clear Sky Science · de
Funktionelle Kennzeichen de novo GABBR1- und GABBR2-Varianten, die mit neuroentwicklungsbedingten Störungen assoziiert sind
Warum winzige Veränderungen in der Hirnchemie wichtig sind
Viele Kinder mit Autismus, Lernschwierigkeiten oder Bewegungs- und Aufmerksamkeitsproblemen erhalten nie eine klare biologische Erklärung für ihre Symptome. Diese Studie untersucht eine mögliche Ursache: seltene genetische Veränderungen, die auf subtile Weise beeinflussen, wie Nervenzellen auf eine beruhigende Botensubstanz namens GABA reagieren. Indem die Forscher diese Veränderungen vom DNA-Level bis zu einzelnen Rezeptoren auf Neuronen zurückverfolgen, zeigen sie, wie kleine molekulare Fehler das Gleichgewicht der Hirnaktivität kippen können und Wege zu präziseren, personalisierten Behandlungen aufzeigen.
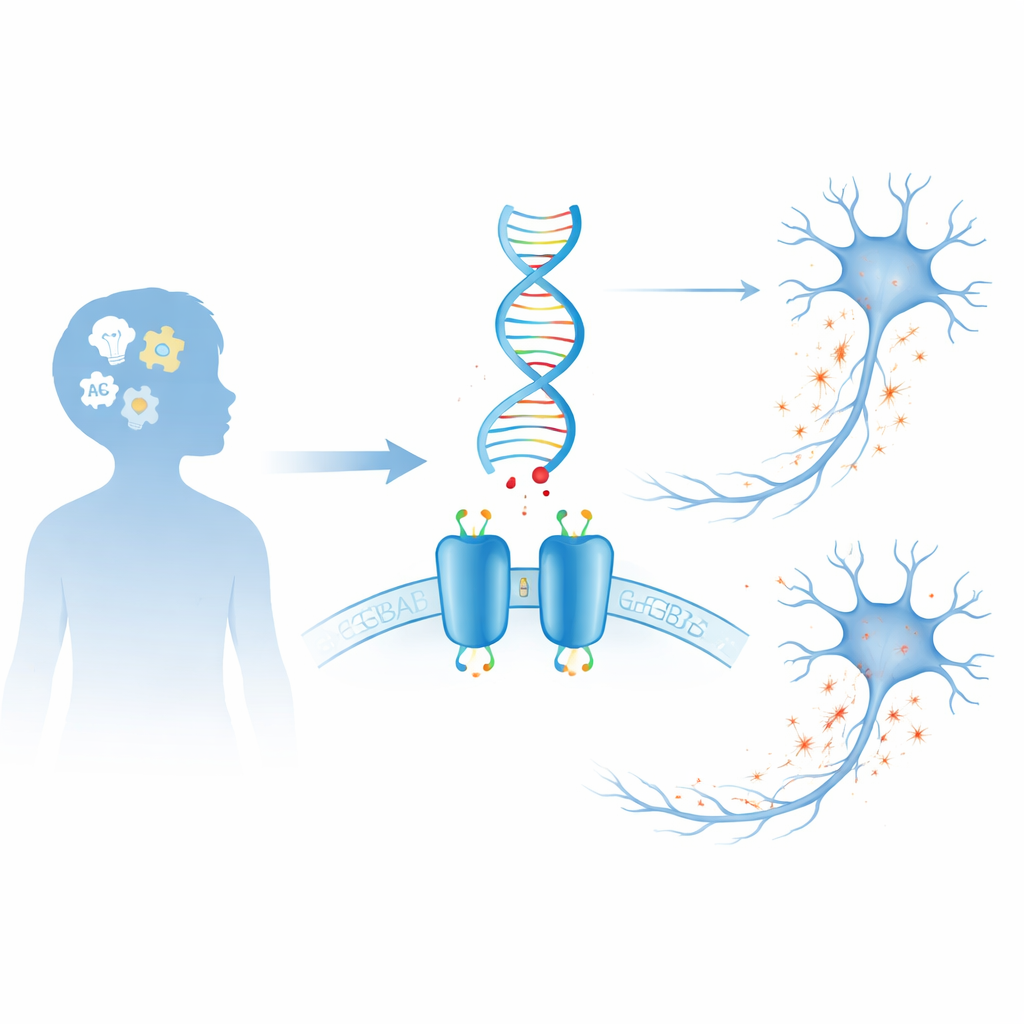
Das Bremssystem des Gehirns
Unser Gehirn beruht auf einem dauerhaften Tauziehen zwischen Signalen, die Neurone erregen, und solchen, die sie beruhigen. GABA ist die wichtigste „Bremse“ des Gehirns. Eines der zentralen Instrumente dafür ist der GABAB-Rezeptor, ein zweiteiliges Protein, das auf der Oberfläche von Neuronen und einigen Stützzellen sitzt. Wenn GABA bindet, löst der Rezeptor interne Veränderungen aus, die die zelluläre Aktivität senken, Überlastung verhindern, Hirnrhythmen formen und die Kommunikation zwischen Zellen feinabstimmen. Da dieser Rezeptor so zentral für die Kontrolle der Erregbarkeit ist, können schon leichte Veränderungen seiner Struktur weitreichende Auswirkungen auf Gehirnfunktion und Verhalten haben.
Sieben seltene genetische Veränderungen unter dem Mikroskop
Die Forscher konzentrierten sich auf sieben seltene, spontane DNA-Veränderungen – sogenannte de novo-Varianten – in den Genen, die die beiden Hälften des GABAB-Rezeptors kodieren, GABBR1 und GABBR2. Jede Variante wurde bei einem Kind mit neuroentwicklungsbedingten Problemen gefunden, etwa verzögerter Sprach- und Motorikentwicklung, geistiger Behinderung, autistischen Merkmalen oder Aufmerksamkeitsstörungen; einige hatten zusätzlich Anfälle oder Bewegungsauffälligkeiten. Computeralgorithmen deuteten alle darauf hin, dass diese Varianten wahrscheinlich schädlich sind, aber solche Vorhersagen sagen nicht, ob ein Rezeptor überaktiv, unteraktiv oder fehlplatziert ist. Um das zu klären, rekonstruierten die Wissenschaftler jede Variante in menschlichen Zellen im Labor und maßen, wie sich die veränderten Rezeptoren verhielten.
Wenn die Bremsen des Gehirns kleben oder durchrutschen
Die Experimente zeigten, dass die sieben Varianten nicht alle gleich wirkten. Manche schwächten die Reaktion des Rezeptors auf GABA: wesentlich mehr des Neurotransmitters war nötig, um den Rezeptor vollständig zu aktivieren, oder weniger Rezeptoren gelangten überhaupt an die Zelloberfläche. Diese Veränderungen reduzierten effektiv die verfügbare Bremskraft im Gehirn. Andere Varianten hatten nahezu den entgegengesetzten Effekt und ließen den Rezeptor teilweise aktiviert, selbst wenn kein GABA vorhanden war. Diese konstante Niedrigaktivität erhöhte die Basissignalisierung, ließ paradox weniger Spielraum für weitere Reaktionen, wenn GABA anstieg, und schwächte die Wirkung echter hemmender Signale bei intensiver Hirnaktivität.
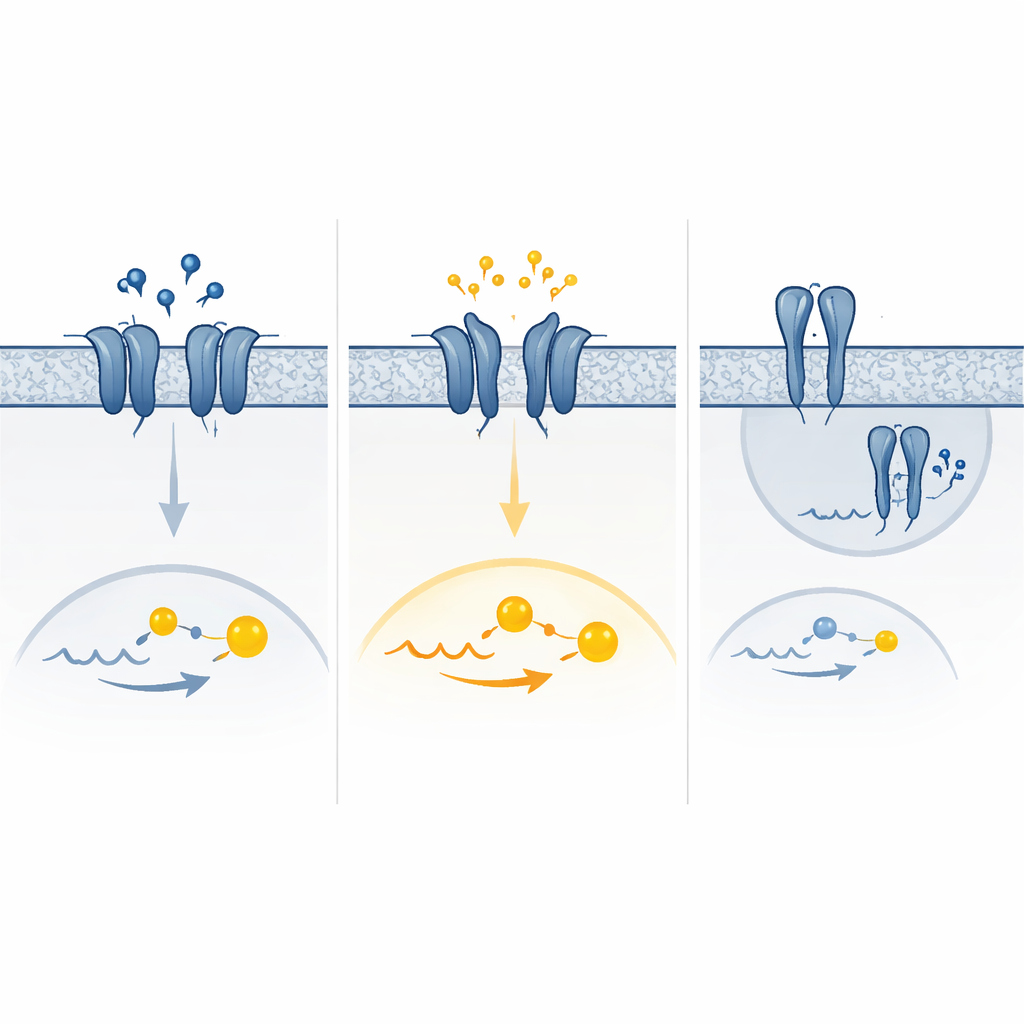
Ein Mix aus zu viel und zu wenig Signal
Computersimulationen der Rezeptorbewegung halfen, eine auffällige Variante zu erklären, die starke Basisaktivität und praktisch keine Reaktion auf GABA zeigte. In diesem Fall neigte ein Teil der äußeren „Klammer“-Domäne des Rezeptors dazu, sich von selbst zu schließen und in einer aktiven-ähnlichen Form zu verharren, was das imitiert, was normalerweise nur bei GABA-Bindung geschieht. Andere Varianten schienen aktive Anordnungen der membranüberspannenden Segmente des Rezeptors zu begünstigen oder veränderten, wie Rezeptorpärchen assemblierten und die Zelloberfläche erreichten. Das Endergebnis war ein Spektrum an Effekten – reiner Funktionsverlust, reine Funktionssteigerung oder eine Kombination aus beidem, abhängig von den GABA-Spiegeln und davon, wie Zellen im Laufe der Zeit durch Entfernung oder Herunterregulierung überaktiver Rezeptoren reagieren.
Folgen für personalisierte Therapien
Obwohl die Kinder überlappende Symptome zeigten, waren die zugrundeliegenden Rezeptorprobleme ganz unterschiedlich. Das ist für die Therapie entscheidend. Varianten, die Rezeptoranzahl oder -empfindlichkeit reduzieren, könnten von Medikamenten profitieren, die die Wirkung von GABA auf die verbleibenden normalen Rezeptoren verstärken. Im Gegensatz dazu könnten Varianten, die Rezeptoren zu aktiv machen, sehr unterschiedlich reagieren, und ein einfaches Blockieren des Rezeptors könnte bestimmte Signalaspekte sogar verschlechtern. Die Studie zeigt, dass man sich nicht allein auf Computervorhersagen verlassen kann: Direkte funktionelle Tests sind entscheidend, um zwischen diesen Szenarien zu unterscheiden. Indem sie genau abbilden, wie jede GABAB-Rezeptor-Variante die Signalübertragung verändert, schafft diese Arbeit die Grundlage für gezieltere Behandlungsstrategien bei neuroentwicklungsbedingten Störungen, bei denen das Bremssystem des Gehirns aus dem Gleichgewicht gerät.
Zitation: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Schlüsselwörter: GABAB-Rezeptor, neuroentwicklungsbedingte Störungen, genetische Varianten, Autismus-Spektrum, präzisionsmedizin