Clear Sky Science · es
Firmas funcionales de variantes de novo en GABBR1 y GABBR2 asociadas a trastornos del neurodesarrollo
Por qué importan los pequeños cambios en la química cerebral
Muchos niños con autismo, dificultades de aprendizaje o problemas de movimiento y atención nunca reciben una explicación biológica clara para sus síntomas. Este estudio examina una causa posible: cambios genéticos raros que distorsionan sutilmente cómo las células cerebrales responden a un químico calmante llamado GABA. Al rastrear estos cambios desde el ADN hasta receptores individuales en las neuronas, los investigadores muestran cómo pequeños fallos moleculares pueden inclinar el equilibrio de la actividad cerebral y apuntar hacia tratamientos más precisos y personalizados.
El sistema de freno del cerebro
Nuestros cerebros dependen de un tira y afloja constante entre señales que excitan a las neuronas y señales que las calman. El GABA es el principal químico “freno” del cerebro. Uno de los dispositivos clave que emplea es el receptor GABAB, una proteína de dos partes que se sitúa en la superficie de las neuronas y de algunas células de soporte. Cuando el GABA se une, el receptor desencadena cambios internos que reducen la actividad celular, ayudando a prevenir sobrecargas, a dar forma a los ritmos cerebrales y a afinar la comunicación entre células. Dado que este receptor es tan central en el control de la excitabilidad, incluso cambios leves en su estructura pueden tener efectos de gran alcance sobre la función cerebral y el comportamiento.
Siete cambios genéticos raros bajo el microscopio
Los investigadores se centraron en siete cambios raros y espontáneos en el ADN —llamados variantes de novo— en los genes que codifican las dos mitades del receptor GABAB, GABBR1 y GABBR2. Cada variante se encontró en un niño con problemas del neurodesarrollo como retraso del lenguaje y de las habilidades motoras, discapacidad intelectual, rasgos del espectro autista o dificultades de atención; algunos también tenían convulsiones o anormalidades del movimiento. Los algoritmos informáticos sugerían de forma uniforme que estas variantes eran probablemente dañinas, pero tales predicciones no pueden decir si un receptor se vuelve hiperactivo, hipoactivo o se localiza mal. Para responder a eso, el equipo recreó cada variante en células humanas en el laboratorio y midió cómo se comportaban los receptores alterados.
Cuando el freno cerebral se queda pegado o patina
Los experimentos revelaron que las siete variantes no actuaban todas de la misma manera. Algunas debilitaban la respuesta del receptor al GABA: se necesitaba mucha más cantidad del químico para activar completamente el receptor, o menos receptores alcanzaban la superficie celular. Estos cambios redujeron efectivamente la potencia de frenado disponible en el cerebro. Otras variantes tuvieron casi el efecto opuesto, dejando el receptor parcialmente activado aun cuando no había GABA presente. Esta actividad constante a bajo nivel aumentaba la señalización basal pero paradójicamente dejaba menos margen para una respuesta adicional cuando los niveles de GABA aumentaban, atenuando el impacto de las señales inhibitorias reales durante períodos de intensa actividad cerebral.
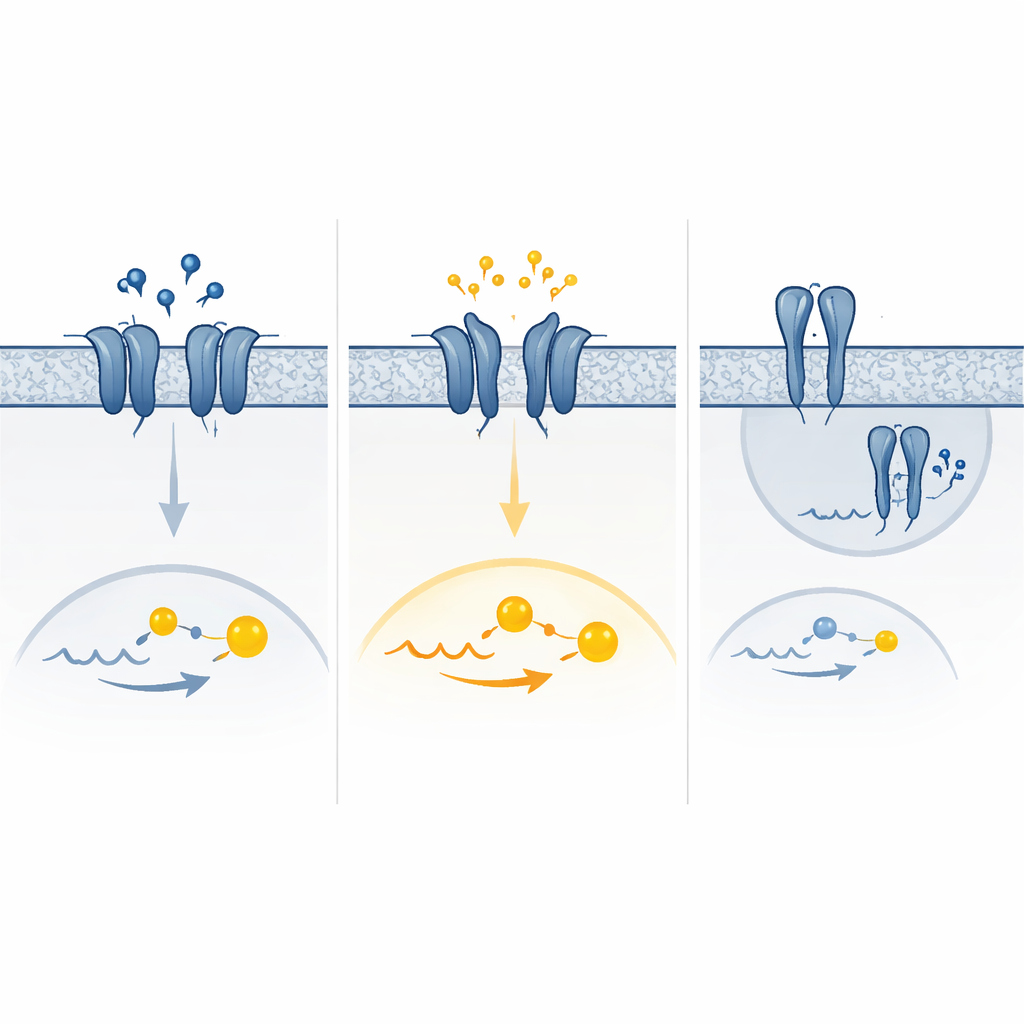
Una mezcla de señal demasiado alta y demasiado baja
Simulaciones informáticas del movimiento del receptor ayudaron a explicar una variante llamativa que mostraba una fuerte actividad basal y virtualmente ninguna respuesta al GABA. En este caso, parte del dominio exterior “abrazadera” del receptor tendía a cerrarse por sí sola y permanecer en una conformación similar a la activa, imitando lo que normalmente ocurre solo cuando el GABA está ligado. Otras variantes parecían favorecer disposiciones activas de los segmentos transmembrana del receptor o alteraban cómo los pares de receptores se ensamblaban y alcanzaban la superficie celular. El resultado final fue un espectro de efectos —pérdida pura de función, ganancia pura de función o una combinación de ambas dependiendo de los niveles de GABA y de cómo las células se adaptan con el tiempo eliminando o regulando a la baja los receptores hiperactivos.
Implicaciones para el tratamiento personalizado
Aunque los niños compartían síntomas superpuestos, los problemas subyacentes en los receptores eran muy distintos. Este hallazgo es importante para la terapia. Las variantes que reducen el número o la sensibilidad de los receptores podrían beneficiarse de fármacos que potencien el efecto del GABA sobre los receptores normales restantes. En contraste, las variantes que hacen que los receptores estén demasiado activos podrían responder de manera muy diferente, y bloquear simplemente el receptor podría empeorar ciertos aspectos de la señalización. El estudio demuestra que confiar solo en predicciones informáticas no es suficiente: las pruebas funcionales directas son cruciales para distinguir entre estos escenarios. Al mapear exactamente cómo cada variante del receptor GABAB modifica la señalización, este trabajo sienta las bases para estrategias de tratamiento más personalizadas en trastornos del neurodesarrollo donde el sistema de freno cerebral falla.
Cita: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Palabras clave: Receptor GABAB, trastornos del neurodesarrollo, variantes genéticas, espectro autista, medicina de precisión