Clear Sky Science · fr
Signatures fonctionnelles de variants de novo de GABBR1 et GABBR2 associés à des troubles du développement neurologique
Pourquoi de petites modifications de la chimie cérébrale comptent
Beaucoup d’enfants atteints d’autisme, de difficultés d’apprentissage ou de troubles du mouvement et de l’attention ne reçoivent jamais d’explication biologique claire à leurs symptômes. Cette étude examine une cause possible : des modifications génétiques rares qui altèrent subtilement la manière dont les cellules cérébrales répondent à un produit chimique calmant appelé GABA. En retraçant ces changements de l’ADN jusqu’aux récepteurs individuels sur les neurones, les chercheurs montrent comment de petites défaillances moléculaires peuvent faire basculer l’équilibre de l’activité cérébrale et indiquer des pistes pour des traitements plus précis et personnalisés.
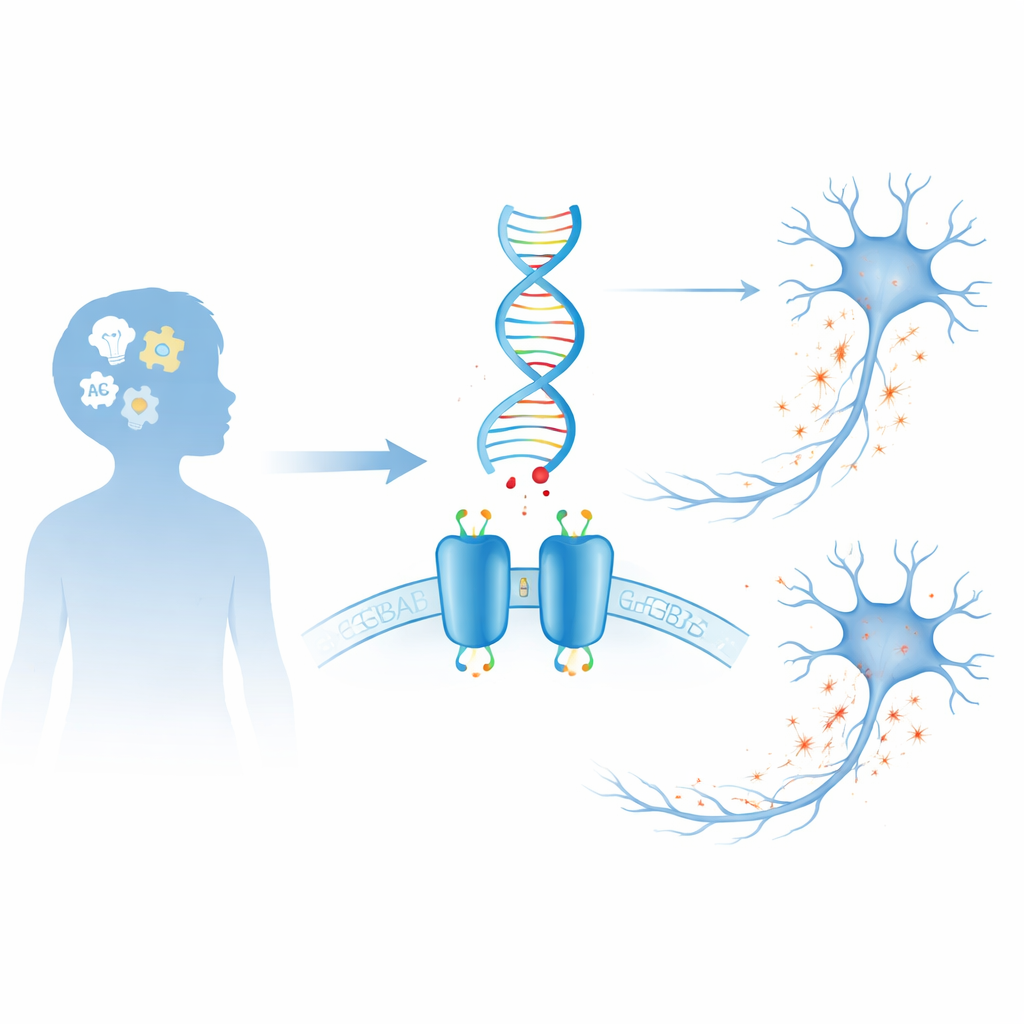
Le système de freinage du cerveau
Nos cerveaux reposent sur un combat constant entre des signaux qui excitent les neurones et des signaux qui les apaisent. Le GABA est le principal « frein » chimique du cerveau. L’un des dispositifs clés qu’il utilise est le récepteur GABAB, une protéine en deux parties qui se trouve à la surface des neurones et de certaines cellules de soutien. Lorsque le GABA se lie, le récepteur déclenche des changements internes qui réduisent l’activité cellulaire, aidant à prévenir la surcharge, à modeler les rythmes cérébraux et à affiner la communication entre cellules. Parce que ce récepteur est central pour contrôler l’excitabilité, même de légères modifications de sa structure peuvent avoir des effets étendus sur la fonction cérébrale et le comportement.
Sept variants génétiques rares passés au crible
Les chercheurs se sont concentrés sur sept modifications d’ADN rares et spontanées — appelées variants de novo — dans les gènes codant les deux moitiés du récepteur GABAB, GABBR1 et GABBR2. Chaque variant a été trouvé chez un enfant présentant des troubles du développement neurologique tels que retard de la parole et des compétences motrices, déficience intellectuelle, caractéristiques du spectre autistique ou difficultés d’attention ; certains présentaient aussi des crises d’épilepsie ou des anomalies du mouvement. Les algorithmes informatiques suggéraient tous que ces variants étaient probablement délétères, mais ces prédictions ne renseignent pas sur le fait qu’un récepteur devienne hyperactif, hypoactif ou mal localisé. Pour répondre à cette question, l’équipe a recréé chaque variant dans des cellules humaines en laboratoire et a mesuré le comportement des récepteurs altérés.
Quand le frein du cerveau colle ou glisse
Les expériences ont révélé que les sept variants n’agissaient pas tous de la même façon. Certains affaiblissaient la réponse du récepteur au GABA : il fallait beaucoup plus de la molécule pour activer complètement le récepteur, ou moins de récepteurs atteignaient la surface cellulaire. Ces changements réduisaient effectivement la capacité de freinage disponible dans le cerveau. D’autres variants présentaient presque l’effet inverse, laissant le récepteur partiellement activé même en l’absence de GABA. Cette activité basale constante augmentait le signal de fond mais, paradoxalement, laissait moins de marge pour une réponse supplémentaire lorsque les niveaux de GABA augmentaient, atténuant l’impact des véritables signaux inhibiteurs lors d’une activité cérébrale intense.
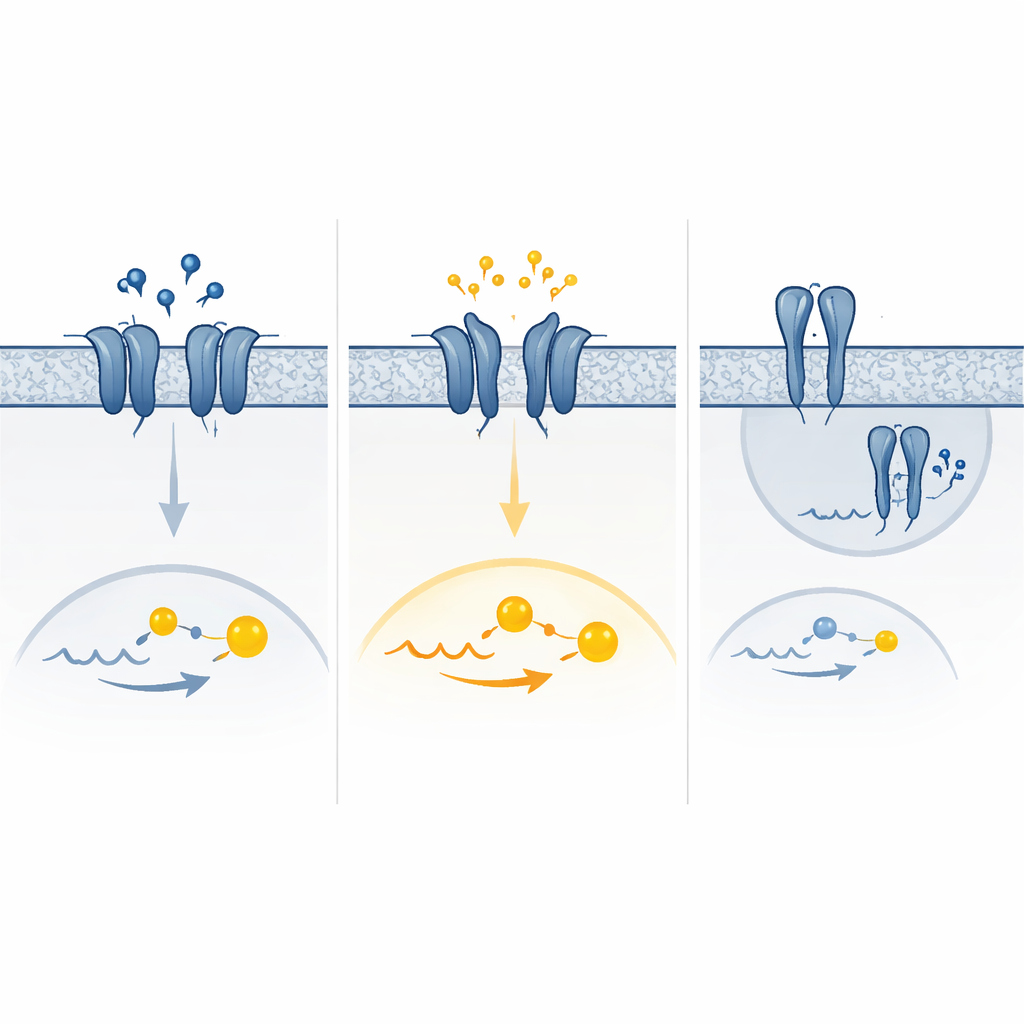
Un mélange de signaux trop forts et trop faibles
Des simulations informatiques du mouvement des récepteurs ont aidé à expliquer un variant frappant qui montrait une forte activité basale et pratiquement aucune réponse au GABA. Dans ce cas, une partie du domaine externe « pince » du récepteur avait tendance à se refermer spontanément et à rester dans une conformation proche de l’état actif, imitant ce qui se produit normalement seulement lorsque le GABA est lié. D’autres variants semblaient favoriser des arrangements actifs des segments transmembranaires du récepteur ou modifiaient la manière dont les paires de récepteurs s’assemblaient et atteignaient la surface cellulaire. Le résultat final était un spectre d’effets — perte de fonction pure, gain de fonction pur, ou une combinaison des deux selon les niveaux de GABA et la manière dont les cellules s’adaptent au fil du temps en éliminant ou en régulant à la baisse les récepteurs hyperactifs.
Conséquences pour un traitement personnalisé
Bien que les enfants partageaient des symptômes qui se recoupaient, les problèmes récepteurs sous-jacents étaient assez différents. Cette constatation a des implications pour la thérapie. Les variants qui réduisent le nombre ou la sensibilité des récepteurs pourraient bénéficier de médicaments qui augmentent l’effet du GABA sur les récepteurs normaux restants. En revanche, les variants qui rendent les récepteurs trop actifs pourraient répondre très différemment, et bloquer simplement le récepteur pourrait aggraver certains aspects de la signalisation. L’étude montre que s’en remettre uniquement aux prédictions informatiques ne suffit pas : des tests fonctionnels directs sont essentiels pour distinguer ces scénarios. En cartographiant exactement comment chaque variant du récepteur GABAB modifie la signalisation, ce travail jette les bases de stratégies de traitement plus adaptées dans les troubles du développement neurologique où le système de freinage du cerveau dysfonctionne.
Citation: Stawarski, M., Bielopolski, N., Roitman, I. et al. Functional signatures of de novo GABBR1 and GABBR2 variants associated with neurodevelopmental disorders. npj Genom. Med. 11, 23 (2026). https://doi.org/10.1038/s41525-026-00558-z
Mots-clés: récepteur GABAB, troubles du développement neurologique, variants génétiques, trouble du spectre autistique, médecine de précision