Clear Sky Science · ru
Раскрытие механизма сохранения конфигурации через «переворачивание» в газофазной реакции Cl− + (CH3)3CI типа SN2
Почему важны крошечные столкновения
Каждую секунду бесчисленное множество химических реакций формируют окружающий нас мир — от действия лекарств до горения топлива. Многие из этих реакций следуют нескольким учебным шаблонам, которые студенты изучают в вводных курсах химии. В этой работе рассматривается очень знакомый тип реакции — когда одна маленькая заряженная частица меняется местами с другой в органической молекуле — и показано, что реальность более удивительна, чем стандартная картина. Наблюдая отдельные молекулы во время столкновений в газовой фазе и моделируя их движение подробно, авторы обнаруживают новый способ перестройки атомов, которого раньше не видели.
Два конкурирующих пути реакции
Когда отрицательно заряженный ион хлора встречает громоздкую молекулу трет-бутилйодида, возможны два основных исхода. В одном пути, известном как замещение, хлор занимает место йода в углеродном скелете. В другом, называемом элиминированием, хлор захватывает атом водорода, а углеродный каркас перестраивается с образованием двойной связи, в то время как йод уходит отдельно. Химики обозначают эти маршруты как SN2 и E2, но по сути это два разных способа, которыми одни и те же ингредиенты могут перестроиться. Понимание того, какой путь выигрывает и почему, имеет решающее значение для проектирования реакций, дающих желаемый продукт в синтетической химии.
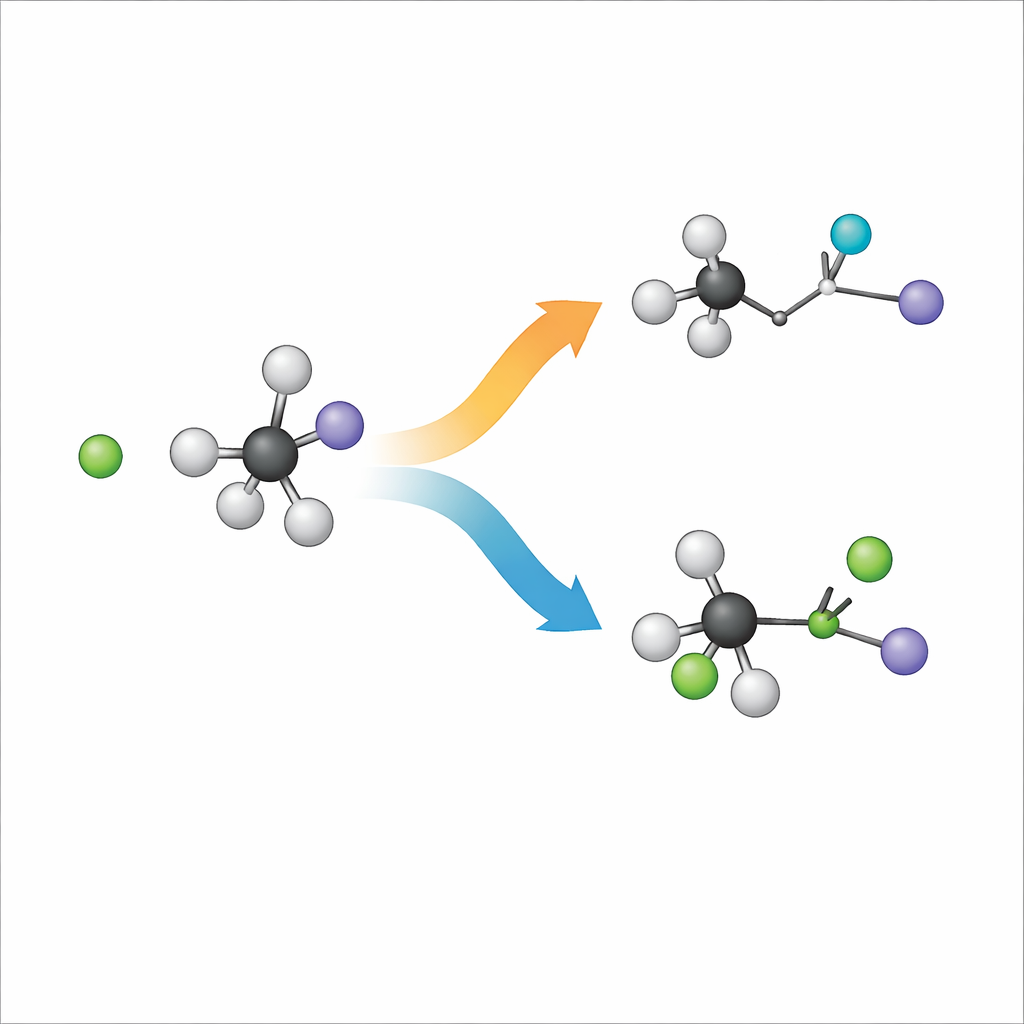
Съёмка реакций «в воздухе»
Чтобы выяснить, что действительно происходит, исследователи устраняют помехи растворителей и изучают реакцию в газовой фазе, где отдельные ионы и молекулы сталкиваются в почти вакууме. Они пересекают пучок ионов хлора с пучком трет-бутилйодида и используют специализированную систему визуализации, чтобы зафиксировать трехмерные скорости и направления фрагментов, содержащих йод, которые отлетают. Одновременно они строят чрезвычайно детальную «карту» сил между всеми 15 атомами с помощью машинного обучения, обученного на высокоуровневых квантово-химических расчётах. Затем они запускают миллионы смоделированных траекторий на этом 39-мерном ландшафте, чтобы проследить, как атомы движутся при каждом столкновении.
Элиминирование выходит в лидеры
Экспериментальные изображения и компьютерные симуляции удивительно хорошо согласуются, что вселяет уверенность в правильность захвата реакции. Оба показывают, что путь элиминирования доминирует: в большинстве столкновений система идет по маршруту E2, особенно по мере увеличения энергии столкновения. В этих событиях продукты несут много внутренней колебательной энергии — большая часть дополнительной энергии идет на колебания и изгибы новых молекул, а не просто на их разлетание. Такое поведение согласуется с ранними работами по родственным системам и подчеркивает, как громоздкий углеродный каркас трет-бутилйодида отводит реакцию от простого замещения.
Новый тип молекулярного «переворота»
В пределах меньшей доли событий замещения команда обнаруживает нечто неожиданное. Классическая картина SN2 предполагает «задний» удар: входящий ион подходит с противоположной стороны от уходящей группы, и центральный углерод инвертирует свою геометрию, как зонт, выворачивающийся наизнанку. Эта инверсия меняет трёхмерную «правую/левую» форму молекулы. Здесь симуляции показывают дополнительный, отличающийся маршрут. В недавно обнаруженном механизме «переворота» хлор сначала приближается и растягивает связь между углеродом и йодом. Громоздная трет-бутильная группа затем переворачивается как единое целое, словно лист страницы, в то время как хлор окончательно связывается с центральным углеродом, а йод уходит. Поскольку углеродный каркас переворачивается, а не инвертирует, общая пространственная организация вокруг ключевого атома углерода сохраняется, а не меняется на обратную.
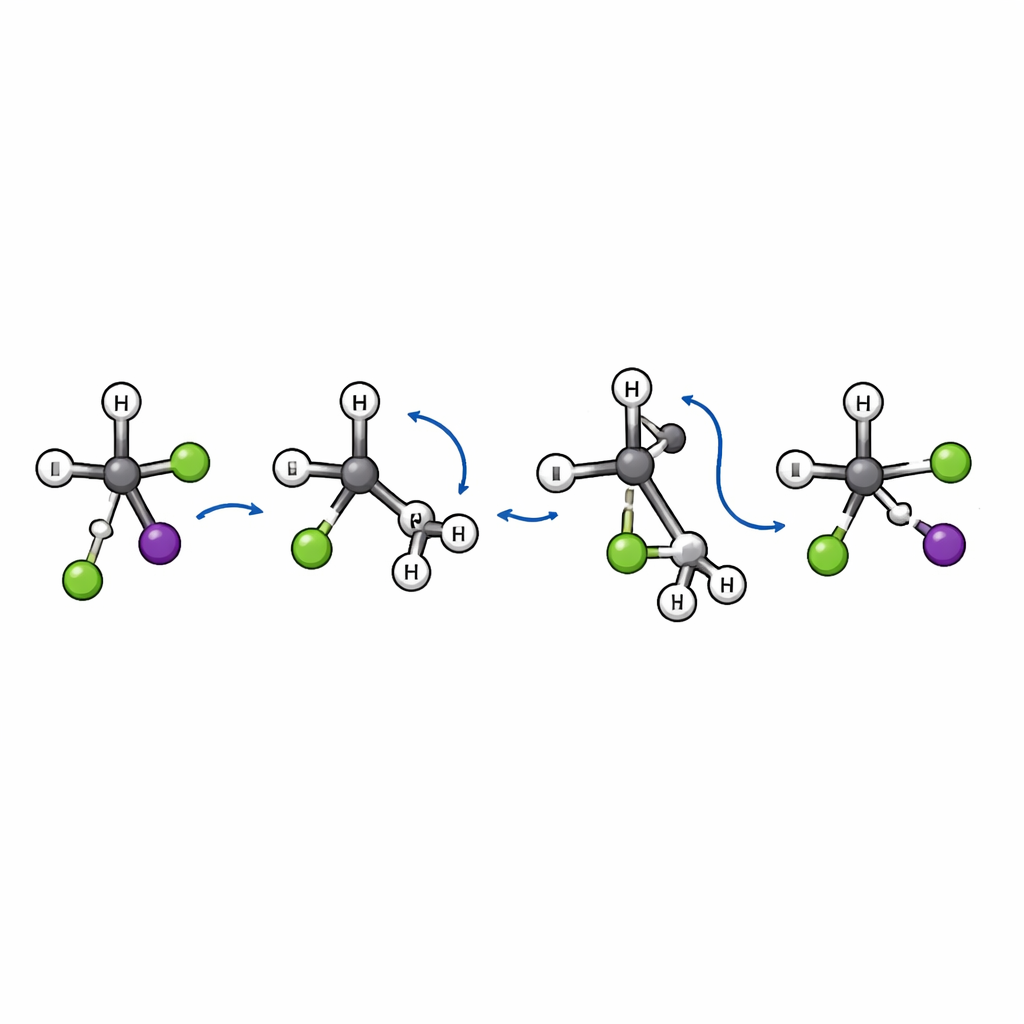
Признаки движения «переворота»
Этот путь через переворот оставляет четкие отпечатки в картинах рассеяния. События замещения, которые идут через обычную инверсию, как правило, посылают йодный фрагмент назад относительно входящего хлора. Напротив, траектории, следующие маршруту переворота, в основном рассеивают йод вперед, что указывает на очень прямой характер столкновения и на то, что вращательное движение громоздкой группы играет ключевую роль. Авторы также идентифицируют специфическое переходное состояние — некую энергетическую «врата», — которое соединяет реагенты и продукты вдоль этого нового пути, подтверждая, что это подлинный и отдельный механизм, а не незначительное вариация известных путей.
Что это значит для химии
Комбинируя передовые эксперименты с точным, обученным машинно энергетическим ландшафтом, это исследование показывает, что даже один из наиболее изученных типов реакций всё ещё хранит сюрпризы. Открытие маршрута переворота, который сохраняет трёхмерную организацию атомов, расширяет известные способы, которыми реакции замещения могут контролировать форму молекулы. На практическом уровне такие инсайты помогают химикам лучше предсказывать, когда будут образовываться определённые продукты, особенно в «переполненных» молекулах, где тонкие движения углеродного каркаса имеют значение. По мере того как аналогичные методы применяются к более сложным системам, могут выявиться и другие скрытые пути, уточняя наше представление о микроскопической хореографии химических превращений.
Цитирование: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Ключевые слова: реакции SN2, динамика реакций, стереохимия, элиминирование против замещения, имиджинг молекулярных столкновений