Clear Sky Science · it
Rivelato un meccanismo di mantenimento tramite ribaltamento nella reazione SN2 in fase gassosa Cl− + (CH3)3CI
Perché le collisioni microscopiche contano
Ogni secondo, innumerevoli reazioni chimiche modellano il mondo che ci circonda, da come funzionano i farmaci a come bruciano i combustibili. Molte di queste reazioni seguono pochi schemi da manuale che gli studenti imparano nella chimica introduttiva. Questo articolo prende un tipo di reazione molto familiare — dove una piccola particella carica scambia posto con un’altra in una molecola organica — e mostra che la realtà è più sorprendente rispetto all’immagine standard. Osservando singole molecole scontrarsi in fase gassosa e simulando i loro moti nei dettagli, gli autori scoprono un nuovo modo in cui gli atomi possono riordinarsi, uno che non era stato osservato prima.
Due percorsi reazionali concorrenti
Quando uno ione cloruro carico negativamente incontra una molecola ingombrante chiamata ioduro di tert-butile, sono possibili due esiti principali. In un percorso, noto come sostituzione, il cloruro prende il posto dello iodio nello scheletro carbonioso. Nell’altro, chiamato eliminazione, il cloruro strappa invece un atomo di idrogeno e lo scheletro carbonioso si riorganizza formando un doppio legame mentre lo iodio se ne allontana separatamente. I chimici etichettano queste vie come SN2 ed E2, ma nel profondo sono due modi diversi in cui gli stessi ingredienti possono riordinarsi. Capire quale percorso prevale, e perché, è cruciale per progettare reazioni che diano il prodotto desiderato nella chimica sintetica.
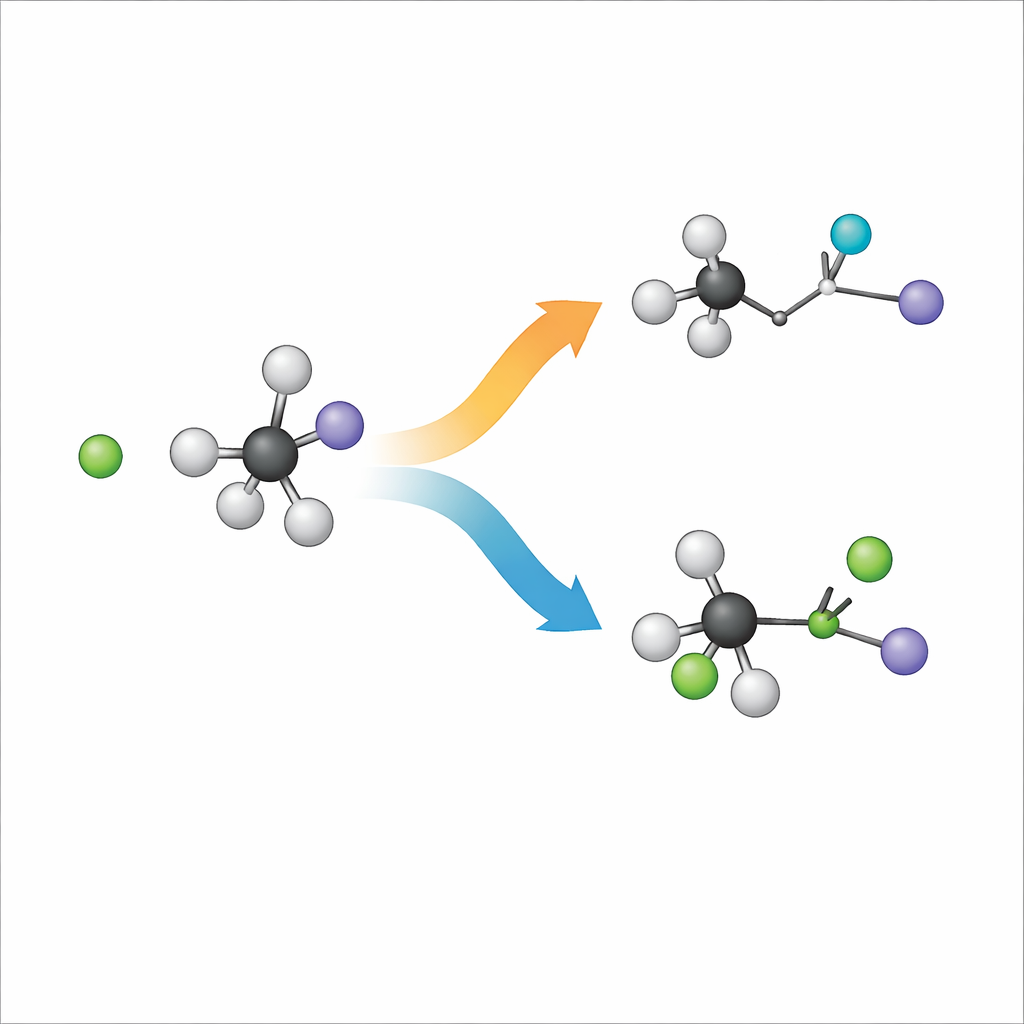
Riprendere le reazioni a mezz’aria
Per scoprire cosa succede realmente, i ricercatori eliminano il disturbo dei solventi e studiano la reazione in fase gassosa, dove singoli ioni e molecole collidono in un quasi-vuoto. Incrociano un fascio di ioni cloruro con un fascio di ioduro di tert-butile e usano un apparato di imaging specializzato per registrare le velocità e le direzioni tridimensionali dei frammenti contenenti iodio che vengono espulsi. Allo stesso tempo costruiscono una mappa estremamente dettagliata delle forze tra tutti i 15 atomi usando un approccio di apprendimento automatico addestrato su calcoli quantistici di alto livello. Lanciano quindi milioni di traiettorie simulate su questo paesaggio a 39 dimensioni per seguire come gli atomi si muovono durante ogni collisione.
L’eliminazione prende il sopravvento
Le immagini sperimentali e le simulazioni al computer coincidono in modo sorprendente, dando fiducia che la reazione sia catturata con precisione. Entrambe mostrano che il percorso di eliminazione domina: la maggior parte delle collisioni porta il sistema lungo la via E2, specialmente quando aumenta l’energia di collisione. In questi eventi, i prodotti trasferiscono molta energia interna vibrazionale — la maggior parte dell’energia in eccesso finisce per far vibrare e torcere le nuove molecole piuttosto che semplicemente separarle. Questo comportamento corrisponde a lavori precedenti su sistemi correlati e mette in evidenza come lo scheletro carbonioso ingombrante dell’ioduro di tert-butile indirizzi la reazione lontano dalla semplice sostituzione.
Un nuovo tipo di ribaltamento molecolare
All’interno della frazione minore di eventi di sostituzione, il gruppo trova qualcosa di inatteso. L’immagine classica della SN2 implica un «attacco dal retro»: lo ione entrante si avvicina dietro il gruppo uscente e il carbonio centrale inverte la sua geometria, come un ombrello che si gira all’inverso. Quell’inversione cambia la maneggevolezza tridimensionale della molecola. Qui, le simulazioni rivelano una via aggiuntiva e distinta. In questo meccanismo di nuova scoperta, chiamato «flip-over», il cloruro si avvicina inizialmente e allunga il legame tra carbonio e iodio. Il voluminoso gruppo tert-butile poi si capovolge come un’unità, come una pagina che viene girata, mentre il cloruro alla fine si lega al carbonio centrale e lo iodio parte. Poiché lo scheletro carbonioso si ribalta invece di invertirsi, la disposizione spaziale complessiva attorno all’atomo di carbonio chiave viene mantenuta anziché invertita.
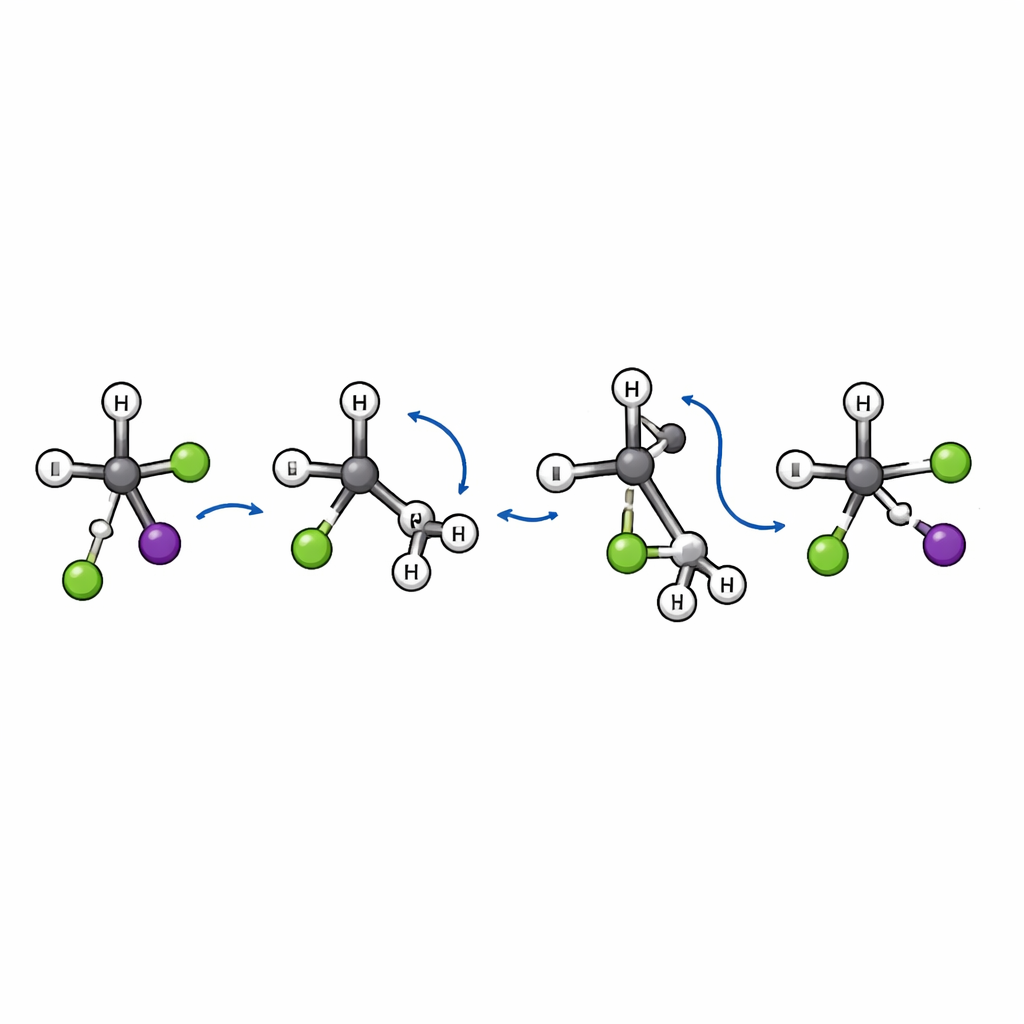
Impronte del moto di ribaltamento
Questa via di flip-over lascia chiare impronte nei modelli di scattering. Gli eventi di sostituzione che procedono attraverso la consueta inversione tendono a mandare il frammento di iodio all’indietro rispetto al cloruro in arrivo. Al contrario, le traiettorie che seguono la via di flip-over disperdono per lo più lo iodio in avanti, segno che la collisione è molto diretta e che il moto rotazionale del gruppo ingombrante gioca un ruolo chiave. Gli autori identificano anche uno stato di transizione specifico — una sorta di porta energetica — che collega reagenti e prodotti lungo questo nuovo percorso, confermando che si tratta di un meccanismo genuino e distinto piuttosto che di una minima variazione di quelli noti.
Cosa significa per la chimica
Combinando esperimenti all’avanguardia con un panorama energetico accurato appreso dalla macchina, questo studio dimostra che anche uno dei tipi di reazione più studiati nasconde ancora sorprese. La scoperta di una via di flip-over che preserva la disposizione tridimensionale degli atomi amplia i modi conosciuti in cui le reazioni di sostituzione possono controllare la forma molecolare. In termini pratici, tali intuizioni possono aiutare i chimici a prevedere meglio quando si formeranno certi prodotti, specialmente in molecole affollate dove i movimenti sottili dello scheletro carbonioso contano. Man mano che tecniche simili vengono applicate a sistemi più complessi, potrebbero emergere altri percorsi nascosti, affinando il nostro modo di pensare alla coreografia microscopica del cambiamento chimico.
Citazione: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Parole chiave: Reazioni SN2, dinamica delle reazioni, stereochimica, eliminazione vs sostituzione, imaging di collisioni molecolari