Clear Sky Science · pl
Odkrycie mechanizmu zachowania konfiguracji typu „flip‑over” w reakcji gazowej Cl− + (CH3)3CI typu SN2
Dlaczego drobne zderzenia mają znaczenie
Każdej sekundy niezliczone reakcje chemiczne kształtują otaczający nas świat — od działania leków po spalanie paliw. Wiele z tych reakcji przebiega według kilku podręcznikowych schematów, które studenci poznają na zajęciach z chemii ogólnej. Niniejszy artykuł bada bardzo znany typ reakcji — gdy jedna mała naładowana cząstka zamienia się miejscami z inną w cząsteczce organicznej — i pokazuje, że rzeczywistość bywa bardziej zaskakująca niż standardowy obraz. Obserwując zderzenia pojedynczych molekuł w fazie gazowej i szczegółowo symulując ich ruchy, autorzy odkrywają nowy sposób, w jaki atomy mogą się przearanżować — taki, którego wcześniej nie zanotowano.
Dwie rywalizujące ścieżki reakcji
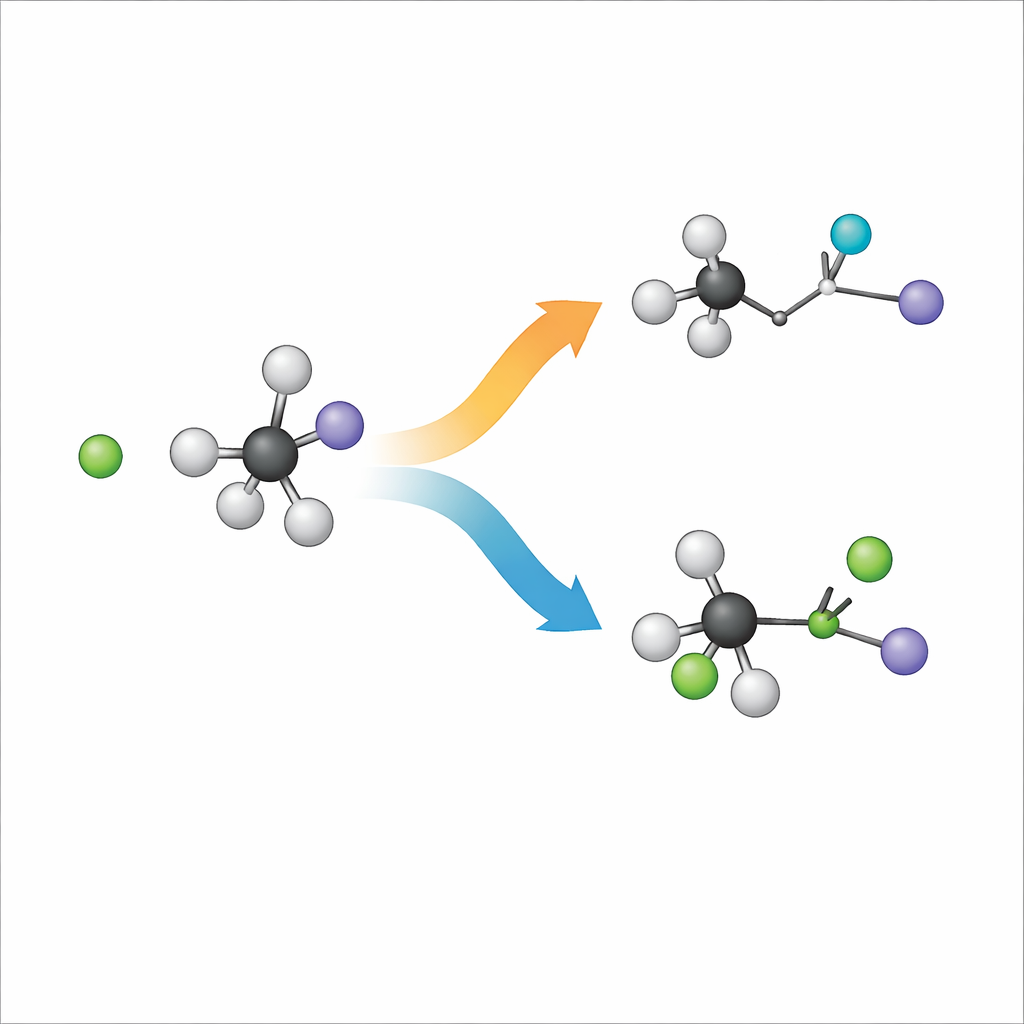
Kiedy ujemnie naładowany jon chlorkowy spotyka masywną cząsteczkę zwaną jodkiem terc‑butylu, możliwe są dwa główne przebiegi. W jednym, zwanym substytucją, chlork zastępuje jod w szkielecie węglowym. W drugim, nazywanym eliminacją, chlork odbiera atom wodoru, a szkielet węglowy przekształca się, tworząc wiązanie podwójne, podczas gdy jod odchodzi osobno. Chemicy oznaczają te drogi jako SN2 i E2, ale w istocie są to dwie różne drogi, w jakie te same składniki mogą się przearanżować. Zrozumienie, która ścieżka zwycięża i dlaczego, jest kluczowe przy projektowaniu reakcji prowadzących do pożądanego produktu w chemii syntezy.
Nagrywanie reakcji w powietrzu
Aby odkryć, co naprawdę się dzieje, badacze usuwają zamieszanie związane z rozpuszczalnikami i badają reakcję w fazie gazowej, gdzie pojedyncze jony i molekuły zderzają się w niemal próżni. Przecinają wiązkę jonów chlorkowych z wiązką jodku terc‑butylu i wykorzystują specjalistyczne urządzenie do obrazowania, które rejestruje trójwymiarowe prędkości i kierunki odłamków zawierających jod, które odlatywane są z reakcji. Równocześnie konstruują niezwykle szczegółową „mapę” sił między wszystkimi 15 atomami, używając podejścia uczenia maszynowego trenowanego na wysokopoziomowych obliczeniach kwantowych. Następnie uruchamiają miliony trajektorii symulacyjnych na tym 39‑wymiarowym krajobrazie, by śledzić, jak atomy poruszają się podczas każdej kolizji.
Eliminacja wychodzi na prowadzenie
Obrazy eksperymentalne i symulacje komputerowe zgadzają się zadziwiająco dobrze, co daje pewność, że reakcja jest wiernie uchwycona. Oba pokazują, że dominującą drogą jest eliminacja: większość zderzeń prowadzi układ szlakiem E2, zwłaszcza przy wyższej energii zderzenia. W tych zdarzeniach produkty przenoszą dużo energii wewnętrznej w postaci drgań — większość nadmiarowej energii przechodzi na drgania i skręty nowych cząsteczek, zamiast jedynie na odpychanie ich od siebie. To zachowanie odpowiada wcześniejszym badaniom pokrewnych układów i podkreśla, jak obszerny szkielet węglowy jodku terc‑butylu kieruje reakcję z dala od prostej substytucji.
Nowy rodzaj molekularnego „przewrócenia”
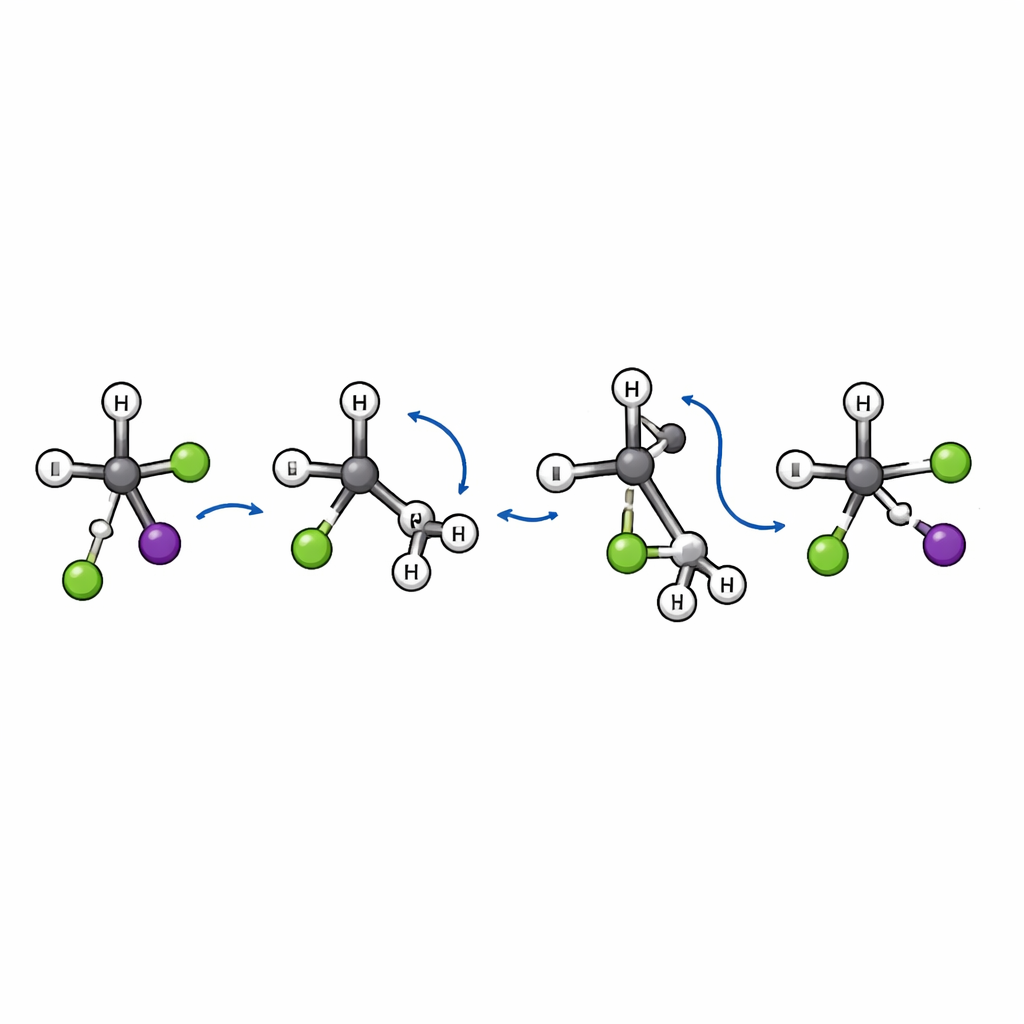
W mniejszej części zdarzeń prowadzących do substytucji zespół odkrywa coś nieoczekiwanego. Klasyczny obraz SN2 zakłada „atak od tyłu”: nadchodzący jon zbliża się od strony przeciwnej do opuszczającej grupy, a centralny atom węgla odwraca swoją geometrię, niczym parasol wywracający się na drugą stronę. Ta inwersja zmienia trójwymiarową „ręczność” cząsteczki. W tej pracy symulacje ujawniają dodatkową, odrębną drogę. W nowo odkrytym mechanizmie „flip‑over” chlork najpierw zbliża się i rozciąga wiązanie między węglem a jodem. Następnie masywna grupa terc‑butylowa przewraca się jako całość, jak przewracana strona kartki, podczas gdy chlork ostatecznie wiąże się z centralnym węglem, a jod odchodzi. Ponieważ szkielet węglowy się przewraca zamiast inwertować, ogólny układ przestrzenny wokół kluczowego atomu węgla zostaje zachowany, a nie odwrócony.
Odciski ruchu flip‑over w rozpraszaniu
Ta ścieżka flip‑over zostawia wyraźne odciski w wzorcach rozpraszania. Zdarzenia substytucji przebiegające przez zwykłą inwersję mają tendencję do wysyłania fragmentu jodu w kierunku przeciwnym do nadchodzącego chlorku. Natomiast trajektorie idące drogą flip‑over zwykle rozpraszają jod do przodu — to znak, że kolizja jest bardzo bezpośrednia i że rotacyjny ruch obfitej grupy odgrywa kluczową rolę. Autorzy identyfikują także specyficzny stan przejściowy — rodzaj energetycznej bramy — który łączy reagent i produkty wzdłuż tej nowej ścieżki, potwierdzając, że jest to prawdziwy i odrębny mechanizm, a nie drobna wariacja znanych dróg.
Co to oznacza dla chemii
Łącząc najnowocześniejsze eksperymenty z dokładnym, uczonym maszynowo krajobrazem energetycznym, badanie to pokazuje, że nawet jeden z najlepiej zbadanych typów reakcji nadal kryje niespodzianki. Odkrycie drogi flip‑over, która zachowuje trójwymiarowe rozmieszczenie atomów, poszerza znane sposoby, w jakie reakcje substytucji mogą kontrolować kształt cząsteczek. W praktycznym ujęciu takie wnioski mogą pomóc chemikom lepiej przewidywać, kiedy powstaną określone produkty, zwłaszcza w przypadkach zatłoczonych cząsteczek, gdzie subtelne ruchy szkieletu węglowego mają znaczenie. W miarę stosowania podobnych technik do bardziej złożonych układów mogą pojawić się kolejne ukryte ścieżki, doprecyzowując nasze wyobrażenie o mikroskopowym choreografia zmian chemicznych.
Cytowanie: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Słowa kluczowe: reakcje SN2, dynamika reakcji, stereochemia, eliminacja kontra substytucja, obrazowanie kolizji molekularnych