Clear Sky Science · pt
Revelando um mecanismo de retenção por virada na reação em fase gasosa Cl− + (CH3)3CI do tipo SN2
Por que pequenas colisões importam
Cada segundo, inúmeras reações químicas moldam o mundo ao nosso redor, desde o funcionamento de medicamentos até a combustão de combustíveis. Muitas dessas reações seguem alguns padrões clássicos que os estudantes aprendem na química introdutória. Este artigo examina um tipo muito familiar de reação — onde uma pequena partícula carregada troca de lugar com outra em uma molécula orgânica — e mostra que a realidade é mais surpreendente do que o quadro padrão. Ao observar moléculas individuais colidindo na fase gasosa e simular seus movimentos em detalhe, os autores descobrem uma nova forma de rearranjo atômico, até então não vista.
Dois caminhos rivais de reação
Quando um íon cloreto carregado negativamente encontra uma molécula volumosa chamada iodeto de terc-butila, dois desfechos principais são possíveis. Em um caminho, conhecido como substituição, o cloreto ocupa o lugar do iodo na estrutura de carbono. No outro, chamado eliminação, o cloreto captura um átomo de hidrogênio, e o esqueleto de carbono se reorganiza para formar uma ligação dupla enquanto o iodo sai separadamente. Químicos rotulam essas rotas como SN2 e E2, mas na essência são duas maneiras diferentes de os mesmos ingredientes se rearranjarem. Entender qual caminho prevalece, e por quê, é crucial para projetar reações que produzam o produto desejado na síntese química.
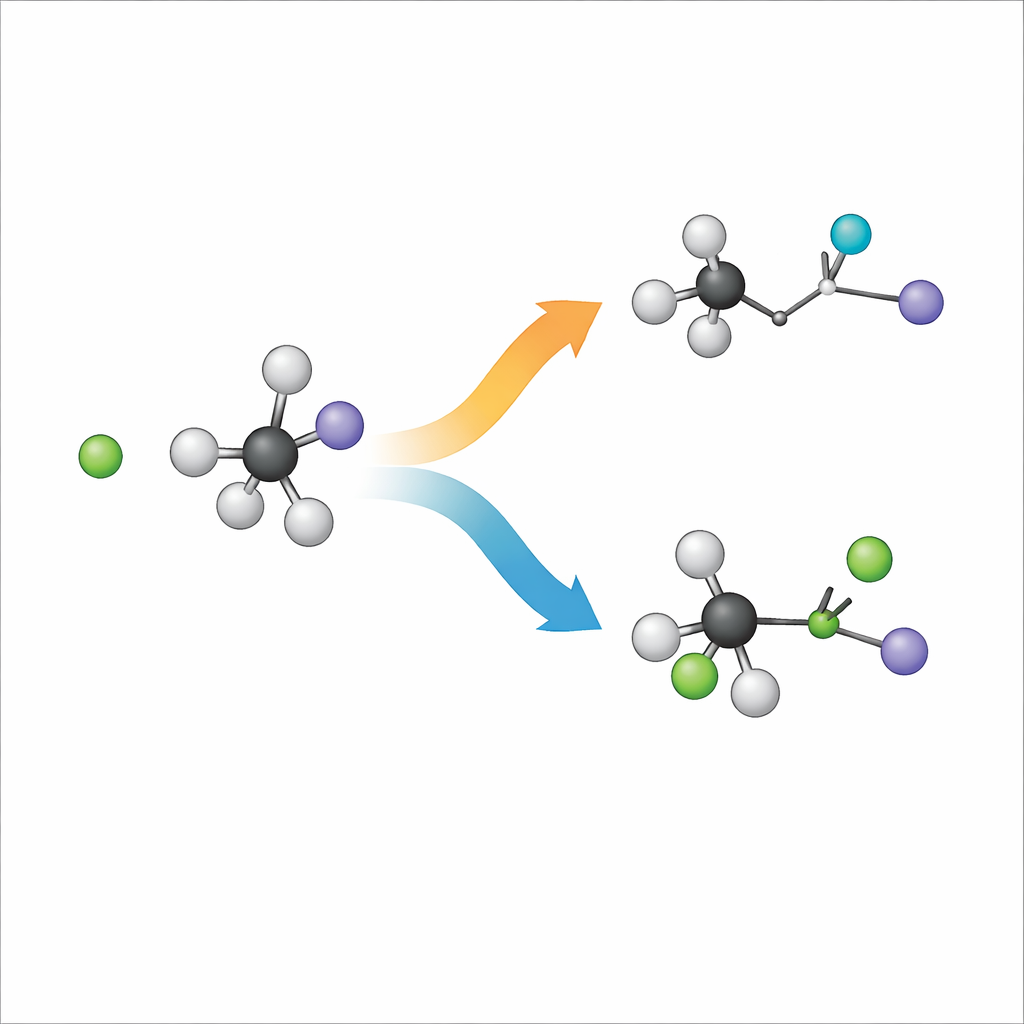
Filmando reações no ar
Para descobrir o que realmente acontece, os pesquisadores eliminam a interferência dos solventes e estudam a reação em fase gasosa, onde íons e moléculas individuais colidem em quase-vácuo. Eles cruzam um feixe de íons cloreto com um feixe de iodeto de terc-butila e usam um sistema de imagem especializado para registrar as velocidades tridimensionais e direções dos fragmentos contendo iodo que voam para fora. Ao mesmo tempo, constroem um “mapa” extremamente detalhado das forças entre todos os 15 átomos usando uma abordagem de aprendizado de máquina treinada com cálculos quânticos de alto nível. Em seguida, lançam milhões de trajetórias simuladas nessa paisagem de 39 dimensões para seguir como os átomos se movem durante cada colisão.
A eliminação sai na frente
As imagens experimentais e as simulações computacionais coincidem notavelmente bem, dando confiança de que a reação está sendo capturada com precisão. Ambas mostram que o caminho de eliminação domina: a maioria das colisões segue a rota E2, especialmente conforme aumenta a energia de colisão. Nesses eventos, os produtos carregam muita energia vibracional interna — a maior parte da energia extra acaba tremendo e torcendo as novas moléculas em vez de simplesmente lançá-las para longe. Esse comportamento coincide com trabalhos anteriores em sistemas relacionados e destaca como o esqueleto de carbono volumoso do iodeto de terc-butila direciona a reação para longe da substituição simples.
Um novo tipo de virada molecular
Dentro da fração menor de eventos de substituição, a equipe encontra algo inesperado. O quadro clássico de SN2 envolve um “ataque por trás”: o íon que chega aproxima-se por trás do grupo que sai e o carbono central inverte sua geometria, como um guarda-chuva virando do avesso. Essa inversão altera a quiralidade tridimensional da molécula. Aqui, as simulações revelam uma rota adicional e distinta. Nesse mecanismo recém-descoberto de “virada” (flip-over), o cloreto primeiro se aproxima e estica a ligação entre o carbono e o iodo. O grupo terc-butila volumoso então vira como uma unidade, como se uma página fosse folheada, enquanto o cloreto finalmente se liga ao carbono central e o iodo parte. Como a estrutura de carbono vira em bloco em vez de inverter, o arranjo espacial ao redor do átomo de carbono chave é mantido em vez de ser invertido.
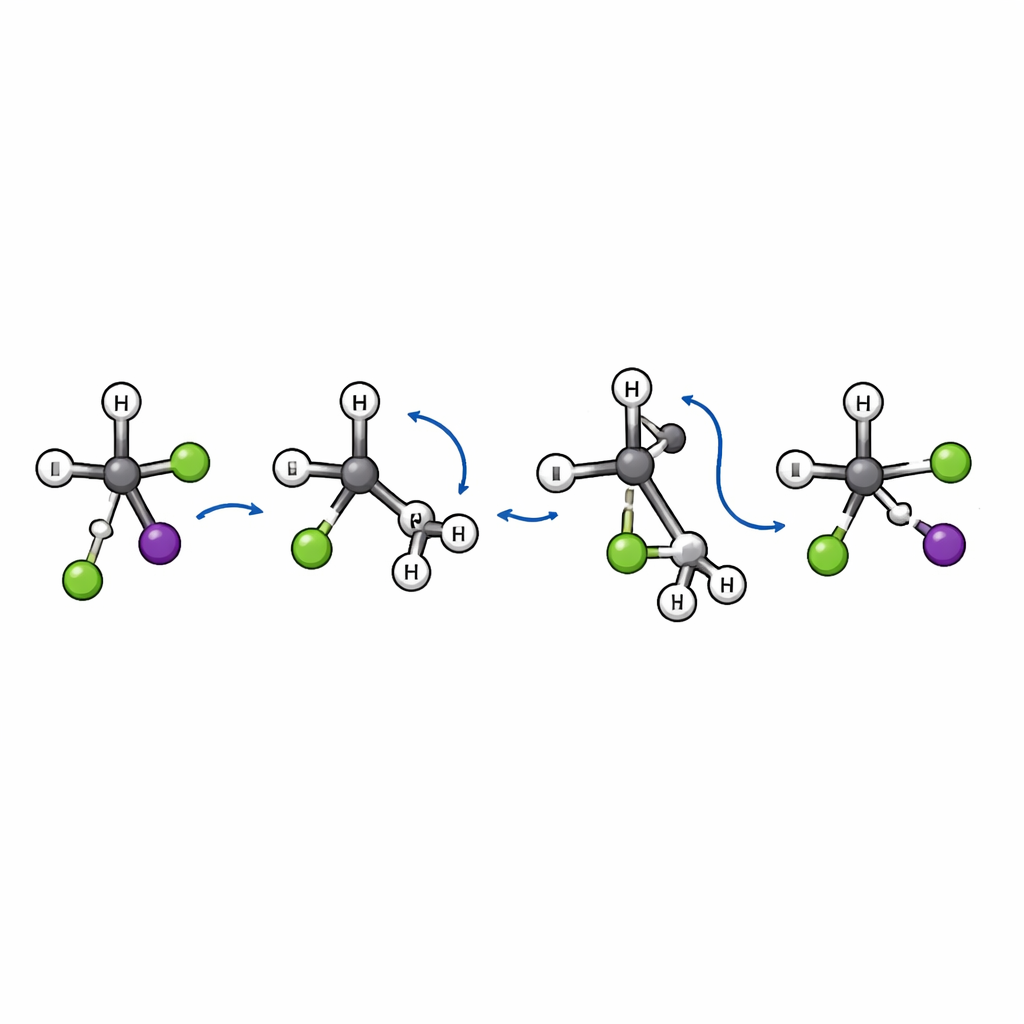
Assinaturas do movimento de virada
Essa via de virada deixa impressões claras nos padrões de espalhamento. Os eventos de substituição que seguem a inversão usual tendem a enviar o fragmento de iodo para trás em relação ao cloreto incidente. Em contraste, trajetórias que seguem a rota de virada espalham principalmente o iodo para frente, um sinal de que a colisão é muito direta e de que o movimento rotacional do grupo volumoso desempenha um papel chave. Os autores também identificam um estado de transição específico — uma espécie de portal energético — que conecta reagentes e produtos ao longo desse novo caminho, confirmando que se trata de um mecanismo genuíno e distinto, e não de uma variação menor de mecanismos conhecidos.
O que isso significa para a química
Ao combinar experimentos de ponta com uma paisagem energética precisa aprendida por máquina, este estudo mostra que mesmo um dos tipos de reação mais estudados ainda pode esconder surpresas. A descoberta de uma rota de virada que preserva o arranjo tridimensional dos átomos amplia as maneiras conhecidas pelas quais reações de substituição podem controlar a forma molecular. Em termos práticos, tais insights podem ajudar químicos a prever melhor quando certos produtos irão se formar, especialmente em moléculas congestionadas onde movimentos sutis do esqueleto de carbono importam. À medida que técnicas semelhantes são aplicadas a sistemas mais complexos, outros caminhos ocultos podem emergir, refinando nossa visão sobre a coreografia microscópica da mudança química.
Citação: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Palavras-chave: Reações SN2, dinâmica de reação, estereoquímica, eliminação vs substituição, imagem de colisão molecular