Clear Sky Science · de
Aufdeckung eines Umklapp-Retention-Mechanismus in der gasphasen Cl− + (CH3)3CI SN2-Reaktion
Warum winzige Kollisionen wichtig sind
Sekündlich formen unzählige chemische Reaktionen die Welt um uns herum – von der Wirkungsweise von Medikamenten bis zum Verbrennen von Brennstoffen. Viele dieser Reaktionen folgen einer Handvoll Lehrbuchmuster, die man in der Einführung zur Chemie lernt. Dieser Artikel betrachtet einen sehr vertrauten Reaktionstyp – bei dem ein kleines geladenes Teilchen in einem organischen Molekül den Platz mit einem anderen tauscht – und zeigt, dass die Wirklichkeit überraschender ist als das Standardbild. Durch das Beobachten einzelner Molekülkollisionen in der Gasphase und das detaillierte Simulieren ihrer Bewegung entdecken die Autoren eine neue Art, wie Atome sich umordnen können, die zuvor nicht gesehen wurde.
Zwei konkurrierende Reaktionswege
Wenn ein negativ geladenes Chloridion auf ein sperriges Molekül namens tert-Butyljodid trifft, sind zwei Hauptergebnisse möglich. Auf dem einen Weg, der als Substitution bekannt ist, ersetzt Chlor das Jod im Kohlenstoffgerüst. Auf dem anderen, der Elimination genannt wird, greift Chlor ein Wasserstoffatom und das Kohlenstoffgerüst formt sich um, um eine Doppelbindung zu bilden, während Jod separat abgeht. Chemiker bezeichnen diese Wege als SN2 und E2, doch im Kern sind es zwei unterschiedliche Arten, wie dieselben Zutaten sich umordnen können. Zu verstehen, welcher Weg sich durchsetzt und warum, ist entscheidend für das Entwerfen von Reaktionen, die in der Synthese das gewünschte Produkt liefern.
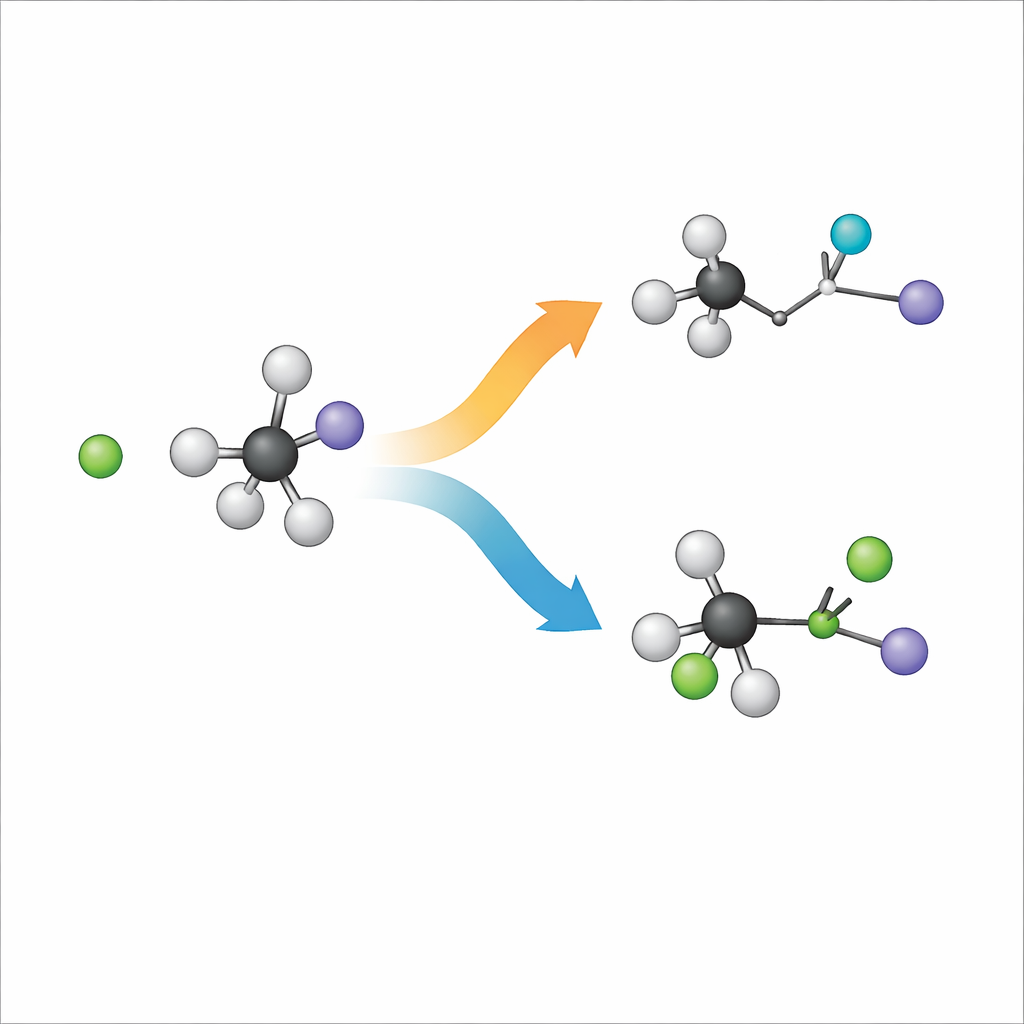
Reaktionen in der Luft filmen
Um herauszufinden, was wirklich passiert, entfernen die Forscher die Störeinflüsse von Lösungsmitteln und untersuchen die Reaktion in der Gasphase, wo einzelne Ionen und Moleküle in nahezu vakuumähnlichen Bedingungen kollidieren. Sie kreuzen einen Strahl von Chloridionen mit einem Strahl von tert-Butyljodid und verwenden eine spezialisierte Bildgebung, um die dreidimensionalen Geschwindigkeiten und Richtungen der jodhaltigen Fragmente aufzuzeichnen, die davonfliegen. Gleichzeitig erstellen sie eine äußerst detaillierte "Landkarte" der Kräfte zwischen allen 15 Atomen mithilfe eines maschinellen Lernverfahrens, das auf hochrangigen Quantenberechnungen trainiert wurde. Anschließend starten sie Millionen simulierten Trajektorien auf dieser 39-dimensionalen Landschaft, um zu verfolgen, wie sich die Atome bei jeder Kollision bewegen.
Elimination übernimmt die Führung
Die experimentellen Aufnahmen und Computersimulationen stimmen bemerkenswert gut überein, was Vertrauen in die genaue Erfassung der Reaktion gibt. Beide zeigen, dass der Eliminationsweg dominiert: Die meisten Kollisionen führen das System auf den E2-Pfad, besonders wenn die Kollisionsenergie zunimmt. Bei diesen Ereignissen tragen die Produkte viel innere Schwingungsenergie – der Großteil der zusätzlichen Energie geht in das Schwingen und Verdrehen der neuen Moleküle, statt sie einfach auseinanderzutreiben. Dieses Verhalten stimmt mit früheren Arbeiten an verwandten Systemen überein und unterstreicht, wie das sperrige Kohlenstoffgerüst des tert-Butyljodids die Reaktion von einfacher Substitution weglenkt.
Eine neue Art von molekularem Umschlag
Innerhalb des kleineren Anteils an Substitutionsereignissen finden die Forschenden etwas Unerwartetes. Das klassische SN2-Bild beinhaltet einen "Rückseitenangriff": das eintreffende Ion nähert sich von der gegenüberliegenden Seite der abgehenden Gruppe und das zentrale Kohlenstoffatom invertiert seine Geometrie, ähnlich einem Regenschirm, der sich umstülpt. Diese Inversion verändert die dreidimensionale Händigkeit des Moleküls. Hier zeigen die Simulationen einen zusätzlichen, klar unterscheidbaren Weg. In diesem neu entdeckten "Flip-over"-Mechanismus nähert sich das Chlorid zunächst und dehnt die Bindung zwischen Kohlenstoff und Jod. Die sperrige tert-Butyl-Gruppe klappt dann als Einheit um, wie eine umgeschlagene Seite, während Chlorid schließlich an das zentrale Kohlenstoffatom bindet und Jod abgeht. Weil das Kohlenstoffgerüst umklappt statt invertiert zu werden, bleibt die Gesamtanordnung um das Schlüsselkohlenstoffatom erhalten statt umgekehrt.
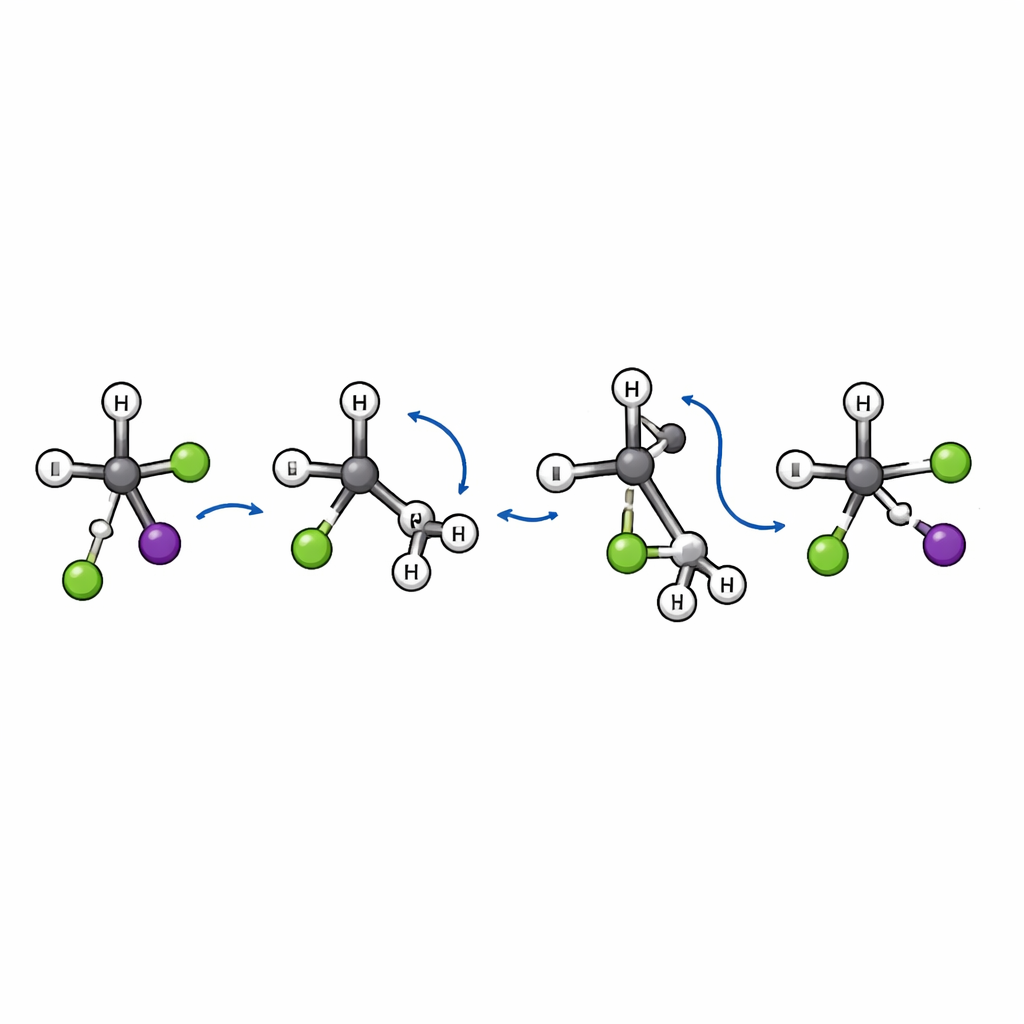
Signaturen der Flip-over-Bewegung
Dieser Flip-over-Pfad hinterlässt deutliche Fingerabdrücke in den Streumustern. Substitutionsereignisse, die über die übliche Inversion verlaufen, tendieren dazu, das Jodfragment rückwärts relativ zum einfallenden Chlorid zu schicken. Im Gegensatz dazu streuen Trajektorien, die dem Flip-over-Weg folgen, das Jod überwiegend vorwärts – ein Zeichen dafür, dass die Kollision sehr direkt ist und die Rotationsbewegung der sperrigen Gruppe eine Schlüsselrolle spielt. Die Autoren identifizieren zudem einen spezifischen Übergangszustand – eine Art energetisches Tor – das Reaktanten und Produkte entlang dieses neuen Pfads verbindet und bestätigt, dass es sich um einen echten und unterscheidbaren Mechanismus handelt und nicht bloß um eine marginale Variante bekannter Wege.
Was das für die Chemie bedeutet
Durch die Kombination modernster Experimente mit einer genauen, maschinell gelernten Energielandschaft zeigt diese Studie, dass selbst einer der am intensivsten untersuchten Reaktionstypen noch Überraschungen bereithält. Die Entdeckung eines Flip-over-Wegs, der die dreidimensionale Anordnung der Atome bewahrt, erweitert die bekannten Möglichkeiten, wie Substitutionsreaktionen die Molekülgestalt steuern können. Praktisch können solche Einsichten Chemikern helfen, besser vorherzusagen, wann bestimmte Produkte entstehen, insbesondere in überfüllten Molekülen, bei denen subtile Bewegungen des Kohlenstoffgerüsts wichtig sind. Wenn ähnliche Techniken auf komplexere Systeme angewandt werden, könnten weitere verborgene Pfade auftauchen und unser Verständnis der mikroskopischen Choreografie chemischer Veränderungen verfeinern.
Zitation: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Schlüsselwörter: SN2-Reaktionen, Reaktionsdynamik, Stereochemie, Elimination vs. Substitution, molekulare Kollisionsbildgebung