Clear Sky Science · nl
Onthulling van een flip-over retentiemechanisme in de gasfase Cl− + (CH3)3CI SN2-reactie
Waarom kleine botsingen ertoe doen
Elke seconde bepalen talloze chemische reacties de wereld om ons heen, van hoe medicijnen werken tot hoe brandstoffen verbranden. Veel van deze reacties volgen een handvol tekstboekpatronen die studenten in de inleidende scheikunde leren. Dit artikel behandelt een zeer bekend type reactie—waarbij een klein geladen deeltje van plaats wisselt met een ander in een organisch molecuul—en laat zien dat de werkelijkheid verrassender is dan het standaardbeeld. Door individuele moleculen in de gasfase te observeren en hun bewegingen in detail te simuleren, ontdekken de auteurs een nieuwe manier waarop atomen zich kunnen herschikken, een manier die eerder niet is waargenomen.
Twee concurrerende reactieroutes
Wanneer een negatief geladen chloride-ion een volumineus molecuul genaamd tert-butyljodide ontmoet, zijn twee hoofduitkomsten mogelijk. In de ene route, bekend als substitutie, neemt chloride de plaats van jodium in op het koolstofskelet. In de andere, eliminatie genoemd, pakt chloride een waterstofatoom in plaats daarvan, en hervormt het koolstofskelet zich om een dubbele binding te vormen terwijl jodium afzonderlijk vertrekt. Chemici labelen deze routes als SN2 en E2, maar in wezen zijn het twee verschillende manieren waarop dezelfde ingrediënten zich kunnen herschikken. Begrijpen welke route wint, en waarom, is cruciaal voor het ontwerpen van reacties die het gewenste product opleveren in de synthetische chemie.
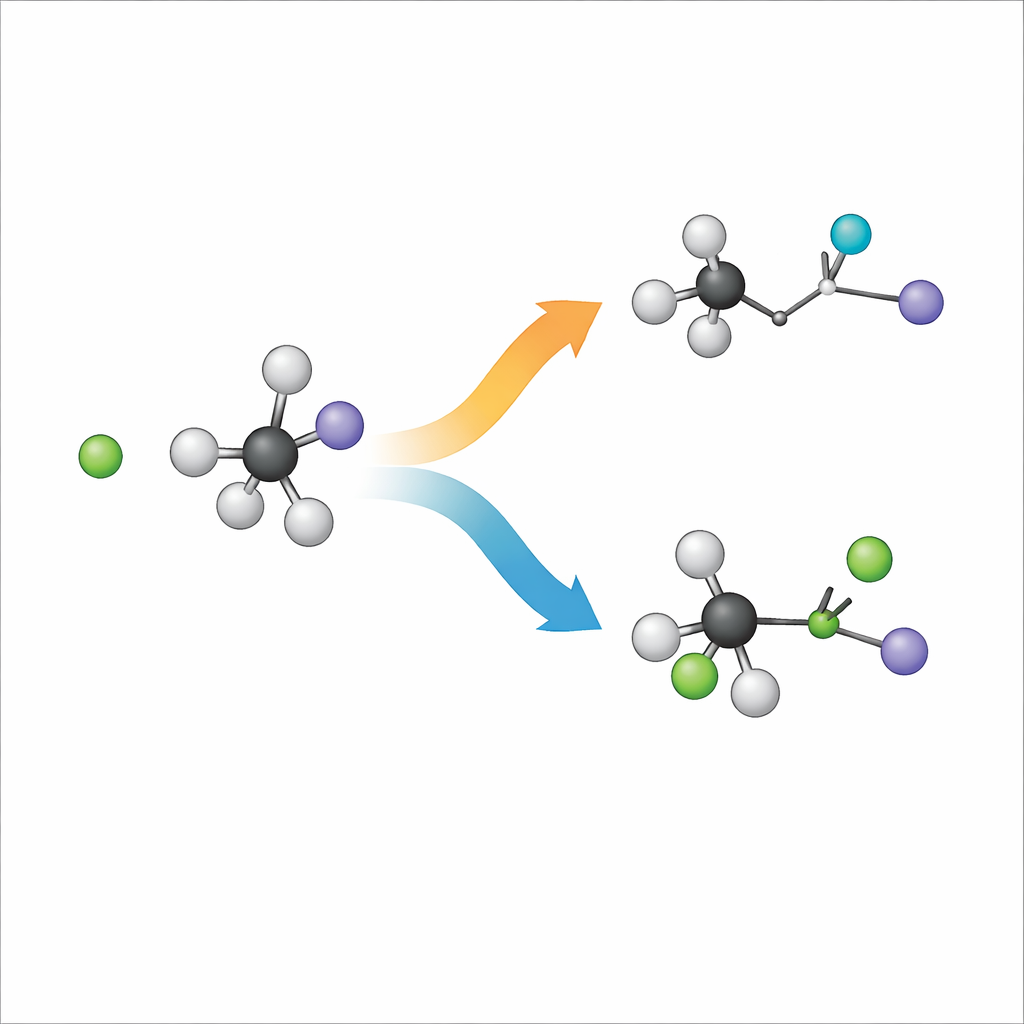
Reacties filmen in de lucht
Om te ontdekken wat er echt gebeurt, halen de onderzoekers de ruis van oplosmiddelen weg en bestuderen ze de reactie in de gasfase, waar individuele ionen en moleculen in een bijna-vacuüm botsen. Ze kruisen een bundel chloride-ionen met een bundel tert-butyljodide en gebruiken een gespecialiseerde beeldopstelling om de driedimensionale snelheden en richtingen van de jodiumhoudende fragmenten die wegvliegen vast te leggen. Tegelijk bouwen ze een uiterst gedetailleerde "kaart" van de krachten tussen alle 15 atomen met een machine-learningbenadering die getraind is op hoogstaande kwantumcalculaties. Vervolgens starten ze miljoenen gesimuleerde trajecten op dit 39-dimensionale landschap om te volgen hoe de atomen tijdens elke botsing bewegen.
Eliminatie neemt de leiding
De experimentele beelden en computersimulaties komen opmerkelijk goed overeen, wat vertrouwen geeft dat de reactie accuraat wordt vastgelegd. Beide laten zien dat de eliminatieroute domineert: de meeste botsingen leiden het systeem naar de E2-route, vooral naarmate de botsingsenergie toeneemt. Bij deze gebeurtenissen dragen de producten veel interne vibratie-energie—het merendeel van de extra energie gaat zitten in het laten trillen en draaien van de nieuwe moleculen in plaats van ze simpelweg uit elkaar te stuwen. Dit gedrag komt overeen met eerder werk aan verwante systemen en benadrukt hoe het volumineuze koolstofskelet van tert-butyljodide de reactie wegstuurt van eenvoudige substitutie.
Een nieuw soort moleculaire flip
Binnen het kleinere aandeel substitutiegebeurtenissen vindt het team iets onverwachts. Het klassieke SN2-beeld omvat een "aanval van de achterkant": het binnenkomende ion nadert achter de vertrekkende groep en de centrale koolstof keert zijn geometrie om, als een paraplu die binnenstebuiten gaat. Die inversie verandert de driedimensionale handigheid van het molecuul. Hier tonen de simulaties een aanvullende, onderscheidende route. In dit nieuw ontdekte "flip-over"-mechanisme nadert chloride eerst en rekt de binding tussen koolstof en jodium uit. De volumineuze tert-butylgroep kantelt daarna als een geheel, als een omgeslagen pagina, terwijl chloride uiteindelijk aan de centrale koolstof bindt en jodium vertrekt. Omdat het koolstofskelet kantelt in plaats van inverseert, wordt de algehele ruimtelijke ordening rond het sleutel-koolstofatoom behouden in plaats van omgekeerd.
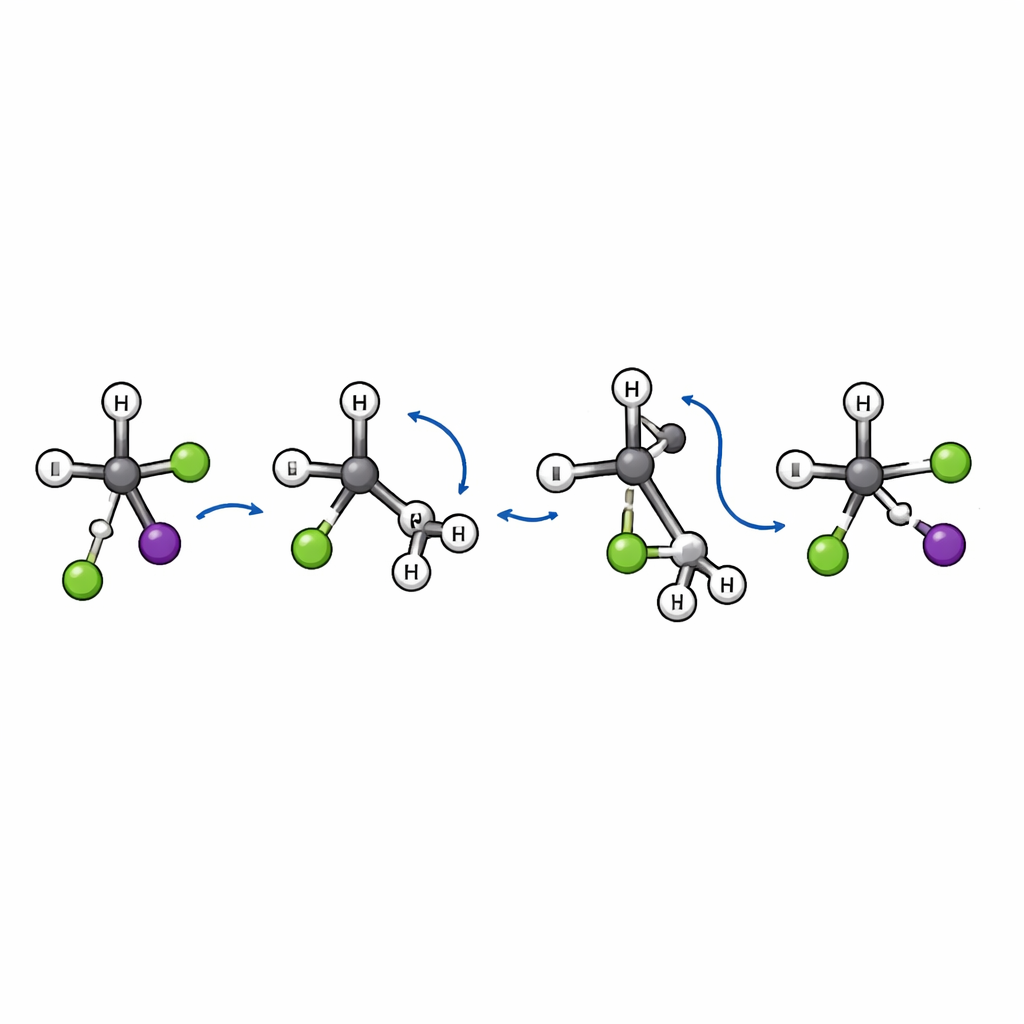
Kenmerken van de flip-over beweging
Deze flip-over-route laat duidelijke vingerafdrukken achter in de verstrooiingspatronen. Substitutiegebeurtenissen die via de gebruikelijke inversie verlopen, sturen het jodiumfragment vaak achterwaarts ten opzichte van het binnenkomende chloride. Ter vergelijking: trajecten die de flip-overroute volgen verstrooien jodium meestal voorwaarts, een teken dat de botsing zeer direct is en dat de roterende beweging van de volumineuze groep een sleutelrol speelt. De auteurs identificeren ook een specifieke overgangstoestand—een soort energetische poort—die reagentia en producten verbindt langs dit nieuwe pad, wat bevestigt dat het een echte en afzonderlijke mechanisme is in plaats van een kleine variatie op bekende routes.
Wat dit betekent voor de chemie
Door grensverleggende experimenten te combineren met een nauwkeurig, door machine geleerd energielandschap, toont deze studie aan dat zelfs een van de meest bestudeerde reactietypen nog verrassingen kan herbergen. De ontdekking van een flip-overroute die de driedimensionale ordening van atomen behoudt, vergroot de bekende manieren waarop substitutiereacties de moleculaire vorm kunnen beheersen. In praktische zin kunnen dergelijke inzichten chemici helpen beter te voorspellen wanneer bepaalde producten zullen ontstaan, vooral in drukbezette moleculen waar subtiele bewegingen van het koolstofskelet ertoe doen. Naarmate vergelijkbare technieken op complexere systemen worden toegepast, kunnen andere verborgen paden aan het licht komen en onze opvatting over de microscopische choreografie van chemische veranderingen verfijnen.
Bronvermelding: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Trefwoorden: SN2-reacties, reactiedynamica, stereochemie, eliminatie versus substitutie, moleculaire botsingsbeeldvorming