Clear Sky Science · es
Revelando un mecanismo de retención por volteo en la reacción SN2 en fase gaseosa Cl− + (CH3)3CI
Por qué importan las colisiones diminutas
Cada segundo, innumerables reacciones químicas conforman el mundo que nos rodea, desde el funcionamiento de los medicamentos hasta la combustión de los combustibles. Muchas de estas reacciones siguen un puñado de patrones de libro de texto que los estudiantes aprenden en química introductoria. Este artículo toma un tipo de reacción muy familiar —en la que una pequeña partícula cargada intercambia su lugar con otra en una molécula orgánica— y muestra que la realidad es más sorprendente que la imagen estándar. Al observar colisionar moléculas individuales en fase gaseosa y simular sus movimientos con detalle, los autores descubren una nueva forma en que los átomos pueden reorganizarse, una que no se había visto antes.
Dos rutas reactivas rivales
Cuando un ion cloruro con carga negativa encuentra una molécula voluminosa llamada yoduro de terc-butilo, son posibles dos resultados principales. En una ruta, conocida como sustitución, el cloruro ocupa el lugar del yodo en la estructura de carbono. En la otra, llamada eliminación, el cloruro captura un átomo de hidrógeno en su lugar y el esqueleto de carbono se reorganiza para formar un doble enlace mientras el yodo sale por separado. Los químicos etiquetan estas rutas como SN2 y E2, pero en el fondo son dos maneras diferentes en las que los mismos ingredientes pueden reorganizarse. Comprender qué ruta gana y por qué es crucial para diseñar reacciones que produzcan el producto deseado en química sintética.
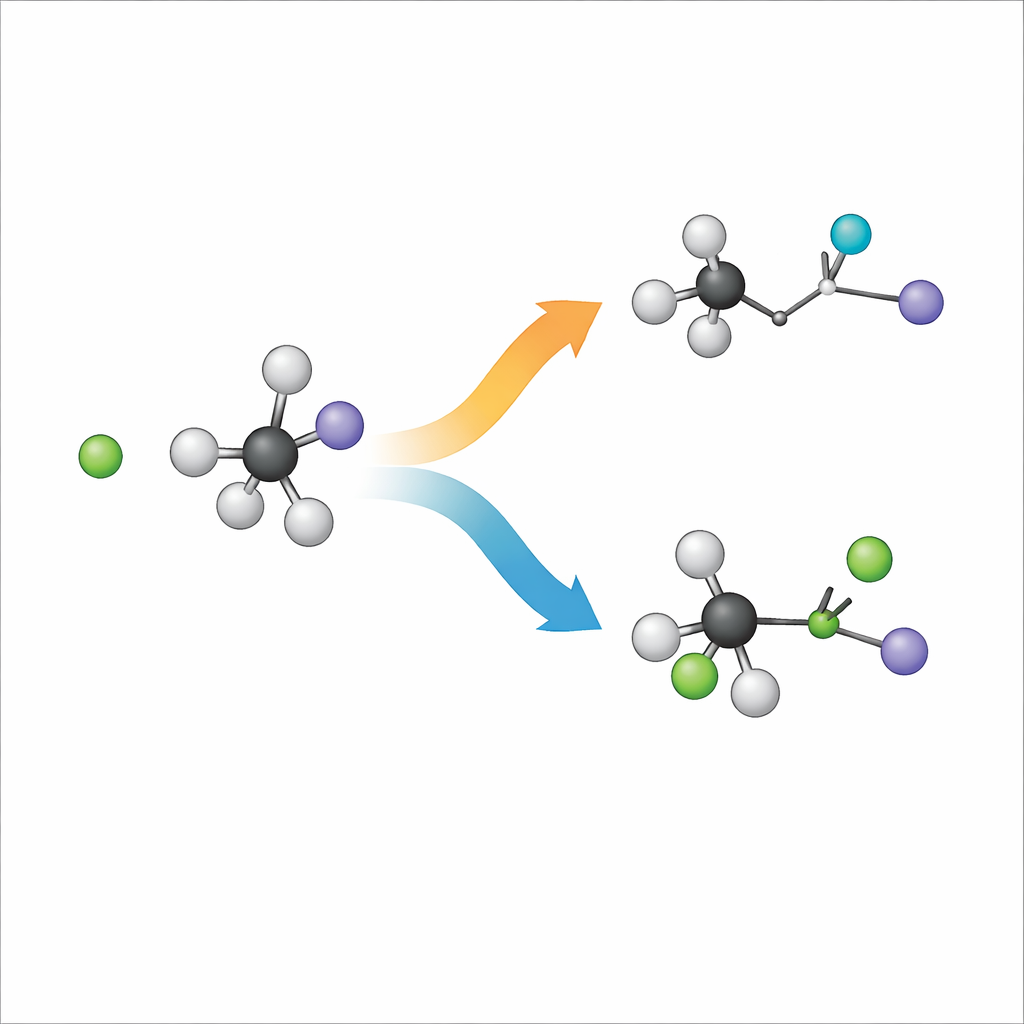
Filmar reacciones en pleno vuelo
Para descubrir qué ocurre realmente, los investigadores eliminan el ruido de los disolventes y estudian la reacción en fase gaseosa, donde iones y moléculas individuales colisionan en un casi vacío. Cruzan un haz de iones cloruro con un haz de yoduro de terc-butilo y usan un montaje de imagen especializado para registrar las velocidades tridimensionales y las direcciones de los fragmentos que contienen yodo que salen volando. Al mismo tiempo, construyen un "mapa" extremadamente detallado de las fuerzas entre los 15 átomos usando un enfoque de aprendizaje automático entrenado con cálculos cuánticos de alto nivel. Luego lanzan millones de trayectorias simuladas en este paisaje de 39 dimensiones para seguir cómo se mueven los átomos durante cada colisión.
La eliminación toma la delantera
Las imágenes experimentales y las simulaciones por ordenador coinciden de forma notable, lo que aporta confianza en que la reacción se está capturando con precisión. Ambas muestran que la ruta de eliminación domina: la mayoría de las colisiones llevan el sistema por la vía E2, especialmente a medida que aumenta la energía de colisión. En estos eventos, los productos portan mucha energía vibracional interna: la mayor parte de la energía extra termina agitando y torsionando las nuevas moléculas en lugar de simplemente separarlas. Este comportamiento coincide con trabajos previos en sistemas relacionados y subraya cómo el armazón carbonado voluminoso del yoduro de terc-butilo desvía la reacción de una simple sustitución.
Un nuevo tipo de volteo molecular
Dentro de la fracción menor de eventos de sustitución, el equipo encuentra algo inesperado. La imagen clásica de SN2 implica un "ataque por la parte trasera": el ion entrante se aproxima por detrás del grupo saliente y el carbono central invierte su geometría, como un paraguas que se da la vuelta. Esa inversión cambia la quiralidad de la molécula. Aquí, las simulaciones revelan una ruta adicional y distinta. En este mecanismo recién descubierto de "volteo", el cloruro primero se aproxima y estira el enlace entre el carbono y el yodo. El grupo terc-butilo voluminoso luego gira como una unidad, semejante a pasar la página, mientras el cloruro finalmente se enlaza al carbono central y el yodo se va. Debido a que el armazón carbonado se gira en bloque en vez de invertir, la disposición espacial alrededor del carbono clave se conserva en lugar de invertirse.
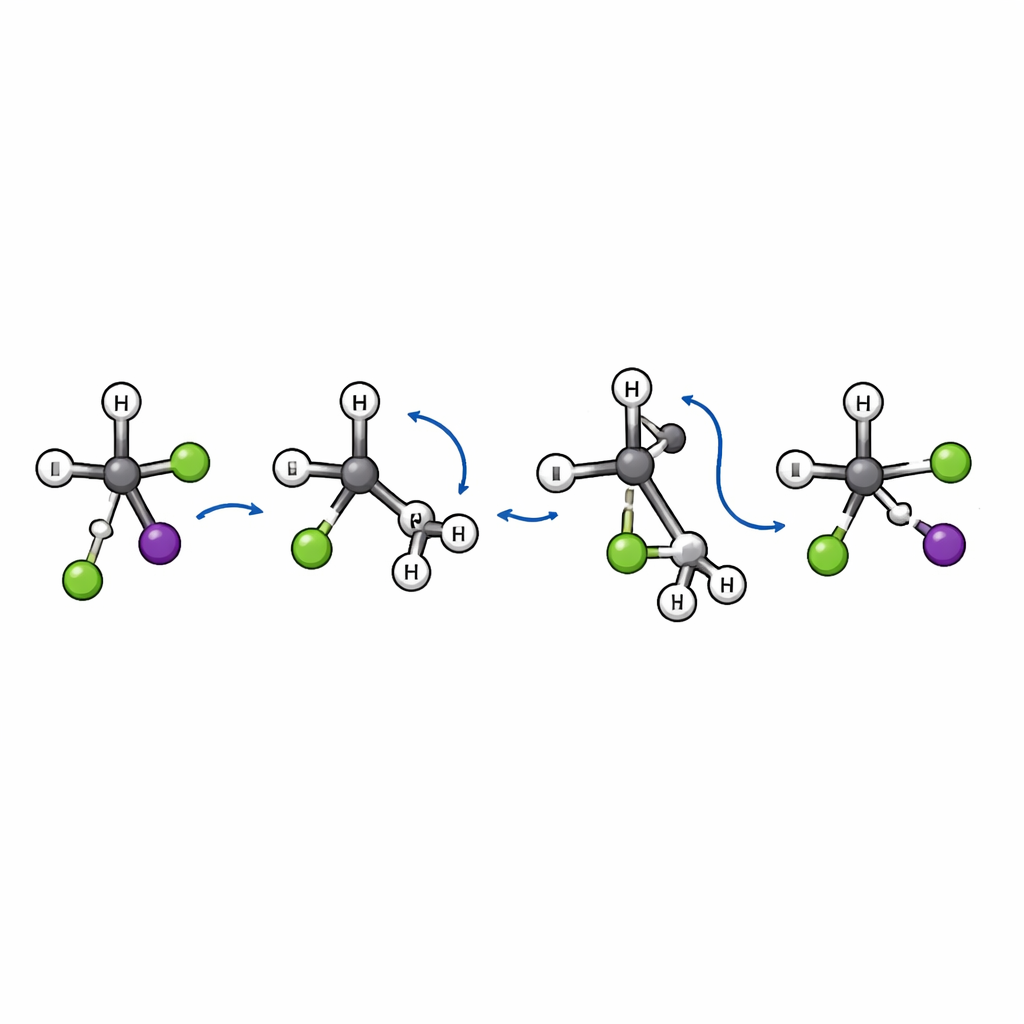
Señales del movimiento de volteo
Esta vía de volteo deja huellas claras en los patrones de dispersión. Los eventos de sustitución que transcurren mediante la inversión habitual tienden a enviar el fragmento de yodo hacia atrás con respecto al cloruro entrante. En cambio, las trayectorias que siguen la ruta de volteo dispersan mayormente el yodo hacia adelante, señal de que la colisión es muy directa y de que el movimiento rotacional del grupo voluminoso juega un papel clave. Los autores también identifican un estado de transición específico —una especie de puerta energética— que conecta reactivos y productos a lo largo de esta nueva vía, confirmando que es un mecanismo genuino y distinto y no una variación menor de los ya conocidos.
Qué significa esto para la química
Al combinar experimentos de vanguardia con un paisaje energético preciso aprendido por máquina, este estudio demuestra que incluso uno de los tipos de reacción más estudiados aún oculta sorpresas. El descubrimiento de una ruta de volteo que preserva la disposición tridimensional de los átomos amplía las formas conocidas en que las reacciones de sustitución pueden controlar la forma molecular. En términos prácticos, tales hallazgos pueden ayudar a los químicos a predecir mejor cuándo se formarán ciertos productos, especialmente en moléculas congestionadas donde los sutiles movimientos del armazón carbonado importan. A medida que se apliquen técnicas similares a sistemas más complejos, podrían surgir otras vías ocultas, afinando nuestra comprensión de la coreografía microscópica del cambio químico.
Cita: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Palabras clave: reacciones SN2, dinámica de reacciones, estereoquímica, eliminación frente a sustitución, imagen de colisiones moleculares