Clear Sky Science · fr
Révélation d’un mécanisme de rétention par basculement dans la réaction SN2 en phase gazeuse Cl− + (CH3)3CI
Pourquoi de petites collisions comptent
Chaque seconde, d’innombrables réactions chimiques façonnent le monde qui nous entoure, de l’action des médicaments à la combustion des carburants. Beaucoup de ces réactions suivent quelques schémas de manuel que les étudiants apprennent en chimie introductive. Cet article prend un type de réaction très familier — où une petite particule chargée échange sa place avec une autre dans une molécule organique — et montre que la réalité est plus surprenante que l’image standard. En observant des collisions entre molécules isolées en phase gazeuse et en simulant leurs mouvements en détail, les auteurs découvrent une nouvelle façon dont les atomes peuvent se réarranger, qui n’avait pas été observée auparavant.
Deux voies réactionnelles rivales
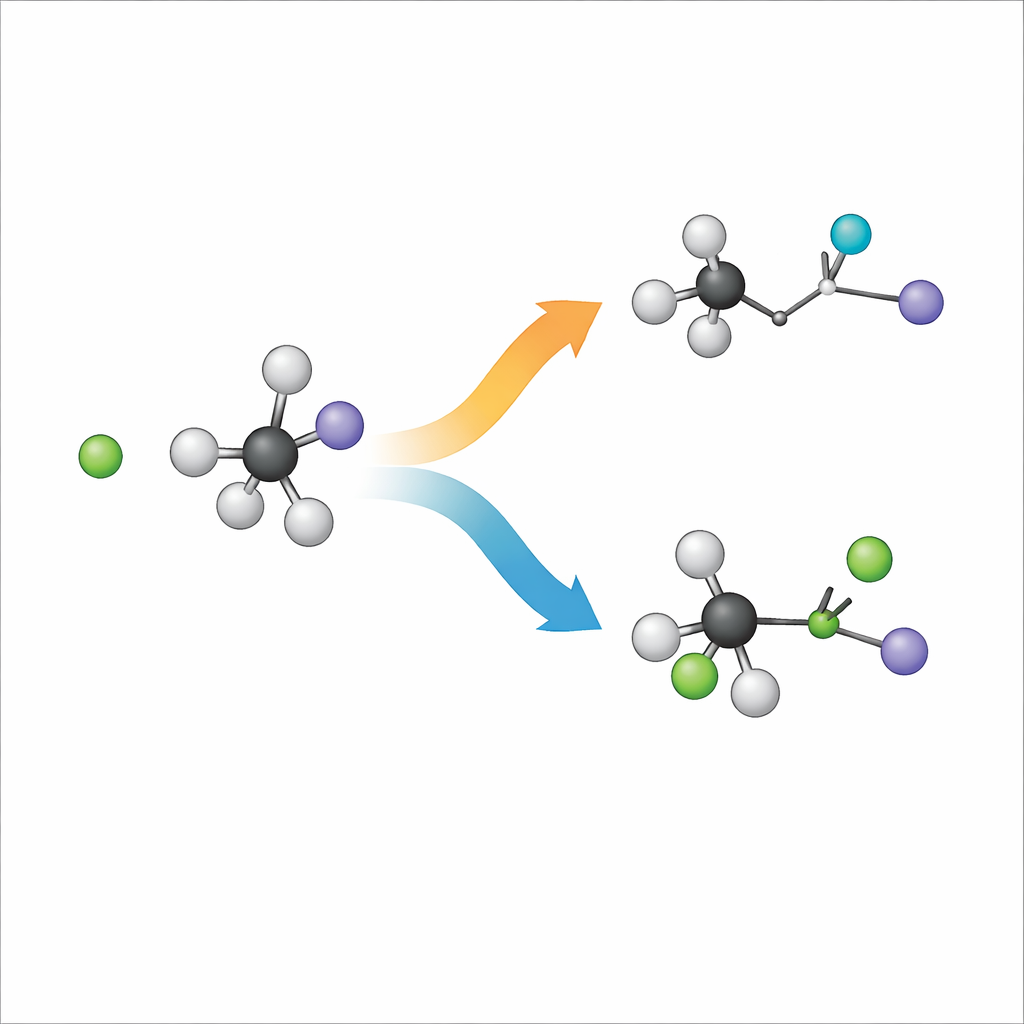
Lorsque l’anion chlorure rencontre une molécule volumineuse appelée iodure de tert-butyle, deux issues principales sont possibles. Dans une voie, dite substitution, le chlorure prend la place de l’iode sur le squelette carboné. Dans l’autre, appelée élimination, le chlorure arrache plutôt un atome d’hydrogène, et le squelette carboné se réorganise pour former une double liaison pendant que l’iode part séparément. Les chimistes désignent ces routes SN2 et E2, mais fondamentalement ce sont deux manières différentes pour les mêmes ingrédients de se réarranger. Comprendre quelle voie l’emporte, et pourquoi, est crucial pour concevoir des réactions donnant le produit désiré en synthèse.
Filmer les réactions en plein vol
Pour découvrir ce qui se passe réellement, les chercheurs éliminent le bruit des solvants et étudient la réaction en phase gazeuse, où des ions et molécules isolés entrent en collision dans un quasi-vide. Ils croisent un faisceau d’anions chlorure avec un faisceau d’iodure de tert-butyle et utilisent un dispositif d’imagerie spécialisé pour enregistrer les vitesses tridimensionnelles et les directions des fragments contenant l’iode qui s’échappent. Parallèlement, ils construisent une « carte » extrêmement détaillée des forces entre les 15 atomes grâce à une approche d’apprentissage automatique entraînée sur des calculs quantiques de haut niveau. Ils lancent ensuite des millions de trajectoires simulées sur ce paysage à 39 dimensions pour suivre le mouvement des atomes au cours de chaque collision.
L’élimination prend l’avantage
Les images expérimentales et les simulations numériques concordent remarquablement bien, ce qui donne confiance dans la bonne capture de la réaction. Les deux montrent que la voie d’élimination domine : la plupart des collisions poussent le système le long de la route E2, en particulier lorsque l’énergie de collision augmente. Dans ces événements, les produits transportent beaucoup d’énergie vibrationnelle interne — la majeure partie de l’énergie excédentaire finit par faire vibrer et tordre les nouvelles molécules plutôt que de simplement les propulser l’une par rapport à l’autre. Ce comportement correspond à des travaux antérieurs sur des systèmes apparentés et souligne comment le cadre carboné volumineux de l’iodure de tert-butyle oriente la réaction loin d’une simple substitution.
Une nouvelle sorte de basculement moléculaire
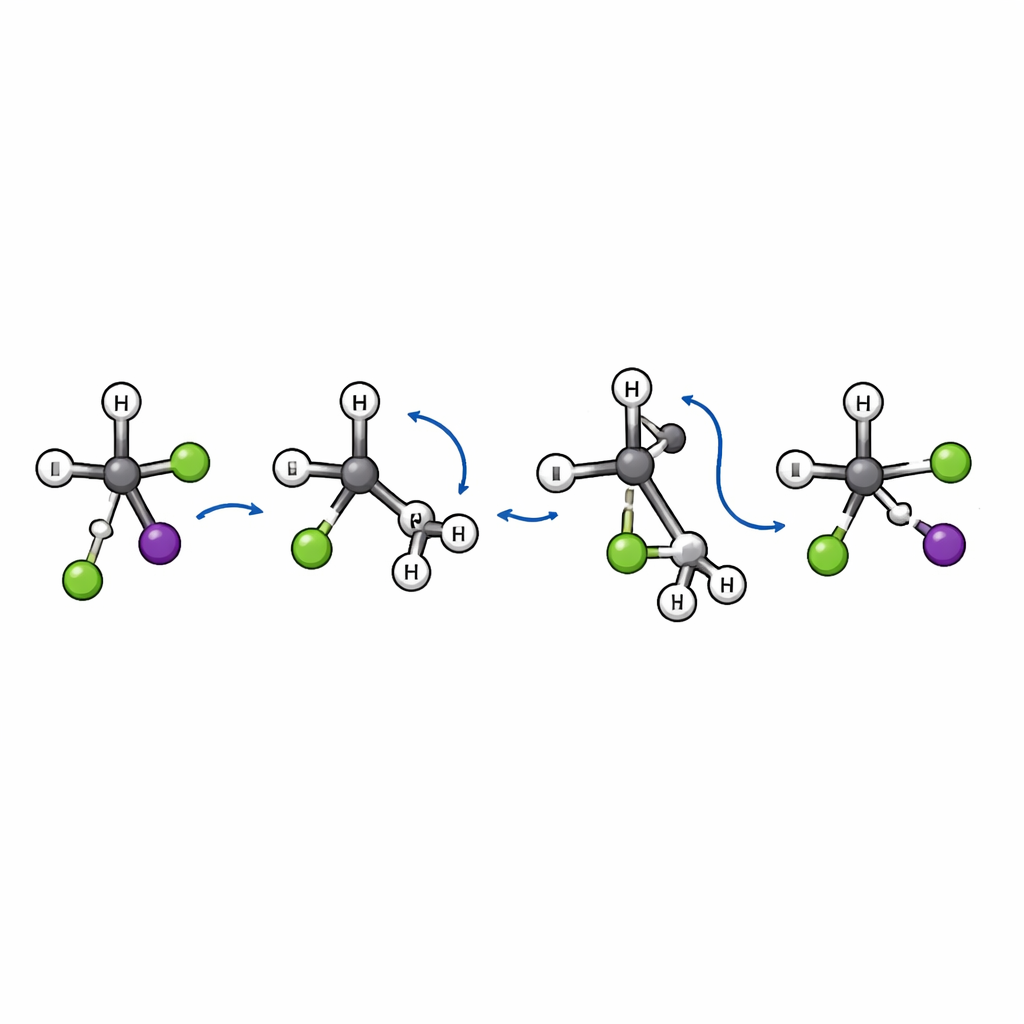
Au sein de la plus petite fraction d’événements de substitution, l’équipe trouve quelque chose d’inattendu. L’image classique de la SN2 implique une « attaque par l’arrière » : l’ion entrant approche derrière le groupe partant et le carbone central inverse sa géométrie, comme un parapluie qui se retourne. Cette inversion change la « main » tridimensionnelle de la molécule. Ici, les simulations révèlent une voie supplémentaire et distincte. Dans ce mécanisme nouvellement découvert de « basculement », le chlorure approche d’abord et étire la liaison carbone–iode. Le groupe tert-butyle volumineux bascule ensuite comme une unité, à la manière d’une page qu’on tourne, tandis que le chlorure finit par se lier au carbone central et que l’iode part. Parce que le cadre carboné bascule au lieu de s’inverser, l’arrangement spatial autour de l’atome de carbone clé est conservé plutôt que renversé.
Signatures du mouvement de basculement
Cette voie de basculement laisse des empreintes nettes dans les motifs de diffusion. Les événements de substitution qui passent par l’inversion habituelle ont tendance à envoyer le fragment iodé vers l’arrière par rapport au chlorure entrant. En revanche, les trajectoires suivant la voie de basculement dispersent majoritairement l’iode vers l’avant, signe que la collision est très directe et que le mouvement de rotation du groupe volumineux joue un rôle clé. Les auteurs identifient également un état de transition spécifique — une sorte de passage énergétique — qui relie réactifs et produits le long de cette nouvelle voie, confirmant qu’il s’agit d’un mécanisme véritable et distinct plutôt que d’une simple variation mineure de mécanismes connus.
Ce que cela signifie pour la chimie
En combinant des expériences de pointe avec un paysage énergétique précis appris par machine, cette étude montre que même l’un des types de réaction les plus étudiés cache encore des surprises. La découverte d’une voie de basculement qui préserve l’arrangement tridimensionnel des atomes élargit les façons connues dont les réactions de substitution peuvent contrôler la forme moléculaire. En termes pratiques, ces connaissances peuvent aider les chimistes à mieux prédire quand certains produits se formeront, surtout dans des molécules encombrées où des mouvements subtils du squelette carboné comptent. À mesure que des techniques similaires seront appliquées à des systèmes plus complexes, d’autres voies cachées pourraient apparaître, affinant notre compréhension de la chorégraphie microscopique du changement chimique.
Citation: Lu, X., Meyer, J., Li, L. et al. Unveiling a flip-over retention mechanism in the gas-phase Cl− + (CH3)3CI SN2 reaction. Nat Commun 17, 3947 (2026). https://doi.org/10.1038/s41467-026-72121-4
Mots-clés: réactions SN2, dynamique des réactions, stéréochimie, élimination vs substitution, imagerie de collisions moléculaires