Clear Sky Science · ru
Кластеры Pt0, индуцированные поверхностными гидроксилами на TiO2, для синергетического катализа реакции водяного газа
Преобразование выхлопов в полезное топливо
Реакция водяного газа тихо поддерживает многие технологии чистой энергетики, помогая превращать угарный газ из промышленных смесей в дополнительный водород и в менее опасный диоксид углерода. В этом исследовании описан новый способ тонкой настройки распространённого платинового катализатора на титановом диоксиде, который делает эту реакцию значительно эффективнее — путём точного контроля крошечных гидроксильных групп, по сути «химических рукояток» из кислорода и водорода на поверхности носителя.
Почему эта реакция важна
Современное производство водорода и улавливание углерода часто опирается на реакцию водяного газа, в которой оксид углерода (CO) реагирует с водой (H2O), образуя диоксид углерода (CO2) и водород (H2). Такие металлы, как платина, отлично ускоряют эту химию, особенно когда они диспергированы в виде очень мелких частиц на оксидах, таких как диоксид титана (TiO2). Однако точный характер взаимодействия металла и носителя может либо способствовать, либо препятствовать работе. Если платина слишком окислена, ей трудно захватывать CO; если на поверхности оксида нет нужных дефектов, вода медленно диссоциирует — оба фактора ограничивают выход водорода.
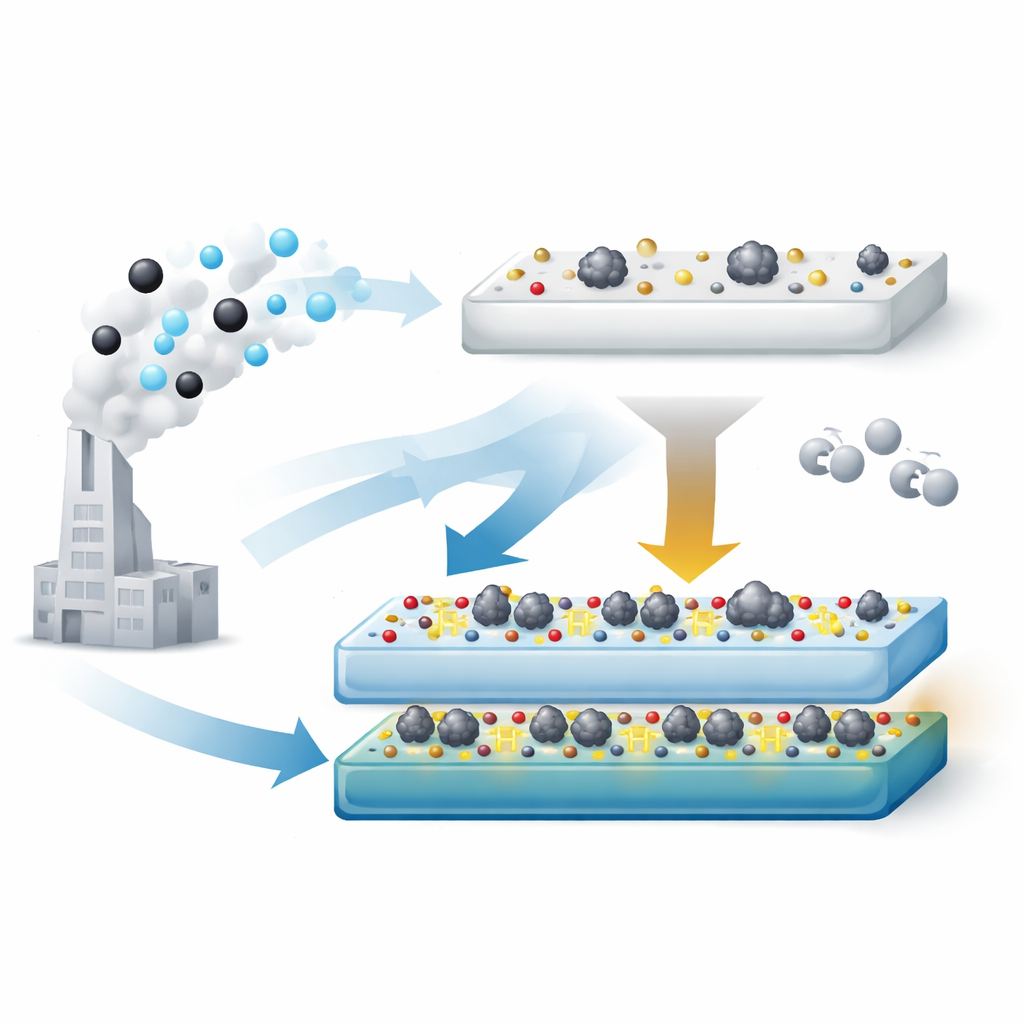
Использование поверхностных «рукояток» для формирования катализатора
Авторы разработали двухэтапный процесс для инженерии носителя TiO2 так, чтобы он нес оптимальное количество поверхностных гидроксилов. Сначала коммерческий TiO2 переводят в титанатную фазу, богатую гидроксил-гр., с помощью сильного щелочного обработки. Затем, нагревая этот материал на воздухе при разных температурах, они постепенно удаляют часть гидроксилов и перестраивают твердое тело. При 500 °C получают носитель (обозначенный TiO2‑T‑500), который всё ещё содержит больше гидроксилов, чем стандартный TiO2, но уже не имеет трубчатой формы, склонной «погружать» металл. При добавлении платины и в рабочем катализаторе формируются крошечные металлические кластеры примерно 2 нанометра, остающиеся доступными на поверхности.
Повышение способности платины захватывать CO
Серия спектроскопических измерений показывает, что дополнительные поверхностные гидроксилы способствуют переводу платины в более металлическое состояние (Pt0) после обработки водородом по сравнению с более окисленным состоянием Ptδ+ на обычном TiO2. Металлическая платина сильнее связывает CO и активирует его легче, что исследователи подтверждают мониторингом адсорбции и десорбции CO в условиях, приближённых к реакционным. На гидроксилсодержащем носителе CO остаётся связанным с платиновыми кластерами даже после длительной промывки и реагирует быстрее с поступающей водой, давая CO2. Участки рядом с интерфейсом между платиной и TiO2 особенно активны, что указывает на то, что в критических шагах участвуют и металл, и носитель.
Гидроксилы как жертвенные помощники
Гидроксилы на TiO2 не просто пассивные наблюдатели. Исследование показывает, что CO может непосредственно потреблять эти гидроксилы, образуя водород и CO2 ещё до полного запуска основной реакции. При этом атомы кислорода удаляются с поверхности, оставляя кислородные вакансии — пропущенные позиции кислорода, которые служат мощными якорями для расщепления новых молекул воды. Данные Рамана, инфракрасной спектроскопии и измерений электронного спинового резонанса указывают на сильное увеличение таких вакансий на модифицированном носителе после начала реакции. Эти дефекты, регенерируемые и пополняемые по мере повторного расщепления воды, повышают способность катализатора активировать H2O без изменения общего механизма реакции.
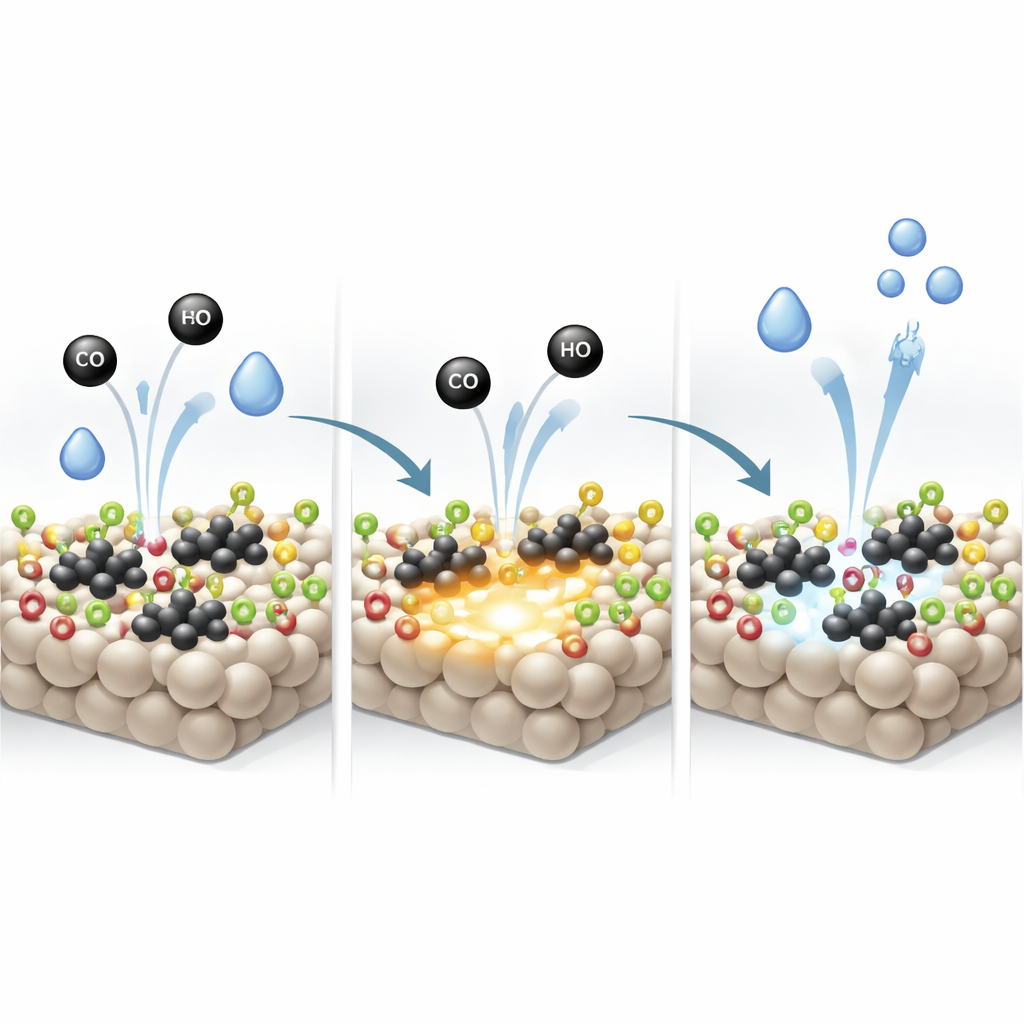
Более быстрая реакция и устойчивая работоспособность
Поскольку гидроксилсодержащий носитель одновременно усиливает активацию CO на металлической платине и активацию воды в кислородных вакансиях, общая реакция водяного газа становится значительно эффективнее. Оптимизированный катализатор демонстрирует скорости реакции и активность на центр примерно в два — три раза выше, чем у сопоставимых платиновых систем на TiO2, описанных ранее, достигая почти полного превращения CO при 250 °C. Он также остаётся стабильным как минимум в течение 70 часов непрерывной работы без потери активности. Проще говоря, исследователи нашли способ «точно настроить» количество поверхностных гидроксилов так, чтобы платиновые кластеры и оксидная поверхность работали сообща, превращая знакомый материал в гораздо более эффективный двигатель для чистого производства водорода.
Цитирование: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Ключевые слова: реакция водяного газа, производство водорода, платиновый катализатор, титановая опора, поверхностные гидроксилы