Clear Sky Science · ar
كتل Pt0 الناتجة عن الهيدروكسيل السطحي على TiO2 لتحفيز متآزر لتفاعل إزاحة غاز الماء
تحويل العادم إلى وقود مفيد
تفاعل إزاحة غاز الماء يدعم بهدوء العديد من تقنيات الطاقة النظيفة، حيث يساعد على تحويل أول أكسيد الكربون من الغازات الصناعية إلى هيدروجين إضافي واثنين أكسيد الكربون الأقل خطورة. تُبلغ هذه الدراسة عن طريقة جديدة لضبط عامل محفز شائع من بلاتين–تيتانيا بحيث يؤدي هذا التفاعل بكفاءة أكبر بكثير، عبر التحكم الدقيق بمجموعات الهيدروكسيل الصغيرة — التي يمكن اعتبارها «مقابض كيميائية» مكوّنة من الأكسجين والهيدروجين — على سطح مادة الدعم.
لماذا يهم هذا التفاعل
تعتمد طرق إنتاج الهيدروجين الحديثة واحتجاز الكربون في كثير من الأحيان على تفاعل إزاحة غاز الماء، حيث يتفاعل أول أكسيد الكربون (CO) مع الماء (H2O) لتكوين ثاني أكسيد الكربون (CO2) والهيدروجين (H2). المعادن مثل البلاديوم والبلاتين ممتازة في تسريع هذه الكيمياء، لا سيما عندما تكون موزعة كجسيمات صغيرة جداً على أكاسيد مثل ثنائي أكسيد التيتانيوم (TiO2). ومع ذلك، فإن الطريقة الدقيقة لتفاعل المعدن مع الدعم يمكن أن تعزز أو تعيق الأداء. إذا أصبح البلاتين مؤكسداً بشدة، فإنه يواجه صعوبة في التقاط CO؛ وإذا افتقر سطح الأكسيد إلى العيوب المناسبة، يكون انقسام الماء بطيئاً — وكلاهما يحد من كمية الهيدروجين الممكن إنتاجها.
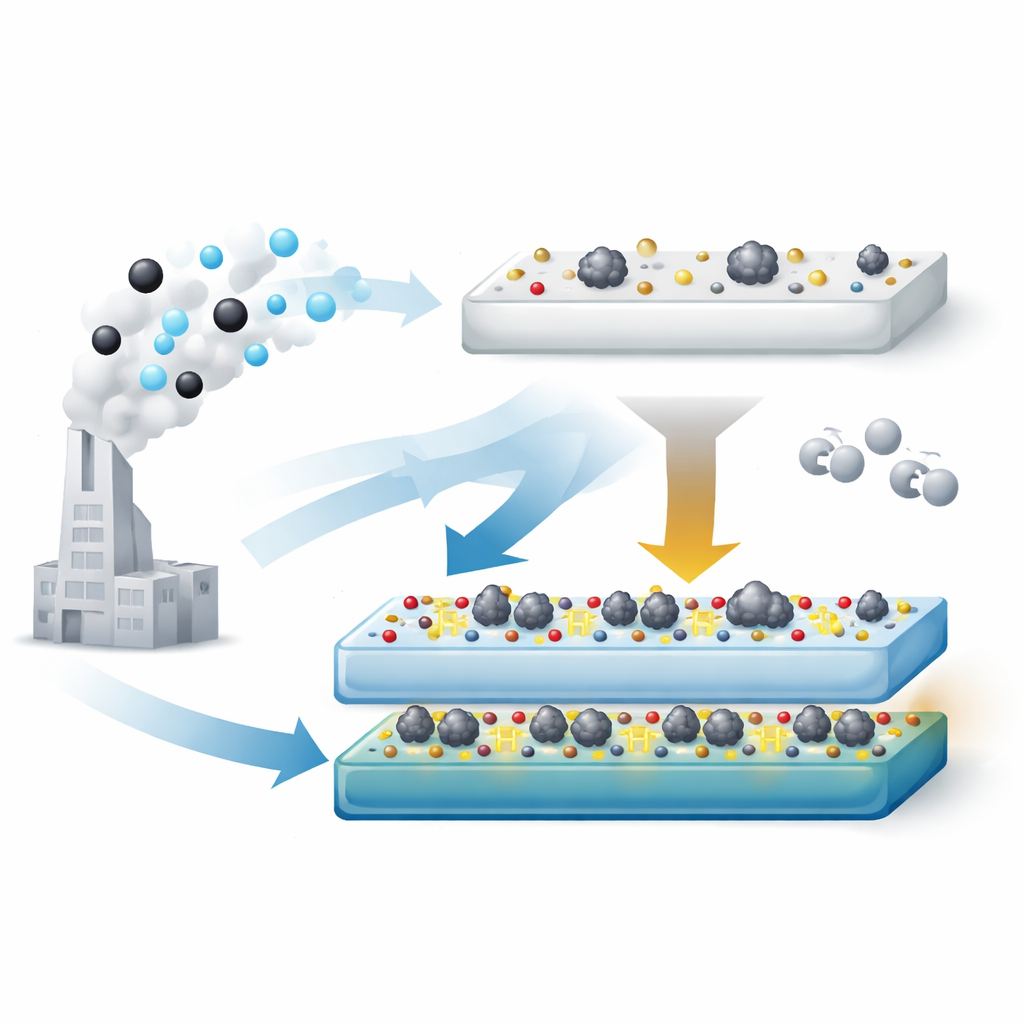
استخدام «مقابض» سطحية لنحت العامل المحفز
طور الباحثون عملية من خطوتين لهندسة دعم TiO2 بحيث يحمل كمية مثالية من مجموعات الهيدروكسيل السطحية. أولاً، يحولون TiO2 التجاري إلى طور تيتانات غني بالهيدروكسيلات باستخدام معالجة قلوية قوية. ثم، عبر تسخين هذه المادة في الهواء عند درجات حرارة مختلفة، يزيلون تدريجياً بعض الهيدروكسيلات ويعيدون تشكيل الصلب. عند 500 °م يحصلون على دعم (يسمى TiO2‑T‑500) يظل حاملاً للمزيد من الهيدروكسيلات مقارنةً بـTiO2 القياسي، لكنه لم يعد في شكل أنبوبي يميل إلى دفن المعدن. عندما يُضاف البلاتين ويُستخدم المحفز، يتشكل على السطح عنقودية معدنية دقيقة بحجم نحو 2 نانومتر تظل متاحة على السطح.
جعل البلاتين أفضل في التقاط CO
من خلال سلسلة من القياسات الطيفية، يُظهر الفريق أن هذه الهيدروكسيلات السطحية الإضافية تساعد في دفع البلاتين إلى حالة أكثر فلزية (Pt0) بعد المعالجة بالهيدروجين، مقارنةً بالحالة المؤكسدة جزئياً Ptδ+ على TiO2 العادي. البلاتين الفلزي يرتبط بـCO بقوة أكبر وينشّطه بسهولة أكبر، وهو ما يؤكده الباحثون بمراقبة كيفية ارتباط CO وابتعاده عن السطح في ظروف شبيهة بالتفاعل. على الدعم الغني بالهيدروكسيل، يبقى CO ملتصقاً بعنقوديات البلاتين حتى بعد تبخير طويل، ويتفاعل بسرعة أكبر مع الماء الداخل لتكوين CO2. المواقع القريبة من واجهة البلاتين وTiO2 تكون نشطة بشكل خاص، مما يشير إلى أن المعدن والدعم يشاركان في الخطوات الحاسمة.
الهيدروكسيلات كمساعدات تضحّي بنفسها
مجموعات الهيدروكسيل على TiO2 ليست مجرد متفرجين سلبيين. تكشف الدراسة أن CO يمكنه استهلاك هذه الهيدروكسيلات مباشرة، مفرزاً الهيدروجين وCO2 حتى قبل بدء التفاعل الرئيسي بشكل كامل. أثناء حدوث ذلك، تُزال ذرات الأكسجين من السطح، تاركة فراغات أكسجينية — مواقع نقص الأكسجين التي تعمل كمراسي قوية لانقسام جزيئات الماء الجديدة. تشير الأدلة من قياسات رامان والأشعة تحت الحمراء وقياسات عزم إلكترون الدوران إلى زيادة قوية في مثل هذه الفراغات على الدعم المهندس بمجرد بدء التفاعل. هذه العيوب، التي تتجدد وتُعاد تعبئتها مع كل انقسام متكرر للماء، تمنح العامل المحفز قدرة محسنة على تفعيل H2O من دون تغيير مسار التفاعل العام.
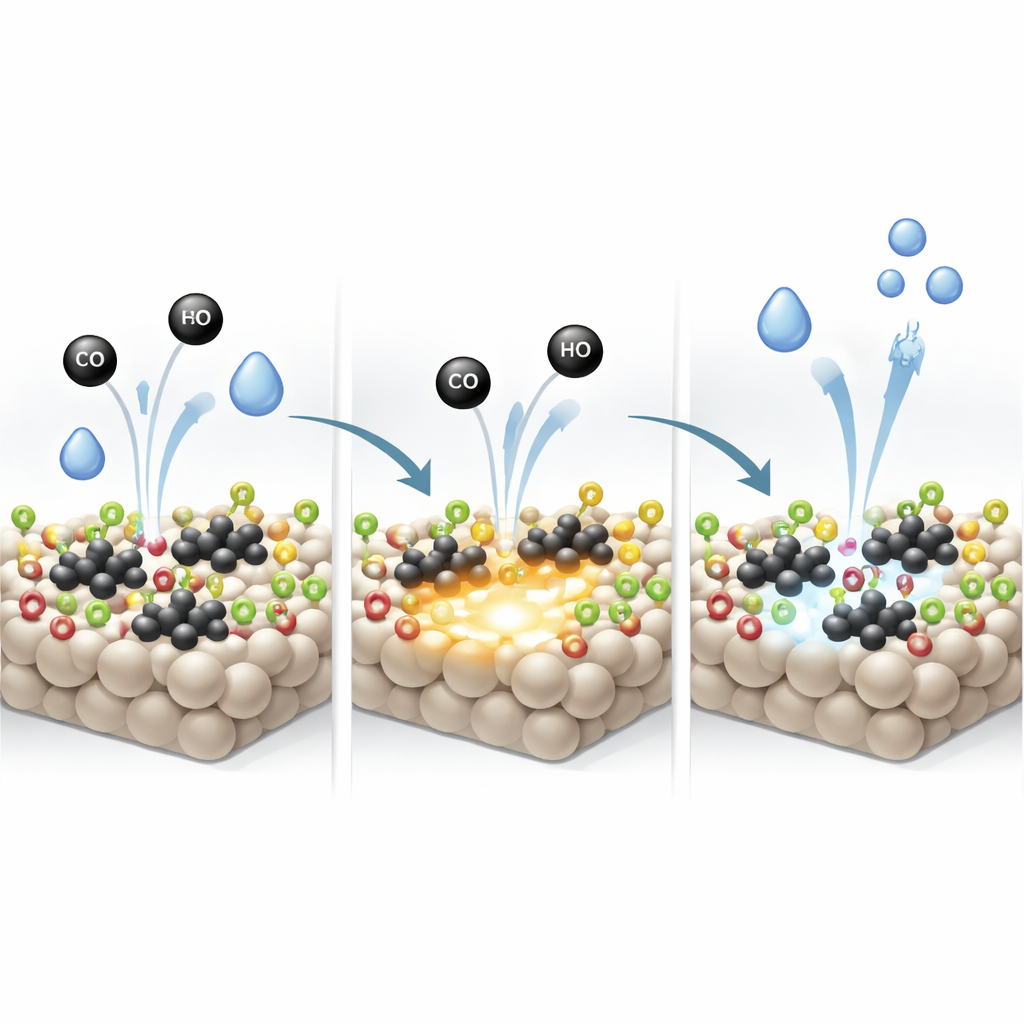
تفاعل أسرع وثبات طويل الأمد
لأن الدعم الغني بالهيدروكسيل يعزز في الوقت نفسه تنشيط CO على البلاتين الفلزي وتنشيط الماء عند فراغات الأكسجين، يصبح تفاعل إزاحة غاز الماء ككل أكثر كفاءة بكثير. يحقق المحفز المحسن معدلات تفاعل وأنشطة لكل موقع أعلى بنحو ضعفين إلى ثلاثة أضعاف مقارنة بأنظمة بلاتين–تيتانيا المماثلة المبلغ عنها سابقاً، ويصل إلى تحويل CO شبه الكامل عند 250 °م. كما يظل مستقراً لمدة لا تقل عن 70 ساعة من التشغيل المستمر، دون فقدان في الأداء. بمصطلحات سهلة الوصول، وجد الباحثون طريقة «لضبط» كمية الهيدروكسيلات السطحية بحيث تتعاون عنقوديات البلاتين وسطح الأكسيد، محولين مادة مألوفة إلى محرك أكثر قدرة لإنتاج الهيدروجين النظيف.
الاستشهاد: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
الكلمات المفتاحية: إزاحة غاز الماء, إنتاج الهيدروجين, عامل محفز بلاتينيوم, دعم تيتانيا, الهيدروكسيلات السطحية