Clear Sky Science · it
Ammassi di Pt0 indotti da idrossili superficiali su TiO2 per catalisi sinergica della reazione water gas shift
Trasformare i gas di scarico in carburante utile
La reazione water gas shift sostiene in modo discreto molte tecnologie per l’energia pulita, aiutando a trasformare il monossido di carbonio proveniente da gas industriali in idrogeno aggiuntivo e in anidride carbonica meno pericolosa. Questo studio presenta un nuovo metodo per mettere a punto un comune catalizzatore platino–titania in modo che svolga quella reazione con molta maggiore efficienza, controllando con cura piccolissimi gruppi idrossilici — sostanzialmente “maniglie chimiche” costituite da ossigeno e idrogeno — sulla superficie del materiale di supporto.
Perché questa reazione è importante
La produzione moderna di idrogeno e la cattura del carbonio si affidano spesso alla reazione water gas shift, in cui il monossido di carbonio (CO) reagisce con l’acqua (H2O) per formare anidride carbonica (CO2) e idrogeno (H2). Metalli come il platino accelerano molto questa chimica, soprattutto quando sono dispersi come particelle molto piccole su ossidi come il biossido di titanio (TiO2). Tuttavia, il modo preciso in cui il metallo e il supporto interagiscono può favorire o ostacolare la prestazione. Se il platino si ossida troppo, fatica ad adsorbire il CO; se la superficie dell’ossido manca dei difetti giusti, l’acqua si scinde lentamente — entrambi i fattori limitano la quantità di idrogeno che si può produrre.
Usare “maniglie” superficiali per scolpire il catalizzatore
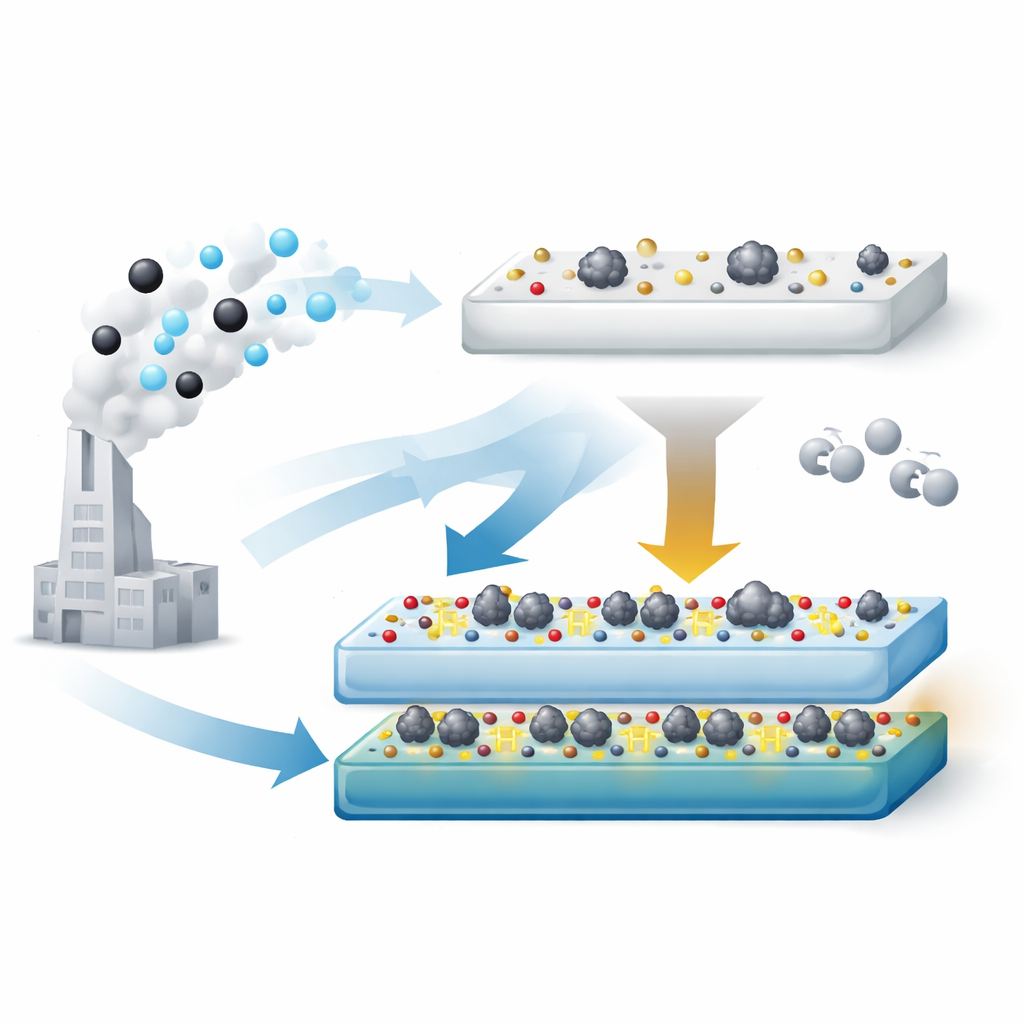
Gli autori hanno ideato un processo in due fasi per progettare il supporto in TiO2 in modo che presenti una quantità ottimale di gruppi idrossilici superficiali. Prima convertono TiO2 commerciale in una fase titanata ricca di idrossili mediante un trattamento con una base forte. Poi, riscaldando questo materiale in aria a diverse temperature, rimuovono gradualmente alcuni idrossili e rimodellano il solido. A 500 °C ottengono un supporto (denominato TiO2‑T‑500) che mantiene più idrossili rispetto al TiO2 standard, ma non è più nella forma tubolare che tende a seppellire il metallo. Quando si aggiunge il platino e si utilizza il catalizzatore, si formano minuscoli ammassi metallici di circa 2 nanometri di dimensione che restano accessibili in superficie.
Rendere il platino più efficace nell’agganciare il CO
Attraverso una serie di misure spettroscopiche, il gruppo mostra che questi idrossili superficiali extra aiutano a convertire il platino in uno stato più metallico (Pt0) dopo il trattamento in idrogeno, rispetto allo stato più ossidato Ptδ+ su TiO2 ordinario. Il platino metallico lega il CO più fortemente e lo attiva più facilmente, come i ricercatori confermano monitorando come il CO si adsorbe e si desorbe dalla superficie in condizioni simili a quelle di reazione. Sul supporto ricco di idrossili, il CO rimane legato agli ammassi di platino anche dopo lunghi lavaggi e reagisce più rapidamente con l’acqua entrante per formare CO2. I siti vicino all’interfaccia tra platino e TiO2 sono particolarmente attivi, suggerendo che sia il metallo sia il supporto partecipano ai passaggi critici.
Idrossili come aiutanti sacrificabili
I gruppi idrossilici sul TiO2 non sono soltanto spettatori passivi. Lo studio rivela che il CO può consumare direttamente questi idrossili, producendo idrogeno e CO2 ancor prima che la reazione principale sia pienamente avviata. Durante questo processo, atomi di ossigeno vengono rimossi dalla superficie, lasciando vacanze di ossigeno — siti mancanti che fungono da ancore potenti per la scissione di nuove molecole d’acqua. Evidenze da misure Raman, infrarosse e di spin elettronico indicano tutte un forte aumento di tali vacanze sul supporto ingegnerizzato una volta che la reazione è in corso. Questi difetti, rigenerati e riempiti man mano che l’acqua si dissocia ripetutamente, conferiscono al catalizzatore una maggiore capacità di attivare l’H2O senza cambiare il percorso reattivo complessivo.
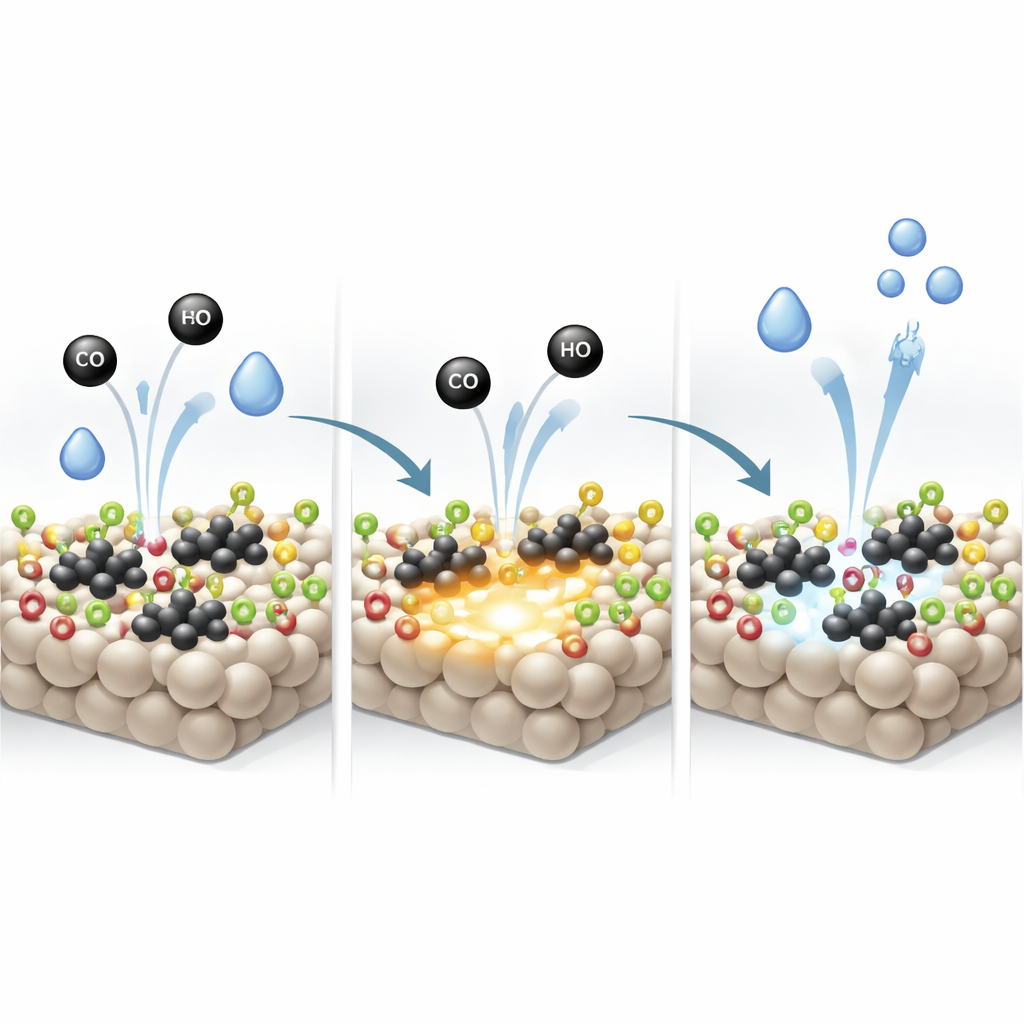
Reazione più rapida e stabilità duratura
Poiché il supporto ricco di idrossili potenzia contemporaneamente l’attivazione del CO sul platino metallico e l’attivazione dell’acqua alle vacanze di ossigeno, la reazione water gas shift nel suo complesso diventa molto più efficiente. Il catalizzatore ottimizzato raggiunge velocità di reazione e attività per sito circa due‑tre volte superiori rispetto a sistemi platino–titania comparabili riportati in precedenza, arrivando a quasi completa conversione del CO a 250 °C. Rimane inoltre stabile per almeno 70 ore di funzionamento continuo, senza perdita di prestazioni. In termini accessibili, i ricercatori hanno trovato un modo per “regolare” la giusta quantità di idrossili superficiali in modo che gli ammassi di platino e la superficie dell’ossido lavorino insieme, trasformando un materiale familiare in un motore molto più efficiente per la produzione di idrogeno pulito.
Citazione: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Parole chiave: water gas shift, produzione di idrogeno, catalizzatore al platino, supporto di titania, idrossili superficiali