Clear Sky Science · pl
Powierzchniowo hydroksylowe klastry Pt0 na TiO2 dla synergicznej katalizy reakcji przesunięcia gazu wodnego
Przekształcanie spalin w użyteczne paliwo
Reakcja przesunięcia gazu wodnego w subtelny sposób wspiera wiele technologii czystej energii, pomagając przekształcać tlenek węgla z gazów przemysłowych w dodatkowy wodór i bezpieczniejszy dwutlenek węgla. W tej pracy opisano nowy sposób precyzyjnego dostrojenia powszechnego katalizatora platyna–tlenek tytanu, dzięki któremu reakcja ta przebiega znacznie wydajniej, przez staranne kontrolowanie maleńkich grup hydroksylowych — w praktyce „chemicznych uchwytów” z tlenu i wodoru — na powierzchni materiału nośnikowego.
Dlaczego ta reakcja ma znaczenie
Współczesna produkcja wodoru i wychwytywanie dwutlenku węgla często opierają się na reakcji przesunięcia gazu wodnego, w której tlenek węgla (CO) reaguje z wodą (H2O), tworząc dwutlenek węgla (CO2) i wodór (H2). Metale takie jak platyna znacznie przyspieszają tę chemię, zwłaszcza gdy są rozproszone jako bardzo małe cząstki na tlenkach, takich jak tlenek tytanu (TiO2). Jednak dokładny sposób, w jaki metal współdziała z nośnikiem, może zarówno wspierać, jak i ograniczać wydajność. Jeśli platyna jest zbyt utleniona, gorzej wiąże CO; jeśli powierzchnia tlenku pozbawiona jest odpowiednich defektów, woda rozbija się powoli — obie sytuacje ograniczają produkcję wodoru.
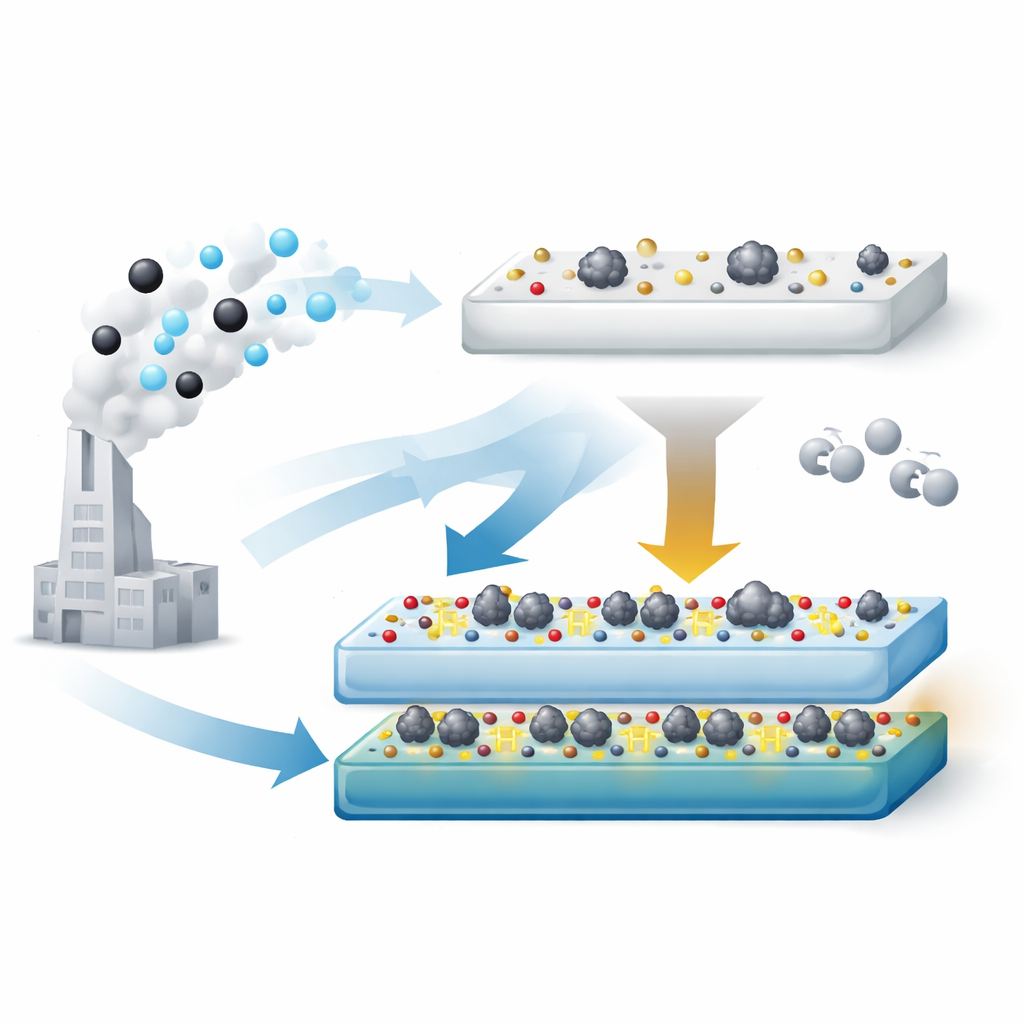
Wykorzystanie powierzchniowych „uchwytów” do formowania katalizatora
Autorzy opracowali dwustopniowy proces w celu zaprojektowania nośnika TiO2 tak, aby miał optymalną ilość grup hydroksylowych na powierzchni. Najpierw przekształcają komercyjny TiO2 w fazę tytanianową bogatą w hydroksyle, stosując silne traktowanie alkaliczne. Następnie, poprzez podgrzewanie tego materiału w powietrzu w różnych temperaturach, stopniowo usuwają część hydroksyli i przeobrażają strukturę stałą. W 500 °C otrzymują nośnik (oznaczony jako TiO2‑T‑500), który nadal nosi więcej hydroksyli niż standardowy TiO2, ale nie ma już rurkowatej formy, która zwykle zatapiałaby metal. Po dodaniu platyny i zastosowaniu katalizatora powstają maleńkie metaliczne klastry o wielkości około 2 nanometrów, które pozostają dostępne na powierzchni.
Uczynienie platyny lepszą w chwytaniu CO
Przez serię pomiarów spektroskopowych zespół wykazał, że dodatkowe hydroksyle powierzchniowe sprzyjają przekształceniu platyny w bardziej metaliczny stan (Pt0) po traktowaniu wodorem, w porównaniu z bardziej utlenionym stanem Ptδ+ na zwykłym TiO2. Metaliczna platyna silniej wiąże CO i aktywuje go łatwiej, co badacze potwierdzili, monitorując przyczepianie się i odchodzenie CO z powierzchni w warunkach podobnych do reakcyjnych. Na nośniku bogatym w hydroksyle CO pozostaje związany z klastrami platyny nawet po długim płukaniu i reaguje szybciej z nadchodzącą wodą, tworząc CO2. Miejsca w pobliżu interfejsu między platyną a TiO2 są szczególnie aktywne, co sugeruje, że zarówno metal, jak i nośnik uczestniczą w kluczowych etapach reakcji.
Hydroksyle jako poświęcające się pomocniki
Grupy hydroksylowe na TiO2 nie są jedynie biernymi obserwatorami. Badanie ujawnia, że CO może bezpośrednio zużywać te hydroksyle, wytwarzając wodór i CO2 nawet zanim główna reakcja w pełni się rozpocznie. W miarę zachodzenia tych procesów atomy tlenu są usuwane z powierzchni, pozostawiając wakansy tlenowe — brakujące miejsca tlenu, które działają jako silne kotwice do rozszczepiania nowych cząsteczek wody. Dowody z pomiarów Ramana, podczerwieni i elektronowego spinu wskazują na wyraźny wzrost takich wakansów na zmodyfikowanym nośniku po uruchomieniu reakcji. Te defekty, regenerowane i uzupełniane w miarę kolejnych rozpadów wody, zwiększają zdolność katalizatora do aktywacji H2O bez zmiany ogólnej ścieżki reakcji.
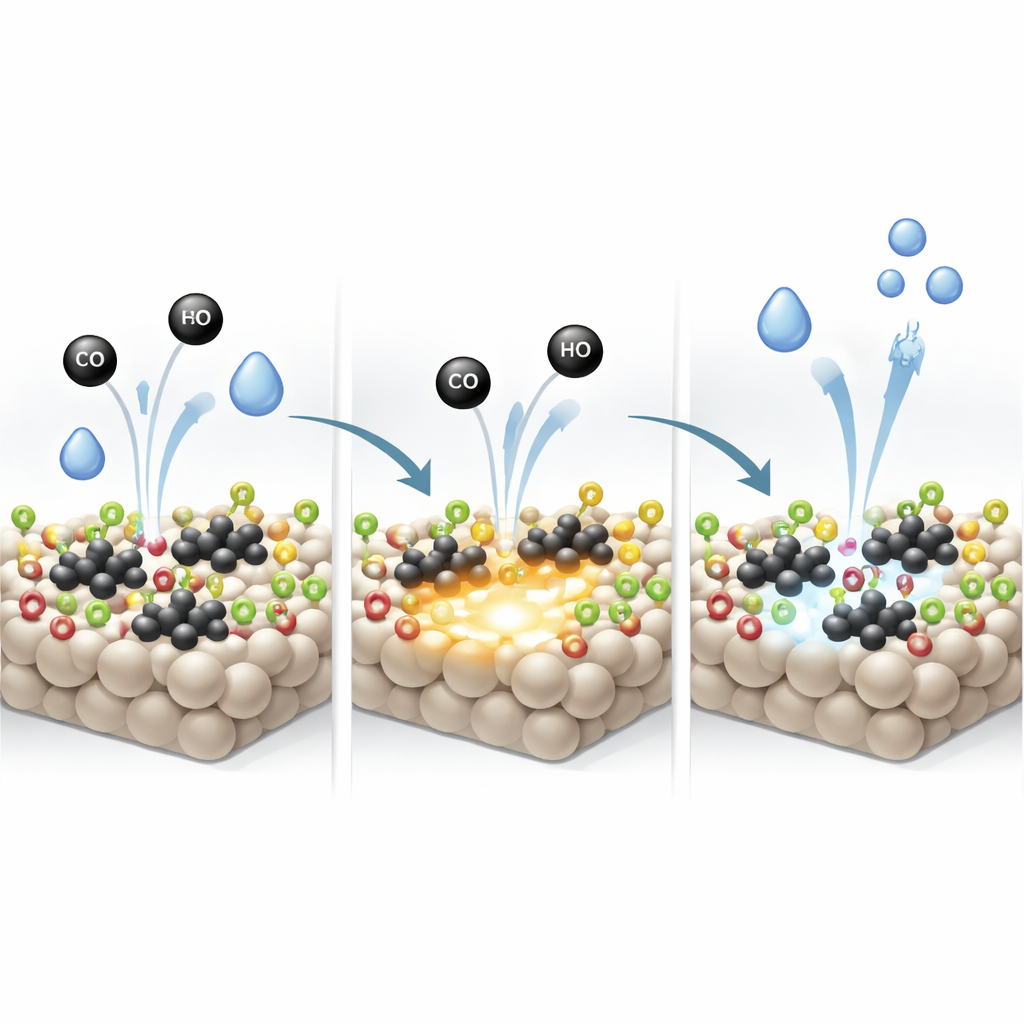
Szybsza reakcja i trwała stabilność
Ponieważ nośnik bogaty w hydroksyle jednocześnie zwiększa aktywację CO na metalicznej platynie i aktywację wody przy wakansach tlenowych, całkowita reakcja przesunięcia gazu wodnego staje się znacznie bardziej efektywna. Optymalizowany katalizator osiąga szybkości reakcji i aktywności na miejsce około dwa do trzech razy wyższe niż porównywalne systemy platyna–TiO2 opisane wcześniej, osiągając niemal całkowitą konwersję CO w 250 °C. Pozostaje również stabilny przez co najmniej 70 godzin ciągłej pracy bez spadku wydajności. Prosto mówiąc, badacze znaleźli sposób, by „ustawić” odpowiednią ilość hydroksyli powierzchniowych tak, aby klastry platyny i powierzchnia tlenku współdziałały, przekształcając znany materiał w znacznie sprawniejszy silnik produkcji czystego wodoru.
Cytowanie: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Słowa kluczowe: reakcja przesunięcia gazu wodnego, produkcja wodoru, katalizator platynowy, nośnik tytanianowy, hydroksyle powierzchniowe