Clear Sky Science · es
Clústeres de Pt0 inducidos por hidroxilos superficiales en TiO2 para catálisis sinérgica del gas de agua
Convertir los gases de escape en combustible útil
La reacción agua‑gas sustenta discretamente muchas tecnologías de energía limpia, ayudando a transformar el monóxido de carbono de gases industriales en hidrógeno adicional y en dióxido de carbono menos peligroso. Este estudio presenta una nueva forma de afinar un catalizador común de platino–titania para que realice esa reacción con mucha mayor eficiencia, mediante el control cuidadoso de pequeños grupos hidroxilo—esencialmente “asas químicas” formadas por oxígeno e hidrógeno—en la superficie del material soporte.
Por qué importa esta reacción
La producción moderna de hidrógeno y la captura de carbono a menudo dependen de la reacción agua‑gas, en la que el monóxido de carbono (CO) reacciona con agua (H2O) para formar dióxido de carbono (CO2) e hidrógeno (H2). Metales como el platino son excelentes para acelerar esta química, especialmente cuando se dispersan como partículas muy pequeñas sobre óxidos como el dióxido de titanio (TiO2). Sin embargo, la forma exacta en que el metal y el soporte interactúan puede favorecer o limitar el rendimiento. Si el platino se oxida demasiado, le cuesta adsorber CO; si la superficie del óxido carece de los defectos adecuados, el agua se fragmenta lentamente—ambas cosas limitan la cantidad de hidrógeno que se puede producir.
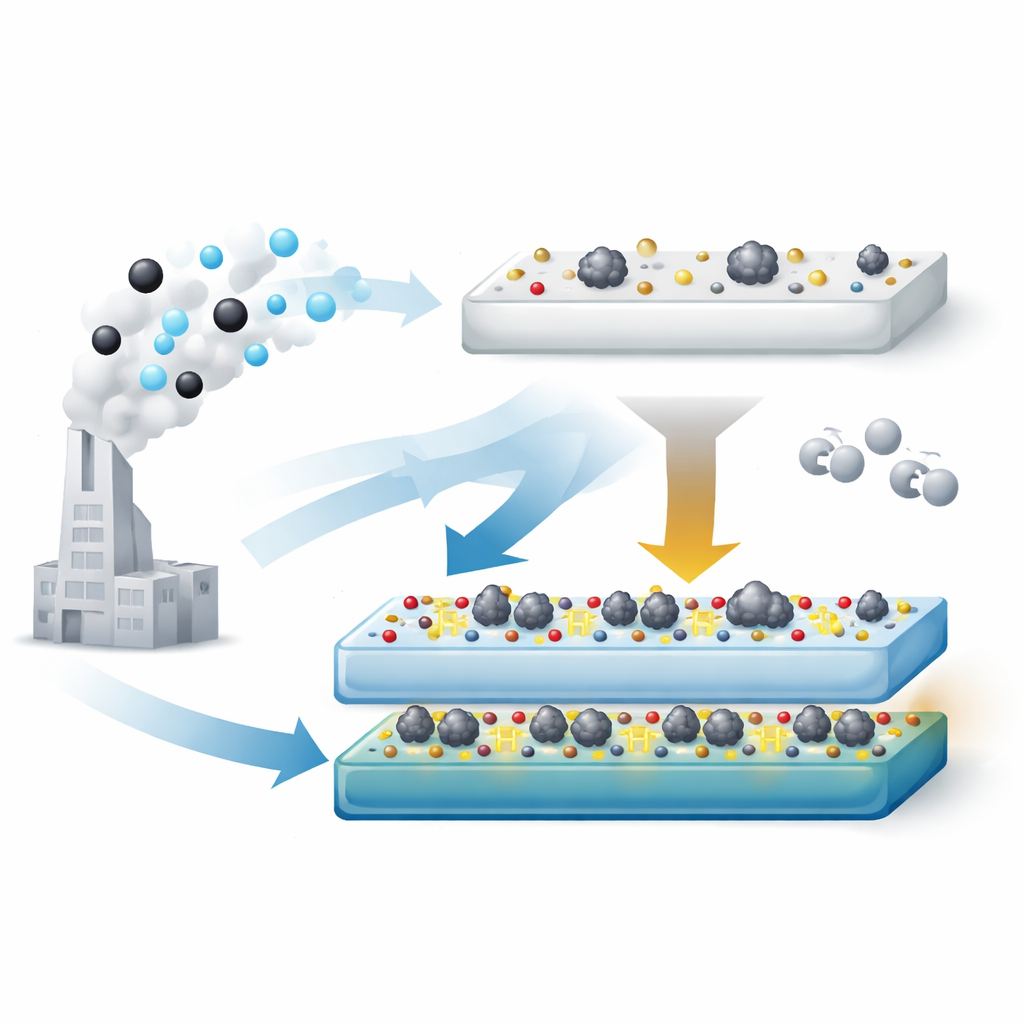
Usar “asas” superficiales para esculpir el catalizador
Los autores idearon un proceso en dos pasos para diseñar el soporte de TiO2 de modo que presente una cantidad óptima de grupos hidroxilo en la superficie. Primero convierten TiO2 comercial en una fase titanato rica en hidroxilos mediante un tratamiento con un álcali fuerte. Luego, al calentar este material en aire a distintas temperaturas, van eliminando gradualmente algunos hidroxilos y remodelando el sólido. A 500 °C obtienen un soporte (denominado TiO2‑T‑500) que sigue conservando más hidroxilos que el TiO2 estándar, pero que ya no tiene la morfología tubular que tiende a enterrar el metal. Cuando se añade platino y se utiliza el catalizador, se forman pequeños clústeres metálicos de alrededor de 2 nanómetros que permanecen accesibles en la superficie.
Hacer que el platino sea mejor para captar CO
A través de una serie de mediciones espectroscópicas, el equipo muestra que estos hidroxilos superficiales adicionales favorecen que el platino adopte un estado más metálico (Pt0) tras el tratamiento con hidrógeno, en comparación con el estado más oxidado Ptδ+ sobre TiO2 ordinario. El platino metálico liga el CO con mayor fuerza y lo activa con más facilidad, lo que los investigadores confirman al monitorizar cómo el CO se adsorbe y desorbe de la superficie en condiciones similares a las de la reacción. En el soporte rico en hidroxilos, el CO permanece unido a los clústeres de platino incluso después de purgas prolongadas, y reacciona más rápidamente con el agua entrante para formar CO2. Los sitios cercanos a la interfaz entre platino y TiO2 son especialmente activos, lo que sugiere que tanto el metal como el soporte participan en los pasos críticos.
Hidroxilos como ayudantes sacrificiales
Los grupos hidroxilo en TiO2 no son meros espectadores pasivos. El estudio revela que el CO puede consumir directamente estos hidroxilos, produciendo hidrógeno y CO2 incluso antes de que la reacción principal comience completamente. A medida que esto ocurre, átomos de oxígeno se eliminan de la superficie, dejando vacantes de oxígeno—sitios sin oxígeno que actúan como anclas potentes para fragmentar nuevas moléculas de agua. Evidencias procedentes de Raman, infrarrojo y mediciones de espín electrónico apuntan todas a un fuerte aumento de tales vacantes en el soporte diseñado una vez que la reacción está en marcha. Estos defectos, regenerados y rellenados conforme el agua se rompe repetidamente, dotan al catalizador de una mayor capacidad para activar H2O sin cambiar la vía global de la reacción.
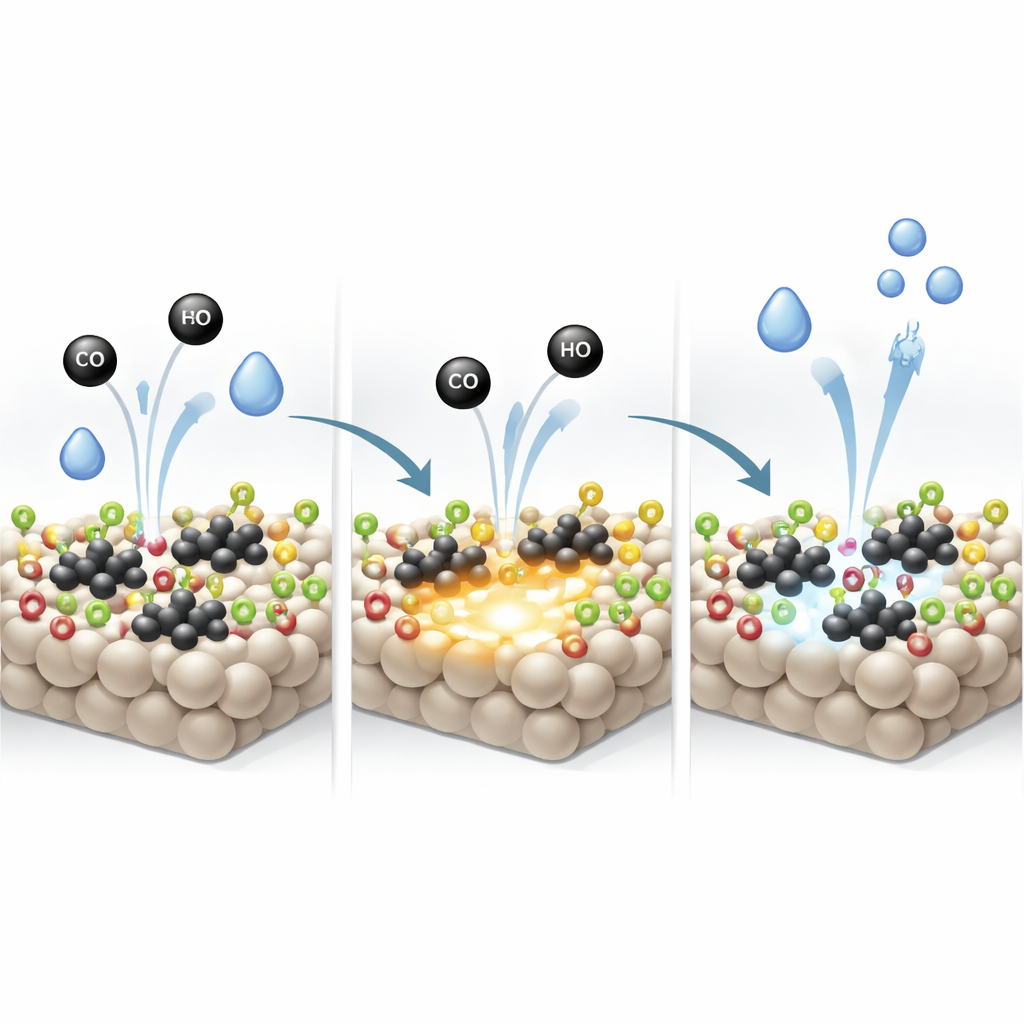
Reacción más rápida y estabilidad duradera
Puesto que el soporte rico en hidroxilos potencia simultáneamente la activación de CO sobre el platino metálico y la activación del agua en las vacantes de oxígeno, la reacción agua‑gas en su conjunto se vuelve mucho más eficiente. El catalizador optimizado alcanza tasas de reacción y actividades por sitio aproximadamente dos a tres veces mayores que sistemas platino–titania comparables reportados anteriormente, logrando casi la conversión completa de CO a 250 °C. Además, se mantiene estable al menos durante 70 horas de operación continua, sin pérdida de rendimiento. En términos accesibles, los investigadores han encontrado una manera de “ajustar” la cantidad justa de hidroxilos superficiales para que los clústeres de platino y la superficie de óxido trabajen juntos, transformando un material conocido en un motor mucho más capaz para la producción de hidrógeno limpio.
Cita: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Palabras clave: reacción agua‑gas, producción de hidrógeno, catálisis con platino, soporte de titania, hidroxilos superficiales