Clear Sky Science · fr
Des amas de Pt0 induits par des hydroxyles de surface sur TiO2 pour une catalyse synergique de la réaction eau‑gaz de synthèse
Transformer les gaz d'échappement en carburant utile
La réaction eau‑gaz de synthèse soutient discrètement de nombreuses technologies d'énergie propre, en aidant à convertir le monoxyde de carbone provenant des gaz industriels en hydrogène supplémentaire et en dioxyde de carbone moins dangereux. Cette étude rapporte une nouvelle façon d'affiner un catalyseur courant platine–titania afin qu'il réalise cette réaction beaucoup plus efficacement, en contrôlant soigneusement de minuscules groupes hydroxyle—essentiellement des « poignées chimiques » constituées d'oxygène et d'hydrogène—à la surface du matériau porteur.
Pourquoi cette réaction compte
La production moderne d'hydrogène et la capture du carbone reposent souvent sur la réaction eau‑gaz de synthèse, où le monoxyde de carbone (CO) réagit avec l'eau (H2O) pour former du dioxyde de carbone (CO2) et de l'hydrogène (H2). Des métaux comme le platine accélèrent très efficacement cette chimie, notamment lorsqu'ils sont dispersés sous forme de très petites particules sur des oxydes tels que le dioxyde de titane (TiO2). Cependant, la manière exacte dont le métal et le support interagissent peut aider ou nuire aux performances. Si le platine devient trop oxydé, il a du mal à capter le CO ; si la surface de l'oxyde manque des défauts appropriés, l'eau se scinde lentement—ce qui limite la quantité d'hydrogène produite.
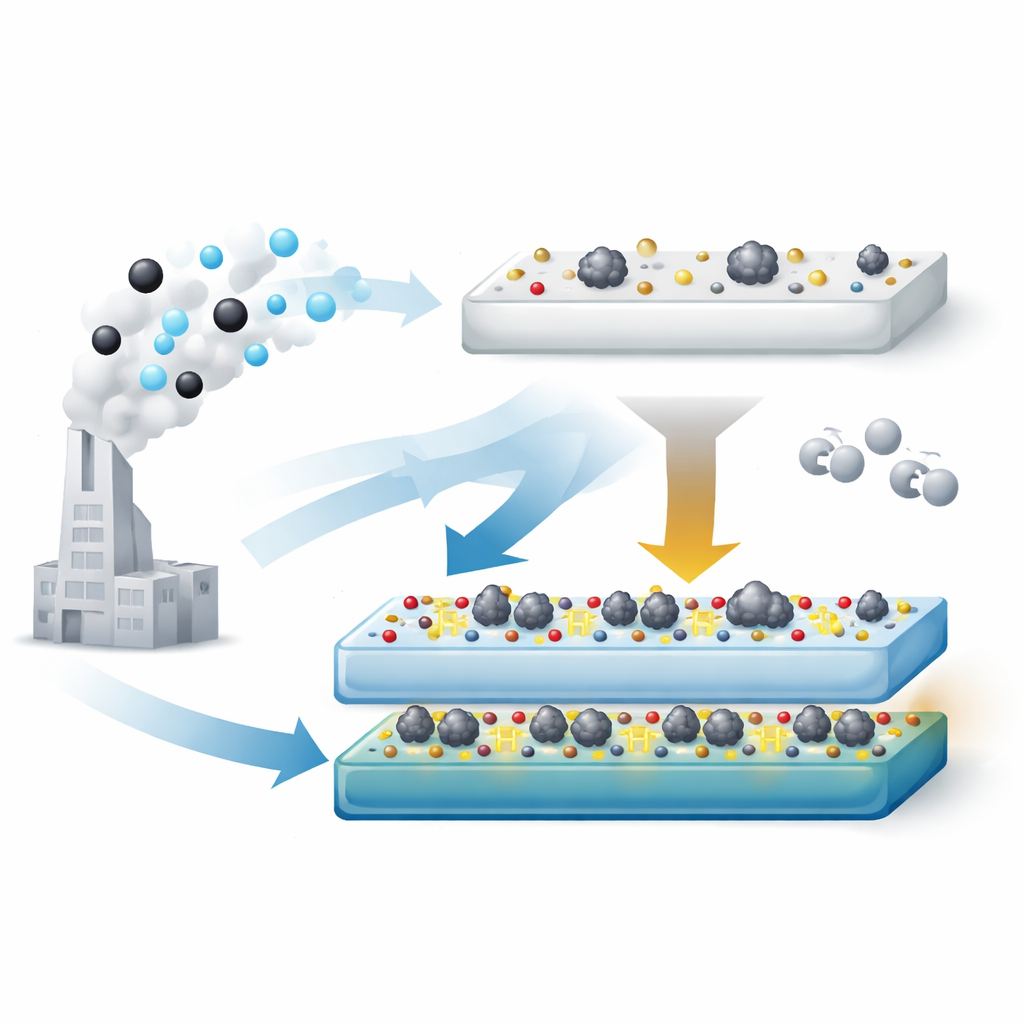
Utiliser des « poignées » de surface pour façonner le catalyseur
Les auteurs ont mis au point un procédé en deux étapes pour ingérer le support TiO2 afin qu'il porte une quantité optimale de groupes hydroxyle de surface. D'abord, ils convertissent le TiO2 commercial en une phase titanate riche en hydroxyles via un traitement alcalin fort. Ensuite, en chauffant ce matériau à l'air à différentes températures, ils éliminent progressivement certains hydroxyles et remodèlent le solide. À 500 °C, ils obtiennent un support (appelé TiO2‑T‑500) qui conserve plus d'hydroxyles que le TiO2 standard, mais n'est plus sous une forme tubulaire qui a tendance à enfouir le métal. Lors de l'ajout de platine et de l'utilisation du catalyseur, de petits amas métalliques d'environ 2 nanomètres se forment et restent accessibles à la surface.
Rendre le platine meilleur pour capter le CO
Au moyen d'une série de mesures spectroscopiques, l'équipe montre que ces hydroxyles de surface supplémentaires favorisent la réduction du platine vers un état plus métallique (Pt0) après traitement à l'hydrogène, par rapport à l'état plus oxydé Ptδ+ observé sur le TiO2 ordinaire. Le platine métallique lie le CO plus fortement et l'active plus facilement, ce que les chercheurs confirment en surveillant comment le CO s'adsorbe et se désorbe de la surface dans des conditions proches de la réaction. Sur le support riche en hydroxyles, le CO reste attaché aux amas de platine même après des purges prolongées, et réagit plus rapidement avec l'eau entrante pour former du CO2. Les sites proches de l'interface entre le platine et le TiO2 sont particulièrement actifs, ce qui suggère que le métal et le support participent tous deux aux étapes critiques.
Les hydroxyles comme aides sacrificielles
Les groupes hydroxyle sur le TiO2 ne sont pas de simples spectateurs. L'étude révèle que le CO peut consommer directement ces hydroxyles, produisant de l'hydrogène et du CO2 avant même que la réaction principale ne soit complètement engagée. Ce faisant, des atomes d'oxygène sont retirés de la surface, laissant des vacants d'oxygène—sites dépourvus d'oxygène qui agissent comme de puissants ancrages pour la scission de nouvelles molécules d'eau. Les preuves issues de mesures Raman, infrarouges et de spin électronique indiquent toutes une forte augmentation de ces vacants sur le support modifié une fois la réaction lancée. Ces défauts, régénérés et réalimentés à mesure que l'eau se dissocie à plusieurs reprises, confèrent au catalyseur une capacité renforcée à activer H2O sans modifier la voie réactionnelle globale.
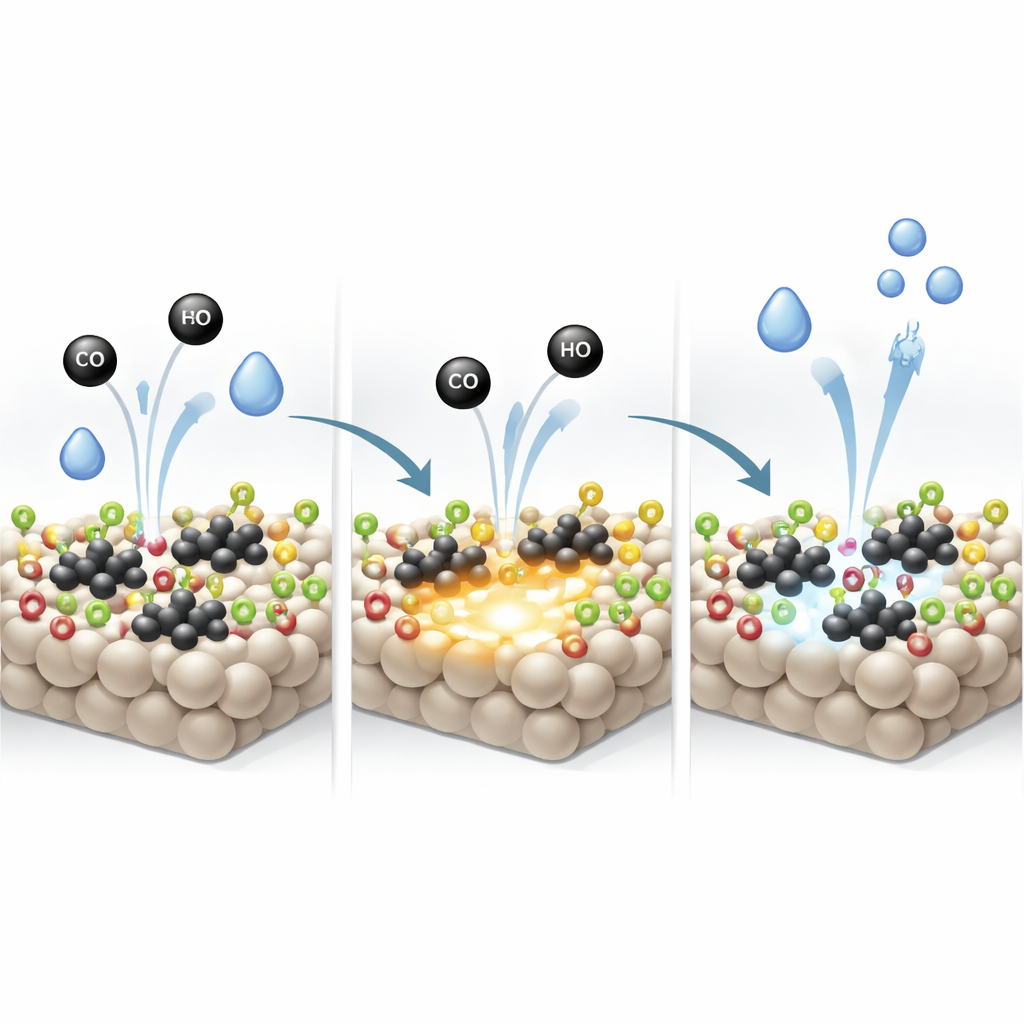
Réaction plus rapide et stabilité durable
Parce que le support riche en hydroxyles renforce simultanément l'activation du CO sur le platine métallique et l'activation de l'eau aux vacants d'oxygène, la réaction eau‑gaz de synthèse dans son ensemble devient beaucoup plus efficace. Le catalyseur optimisé atteint des vitesses de réaction et des activités par site environ deux à trois fois supérieures à celles de systèmes platine–titania comparables rapportés antérieurement, atteignant presque une conversion complète du CO à 250 °C. Il reste également stable pendant au moins 70 heures d'opération continue, sans perte de performance. En termes accessibles, les chercheurs ont trouvé un moyen de « régler » la quantité exacte d'hydroxyles de surface pour que les amas de platine et la surface de l'oxyde travaillent de concert, transformant un matériau familier en un moteur beaucoup plus performant pour la production d'hydrogène propre.
Citation: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Mots-clés: réaction eau‑gaz de synthèse, production d'hydrogène, catalyseur au platine, support titane, hydroxyles de surface