Clear Sky Science · de
Oberflächen‑Hydroxyl-induzierte Pt0‑Cluster auf TiO2 für synergetische Wasser‑Gas‑Shift‑Katalyse
Abgase in nützlichen Brennstoff verwandeln
Die Wasser‑Gas‑Shift‑Reaktion bildet im Stillen die Grundlage vieler sauberer Energietechnologien, indem sie Kohlenmonoxid aus Industriegasen in zusätzlichen Wasserstoff und in weniger problematisches Kohlendioxid überführt. Diese Studie beschreibt eine neue Methode, einen verbreiteten Platin–Titanoxid‑Katalysator so zu optimieren, dass er diese Reaktion deutlich effizienter durchführt, indem winzige Hydroxylgruppen — im Grunde „chemische Griffpunkte“ aus Sauerstoff und Wasserstoff — auf der Oberfläche des Trägermaterials gezielt gesteuert werden.
Warum diese Reaktion wichtig ist
Moderne Wasserstoffproduktion und CO‑Abtrennung stützen sich oft auf die Wasser‑Gas‑Shift‑Reaktion, bei der Kohlenmonoxid (CO) mit Wasser (H2O) zu Kohlendioxid (CO2) und Wasserstoff (H2) reagiert. Metalle wie Platin beschleunigen diese Chemie besonders effektiv, vor allem wenn sie als sehr kleine Partikel auf Oxiden wie Titandioxid (TiO2) verteilt sind. Die genaue Wechselwirkung zwischen Metall und Träger kann jedoch Leistung fördern oder hemmen. Ist Platin zu stark oxidiert, fällt es ihm schwer, CO zu binden; fehlt der Oxidoberfläche die passenden Defekte, spaltet Wasser nur langsam — beides begrenzt die Wasserstoffausbeute.
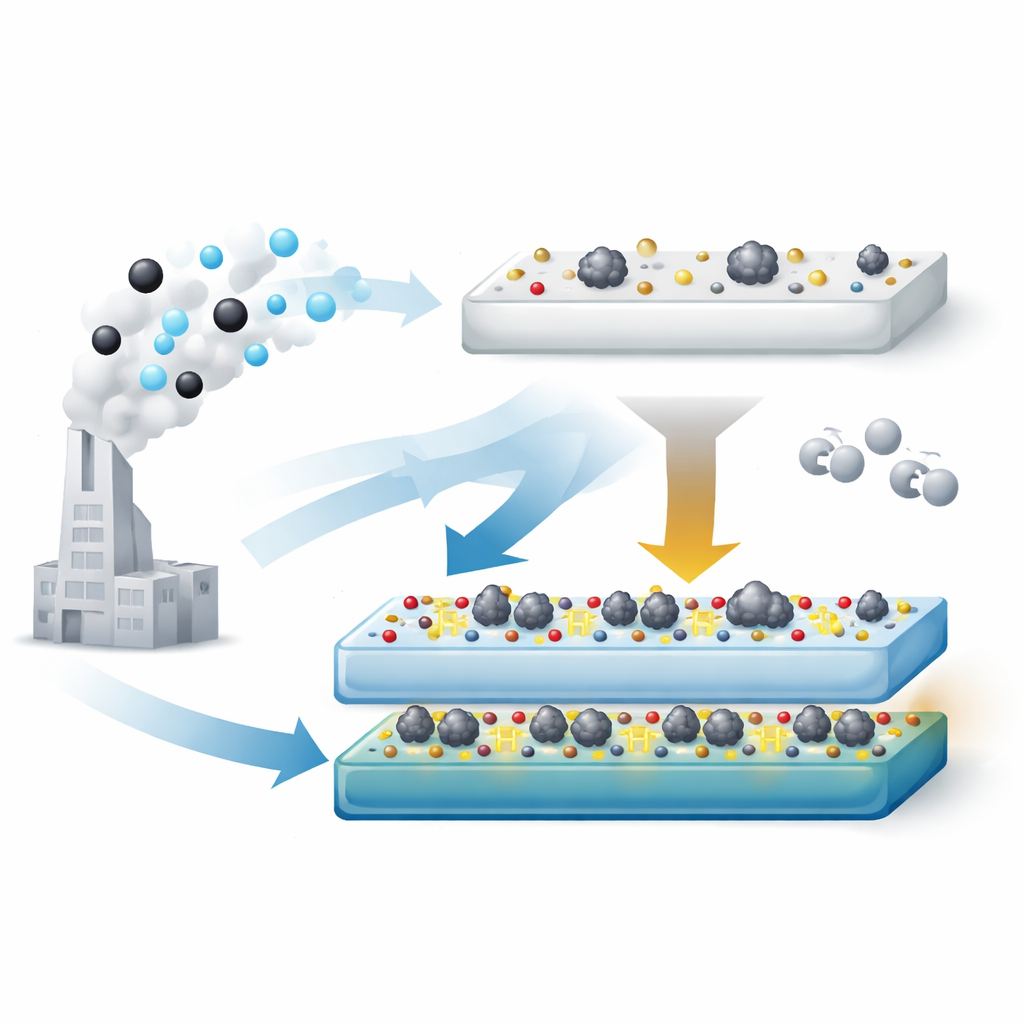
Die Oberfläche mit „Handgriffen“ formen
Die Autoren entwickelten einen zweistufigen Prozess, um den TiO2‑Träger so zu bearbeiten, dass er eine optimale Menge an Oberflächenhydroxylen trägt. Zunächst wandeln sie handelsübliches TiO2 durch eine starke Laugenbehandlung in eine hydroxylreiche Titanat‑Phase um. Durch anschließendes Erhitzen dieses Materials an der Luft bei verschiedenen Temperaturen entfernen sie schrittweise Hydroxylgruppen und formen das Feststoffgefüge um. Bei 500 °C entsteht ein Träger (TiO2‑T‑500), der zwar mehr Hydroxyle aufweist als Standard‑TiO2, aber nicht mehr die röhrenförmige Gestalt hat, die dazu neigt, das Metall zu verbergen. Nach Auftrag von Platin und Einsatz des Katalysators bilden sich winzige metallische Cluster von etwa 2 Nanometern Durchmesser, die an der Oberfläche zugänglich bleiben.
Platin befähigen, CO besser zu binden
Mittels einer Reihe spektroskopischer Messungen zeigen die Forscher, dass diese zusätzlichen Oberflächenhydroxyle Platin nach einer Wasserstoffbehandlung stärker in einen metallischen Zustand (Pt0) treiben, verglichen mit dem stärker oxidierten Ptδ+‑Zustand auf gewöhnlichem TiO2. Metallisches Platin bindet CO stärker und aktiviert es leichter, was das Team durch Beobachtung des CO‑Adsorptions‑ und ‑Desorptionsverhaltens unter reaktionsähnlichen Bedingungen bestätigt. Auf dem hydroxylreichen Träger bleibt CO selbst nach langem Spülen an den Platinclustern haften und reagiert schneller mit zugeführtem Wasser zu CO2. Besonders aktiv sind Stellen in der Grenzfläche zwischen Platin und TiO2, was darauf hindeutet, dass sowohl Metall als auch Träger an den kritischen Schritten beteiligt sind.
Hydroxyle als opferbereite Helfer
Die Hydroxylgruppen auf TiO2 sind nicht nur passive Beobachter. Die Studie zeigt, dass CO diese Hydroxyle direkt verbrauchen kann, wodurch bereits vor dem eigentlichen Reaktionsgeschehen Wasserstoff und CO2 entstehen. Dabei werden Sauerstoffatome von der Oberfläche entfernt und es entstehen Sauerstoffvakanzstellen — fehlende Sauerstoffplätze, die als starke Anker zum Spalten neuer Wassermoleküle wirken. Raman‑, Infrarot‑ und Elektronenspinnmessungen liefern alle Hinweise auf einen starken Anstieg solcher Vakanzstellen im ingenieurmäßig veränderten Träger, sobald die Reaktion in Gang ist. Diese Defekte werden wieder aufgebaut und aufgefüllt, wenn Wasser fortlaufend gespalten wird, und verleihen dem Katalysator eine verbesserte Fähigkeit, H2O zu aktivieren, ohne den gesamten Reaktionsweg zu ändern.
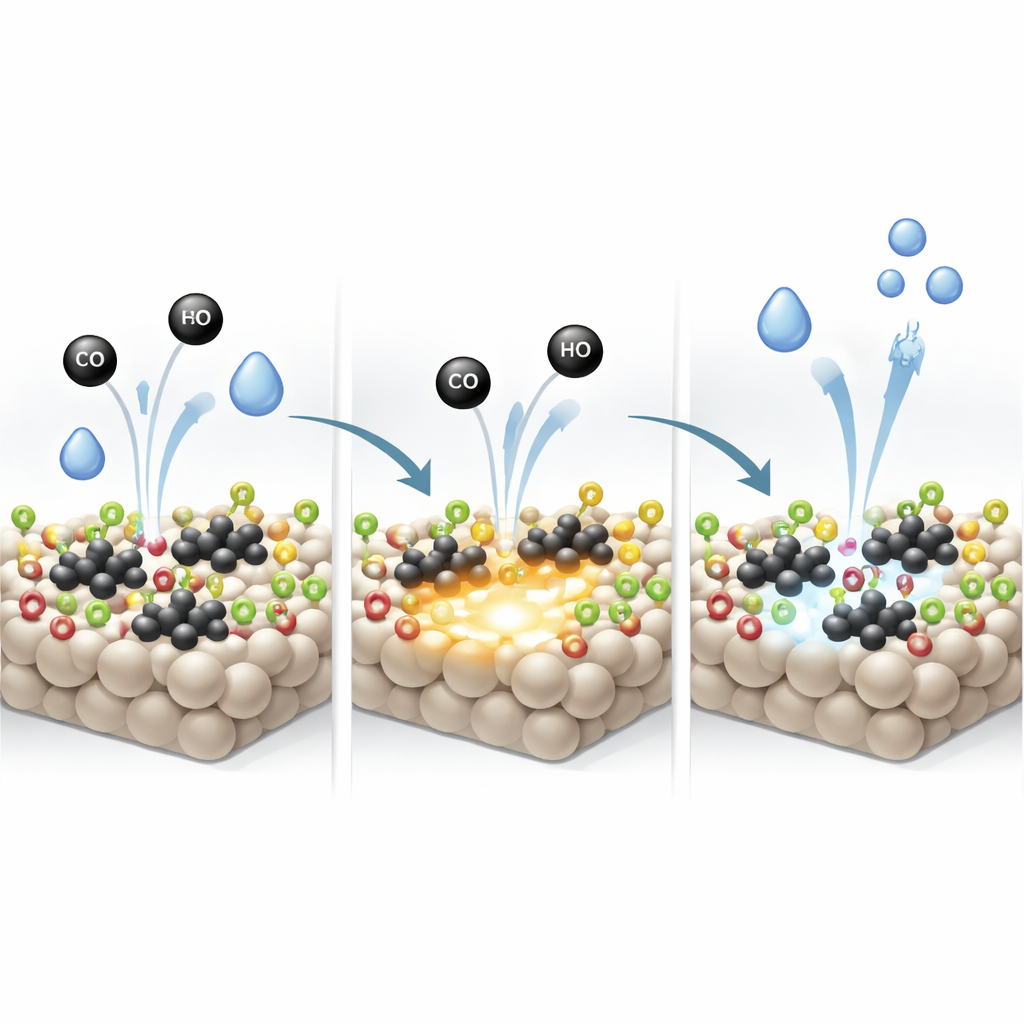
Schnellere Reaktion und anhaltende Stabilität
Weil der hydroxylreiche Träger zugleich die CO‑Aktivierung auf metallischem Platin und die Wasseraktivierung an Sauerstoffvakanzstellen verstärkt, wird die Gesamtleistung der Wasser‑Gas‑Shift‑Reaktion deutlich verbessert. Der optimierte Katalysator erreicht Reaktionsraten und Aktivität pro Wirkstelle, die etwa zwei- bis dreimal höher liegen als bei vergleichbaren Platin–Titanoxid‑Systemen in früheren Berichten, und erzielt bei 250 °C nahezu vollständige CO‑Umwandlung. Zudem bleibt er über mindestens 70 Stunden Dauerbetrieb stabil, ohne Leistungsverlust. Anschaulich haben die Forschenden einen Weg gefunden, genau die richtige Menge an Oberflächenhydroxylen einzustellen, sodass Platincluster und Oxidoberfläche zusammenwirken und ein vertrautes Material in einen deutlich leistungsfähigeren Motor für die saubere Wasserstoffproduktion verwandeln.
Zitation: Wang, CX., Wang, WW., Fu, XP. et al. Surface hydroxyl-induced Pt0 clusters on TiO2 for synergistic water gas shift catalysis. Nat Commun 17, 2757 (2026). https://doi.org/10.1038/s41467-026-69612-9
Schlüsselwörter: Wasser‑Gas‑Shift, Wasserstoffproduktion, Platin‑Katalysator, Titania‑Träger, Oberflächenhydroxylgruppen