Clear Sky Science · ru
Использование иммунной микроокружения: достижения в иммунотерапии носоглоточного карциномы
Почему это важно для повседневного здоровья
Носоглоточный карцином — это рак горла, который необычно часто встречается в некоторых регионах Азии и тесно связан с широко распространённым вирусом Эпштейна—Барр. Многие пациенты диагностируются только после распространения заболевания, и стандартная химио- и радиотерапия не помогают всем. В этой статье объясняется, как учёные учатся вновь вовлекать собственную иммунную систему организма в борьбу с этим раком, используя новые препараты, разумные комбинации методов лечения и лучшие тесты для подбора правильной терапии конкретному пациенту.
Рак, формируемый распространённым вирусом
Носоглоточный карцином развивается в труднодоступной зоне за носом, поэтому ранние симптомы часто остаются незамеченными. Почти все опухоли этого типа содержат скрытый вирус Эпштейна—Барр, который незаметно перепрограммирует инфицированные клетки. Вирус заставляет опухолевые клетки демонстрировать сигналы, которые подавляют атакующие иммунные клетки, скрывать ключевые «удостоверяющие» маркёры, используемые для иммунного распознавания, и привлекать другие клетки, ослабляющие иммунный ответ. Под микроскопом эти опухоли наполнены иммунными клетками, однако многие из них истощены или заблокированы. Это необычное сочетание высокого иммунного присутствия и сильного иммунного паралича делает болезнь одновременно сложной и идеальной для испытания новых иммунных методов лечения.
Преобразование иммунных «тормозов» в мишени терапии
Наиболее впечатляющие успехи достигнуты с препаратами, называемыми ингибиторами иммунных контрольных точек, которые снимают молекулярные «тормоза» с Т-клеток — главных борцов организма с раком. В крупных клинических исследованиях лекарства, блокирующие путь PD-1/PD-L1, в комбинации со стандартной химиотерапией увеличивали выживаемость и стали новым стандартом первой линии для пациентов с рецидивирующим или метастатическим заболеванием. Похожие препараты теперь применяют на более ранних стадиях болезни, сочетая с химиотерапией и точной радиотерапией для пациентов, у которых опухоль всё ещё ограничена областью головы и шеи, но имеет высокий риск прогрессирования. Ранние результаты показывают более высокие показатели полного ответа и более длительные периоды без рецидива, что указывает на то, что «перепрограммирование» иммунной системы до или во время облучения может углубить и стабилизировать контроль болезни. 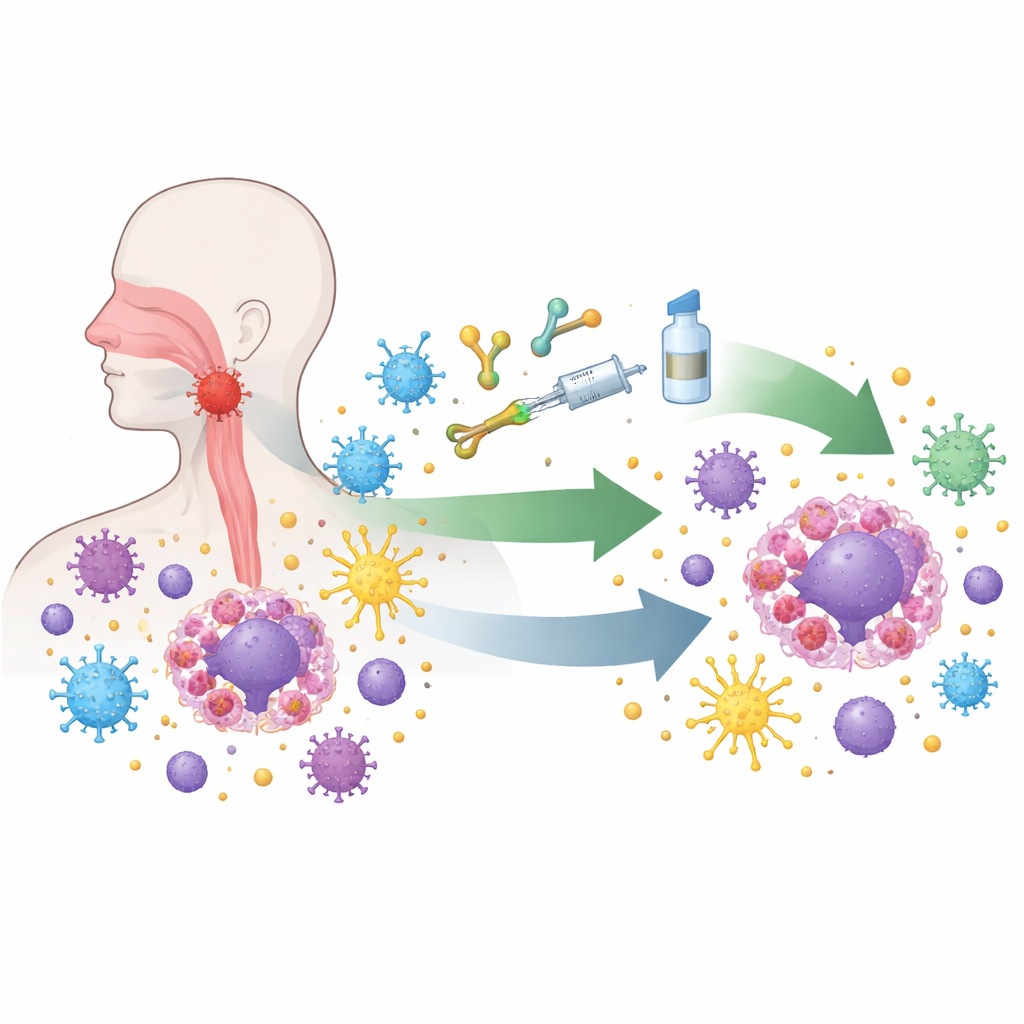
Сочетание сил для более сильного ответа
Поскольку вирус и микроокружение опухоли используют множество перекрывающихся приёмов для подавления иммунитета, одного препарата редко хватает. Исследователи испытывают биспецифические антитела, которые одновременно блокируют две контрольные точки, а также комбинации иммунотерапии с препаратами, направленными на рост сосудов, перестройку стромы опухоли или модуляцию метаболизма. Сама радиотерапия может действовать как вакцина на месте, вызывая гибель раковых клеток таким образом, что это привлекает внимание иммунных клеток; добавление ингибиторов контрольных точек может усилить этот эффект, особенно у пациентов с ограниченным числом метастазов. Для выбранных пациентов операция с последующей иммунотерапией или продолженное поддерживающее иммунное лечение после начальной химио–иммунотерапии может удерживать болезнь под контролем годами, хотя побочные эффекты и качество жизни требуют тщательного мониторинга.
Вакцины следующего поколения, клеточные терапии и умная диагностика
Поскольку вирус Эпштейна—Барр играет ключевую роль в этом раке, учёные разрабатывают вакцины и клеточные терапии, которые специфически распознают вирусные компоненты. Экспериментальные РНК-вакцины, кодирующие укороченные вирусные белки, часто в сочетании с естественными киллерными клетками или генетически модифицированными Т-клетками, показали сильные противоопухолевые эффекты в моделях на животных, хотя ранние крупные испытания на людях подчеркнули, насколько сложно перенести эти успехи в обычную клиническую практику. Параллельно возникает волна новых биомаркёров, призванных точнее направлять решения. Анализы крови, отслеживающие фрагменты вирусной ДНК, белки в крошечных везикулах или простые маркёры воспаления и холестерина, могут помочь оценить риск и следить за ответом на лечение. Продвинутая обработка изображений и искусственный интеллект, применяемые к рутинным сканам и срезам тканей, позволяют картировать иммунный ландшафт каждой опухоли, предсказывая, кто с наибольшей вероятностью извлечёт пользу из конкретной иммунотерапии и кому потребуются более агрессивные комбинации. 
Противостояние резистентности и персонализация ухода
Несмотря на эти достижения, многие опухоли либо изначально не отвечают на иммунотерапию, либо находят способы уйти от неё после первоначального ответа, часто под влиянием продолжающейся активности вируса в микроокружении опухоли. Авторы утверждают, что следующий качественный шаг будет связан с изучением этой меняющейся экосистемы на уровне отдельных клеток и в пространственной контексте и использованием этих данных для разработки более точных комбинаций, которые поражают несколько слабых мест, не перегружая при этом пациента побочными эффектами. Они представляют себе персонализированные схемы лечения, где вирусная нагрузка, шаблоны иммунных клеток, особенности визуализации и простые маркёры крови интегрируются с помощью искусственного интеллекта для выбора и коррекции терапии со временем. Для пациентов и клиницистов главный вывод таков: носоглоточный карцином трансформируется из заболевания, где доминируют химиотерапия и радиация, в состояние, где управление и направленное использование иммунной системы — в сочетании с опережающими манёврами против хитрого вируса — предлагают путь к более долгой и качественной жизни.
Цитирование: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
Ключевые слова: носоглоточный карцином, вирус Эпштейна—Барр, раковая иммунотерапия, ингибиторы иммунных контрольных точек, микроокружение опухоли