Clear Sky Science · pl
Wykorzystanie mikrośrodowiska odpornościowego: postępy w immunoterapii raka nosowo-gardłowego
Dlaczego to ma znaczenie dla zdrowia codziennego
Rak nosowo-gardłowy to nowotwór gardła, który występuje wyjątkowo często w niektórych rejonach Azji i jest silnie powiązany z powszechnym wirusem Epstein–Barra. Wiele przypadków rozpoznawanych jest dopiero po rozsiewie choroby, a standardowa chemioterapia i radioterapia nie pomagają wszystkim pacjentom. Artykuł wyjaśnia, jak naukowcy uczą się ponownie uruchamiać własny układ odpornościowy przeciw temu nowotworowi, stosując nowe leki, przemyślane kombinacje terapii oraz lepsze testy, by dopasować właściwe leczenie do właściwej osoby.
Nowotwór ukształtowany przez powszechny wirus
Rak nosowo-gardłowy rozwija się w trudno dostrzegalnym obszarze za nosem, dlatego wczesne objawy często są przeoczone. Niemal wszystkie guzy tego typu noszą utajonego wirusa Epstein–Barra, który po cichu przestawia program zakażonych komórek. Wirus powoduje, że komórki nowotworowe wystawiają sygnały wyłączające atakujące komórki odpornościowe, ukrywają kluczowe „identyfikatory” rozpoznawania immunologicznego i przyciągają inne komórki tłumiące odpowiedź immunologiczną. Pod mikroskopem te guzy są pełne komórek odpornościowych, a mimo to wiele z nich jest wyczerpanych lub zablokowanych. Ten dziwny miks silnej obecności komórek odpornościowych i zasadniczej ich paraliżu czyni chorobę zarówno wyzwaniem, jak i idealnym polem doświadczalnym dla nowych terapii opartych na odporności.
Przekształcanie hamulców odporności w cele terapeutyczne
Najbardziej dramatyczne postępy przyniosły leki zwane inhibitorami punktów kontrolnych, które zwalniają molekularne „hamulce” na limfocytach T, głównych żołnierzach organizmu zabijających komórki nowotworowe. W dużych badaniach klinicznych leki blokujące szlak PD-1/PD-L1, stosowane wraz ze standardową chemioterapią, wydłużyły przeżycie i stały się nowym leczeniem pierwszego wyboru u osób z nawrotowym lub przerzutowym schorzeniem. Podobne leki są teraz przesuwane wcześniej w przebiegu choroby, łączone z chemioterapią i precyzyjną radioterapią u pacjentów, których guzy nadal ograniczają się do okolicy głowy i szyi, ale znajdują się w grupie wysokiego ryzyka. Wstępne wyniki pokazują wyższe wskaźniki całkowitych odpowiedzi i dłuższe okresy bez wznowy, co sugeruje, że przywrócenie układu odpornościowego przed lub w trakcie radioterapii może pogłębić i ustabilizować kontrolę nad rakiem. 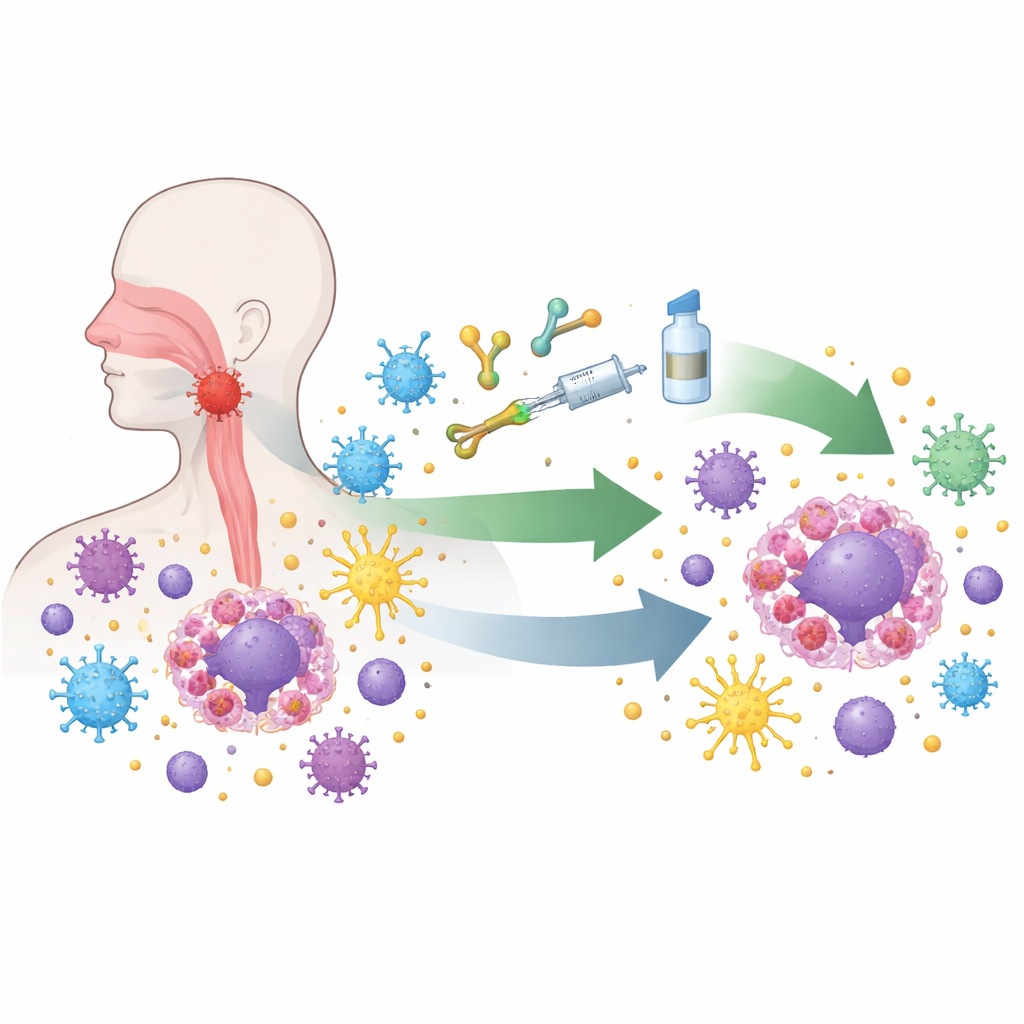
Łączenie sił dla silniejszych odpowiedzi
Ponieważ wirus i mikrośrodowisko guza stosują wiele nakładających się sztuczek tłumiących odporność, pojedyncze leki rzadko rozwiązują problem. Naukowcy testują przeciwciała dwukierunkowe, które blokują jednocześnie dwa punkty kontrolne, a także kombinacje immunoterapii z lekami hamującymi tworzenie naczyń, przebudowującymi tkankę podporową guza lub modulującymi metabolizm. Sama radioterapia może działać jak szczepionka in situ, powodując śmierć komórek nowotworowych w sposób, który alarmuje komórki odpornościowe; dodanie blokerów punktów kontrolnych może wzmocnić ten efekt, szczególnie u pacjentów z ograniczoną liczbą przerzutów. U wybranych pacjentów operacja, a następnie immunoterapia lub przedłużone leczenie podtrzymujące po początkowej chemo‑immunoterapii, może utrzymać chorobę pod kontrolą przez lata, choć efekty uboczne i jakość życia wymagają uważnego monitorowania.
Szczepionki nowej generacji, terapie komórkowe i inteligentne diagnostyki
Ponieważ wirus Epstein–Barra jest tak centralny dla tego nowotworu, naukowcy projektują szczepionki i terapie komórkowe rozpoznające specyficzne składniki wirusa. Eksperymentalne szczepionki mRNA kodujące uproszczone białka wirusowe, często łączone z komórkami NK lub zmodyfikowanymi limfocytami T, wykazywały silne efekty przeciwnowotworowe w modelach zwierzęcych, choć wczesne duże badania u ludzi uwypukliły, jak trudne jest przekształcenie tych wyników w rutynową opiekę. Równolegle pojawia się fala nowych biomarkerów mających precyzyjniej kierować decyzjami terapeutycznymi. Badania krwi śledzące fragmenty wirusowego DNA, białka przenoszone w malutkich pęcherzykach czy proste markery zapalne i lipidowe mogą pomagać w ocenie ryzyka i monitorowaniu odpowiedzi na leczenie. Zaawansowana analiza obrazowa i sztuczna inteligencja stosowane do rutynowych skanów i preparatów tkankowych potrafią odwzorować krajobraz immunologiczny każdego guza, przewidując, kto ma największe szanse skorzystać z określonej immunoterapii, a kto może potrzebować bardziej agresywnych kombinacji. 
Stawianie czoła oporności i personalizacja opieki
Mimo tych postępów wiele guzów albo nigdy nie reaguje na immunoterapię, albo znajduje sposoby ucieczki po początkowej odpowiedzi, często pod wpływem ciągłego oddziaływania wirusa na środowisko guza. Autorzy twierdzą, że następny duży krok naprzód będzie wynikał z rozumienia tego ewoluującego ekosystemu na poziomie pojedynczych komórek i w układzie przestrzennym oraz wykorzystania tej wiedzy do zaprojektowania „czystszych” kombinacji, które uderzają w wiele słabych punktów bez przytłaczania pacjenta działaniami niepożądanymi. Wyobrażają sobie spersonalizowane ścieżki leczenia, w których obciążenie wirusowe, wzorce komórek odpornościowych, cechy obrazowe i proste markery krwi są integrowane przez sztuczną inteligencję w celu wyboru i dostosowywania terapii w czasie. Dla pacjentów i klinicystów kluczowy wniosek jest taki, że rak nosowo-gardłowy przesuwa się od choroby zdominowanej przez chemioterapię i radioterapię w stronę podejścia, w którym wykorzystywanie i ukierunkowanie układu odpornościowego — przy jednoczesnym przechytrzeniu sprytnego wirusa — oferuje drogę do dłuższego i lepszego życia.
Cytowanie: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
Słowa kluczowe: rak nosowo-gardłowy, wirus Epsteina–Barra, immunoterapia nowotworów, inhibitory punktów kontrolnych odporności, mikrośrodowisko guza