Clear Sky Science · he
ניצול המיקרו-סביבה החיסונית: התקדמות באימונותרפיה של קרצינומה של האף-לוע
מדוע זה חשוב לבריאות היומיומית
קרצינומה של האף-לוע היא סוג של סרטן הלוע שכיח באופן יוצא דופן בחלקים מסוימים של אסיה ומקושר בקשר הדוק לוירוס נפוץ בשם וירוס אפשטיין–באר. רבים מהמטופלים מאובחנים רק לאחר שהמחלה התפשטה, וכימותרפיה וקרינת רנטגן סטנדרטיות אינן מועילות לכולם. מאמר זה מסביר כיצד מדענים לומדים להחזיר את מערכת החיסון של הגוף למאבק נגד סרטן זה, באמצעות תרופות חדשות, שילובים חכמים של טיפולים ובדיקות מדויקות יותר להתאמת הטיפול לאדם הנכון.
סרטן המעוצב על ידי וירוס שכיח
קרצינומה של האף-לוע מתפתחת באזור שקשה לראות מאחורי האף, ולכן התסמינים המוקדמים לעיתים קרובות מועטים או מתעלמים מהם. כמעט כל הגידולים מסוג זה נושאים את וירוס אפשטיין–באר בצורה סמויה, שמחדשת את פעילות התאים הנגועים. הווירוס גורם לתאי הגידול להציג אותות שמכבידים על תאי החיסון התוקפים, להסתיר תגי זיהוי חשובים לזיהוי חיסוני ולקרוא לתאים אחרים שמורידים את התגובה החיסונית. במיקרוסקופ, גידולים אלה מורכבים מתאי חיסון רבים, אך רבים מאלו מותשים או חסומים. התערובת המוזרה של נוכחות חיסונית כבדה ושיתוק חיסוני חזק הופכת את המחלה גם לאתגר וגם לשדה ניסוי אידיאלי לטיפולים מבוססי חיסון חדשים.
להפוך את הבלמים החיסוניים למטרות טיפול
ההתקדמות המרשימה ביותר הגיעה מתרופות המכונות מעכבי נקודות ביקורת חיסוניות, שמשחררות את ה"בלמים" המולקולריים על תאי T, הפועלים ככוחות ההרג העיקריים כנגד סרטן. בניסויים קליניים נרחבים, תרופות החוסמות את מסלול PD-1/PD-L1, כשנוספות לכימותרפיה הסטנדרטית, האריכו את ההישרדות והפכו לטיפול הקו הראשון החדש לאנשים עם מחלה חוזרת או גרורתית. תרופות דומות מועברות כעת מוקדם יותר במהלך המהלך של המחלה, בשילוב עם כימותרפיה ורדיוטרפיה מדויקת עבור חולים שגידוליהם עדיין מוגבלים לאזור הראש והצוואר אך נמצאים בסיכון גבוה. תוצאות מוקדמות מראות שיעורי תגובה מלאה גבוהים יותר ופרקי זמן ארוכים יותר ללא התפרצות מחודשת, ומרמזות כי איפוס מערכת החיסון לפני או במהלך הקרינה יכול להעמיק ולייצב את שליטת המחלה. 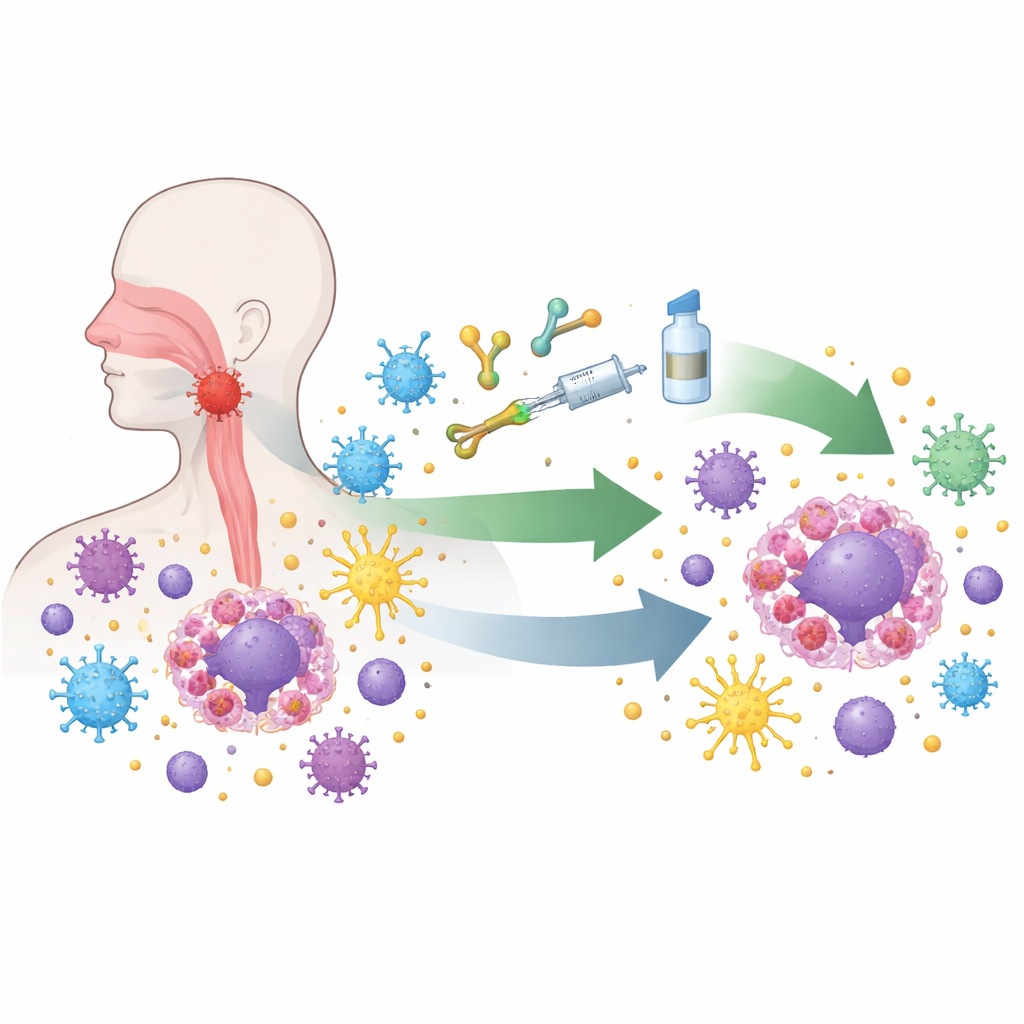
שילוב כוחות לתגובות חזקות יותר
מכיוון שהוירוס ומיקרו-הסביבה של הגידול משתמשים בהרבה תכסיסים חופפים לדיכוי המערכת החיסונית, תרופה בודדת לעיתים נדירות פותרת את הבעיה. חוקרים בודקים נוגדנים ביספציפיים הפוגעים בשתי נקודות ביקורת בו-זמנית, וכן שילובים של אימונותרפיה עם תרופות שמטרתן לצמצם גדילת כלי דם, לעצב מחדש את רקמת התמיכה של הגידול או למתן את המטבוליזם. הקרינה עצמה יכולה לפעול כחיסון מקומי על ידי גרימת מוות תאי באופן שמפעיל את תאי החיסון; הוספת מעכבי נקודות ביקורת יכולה להעצים אפקט זה, במיוחד בחולים עם מספר מוגבל של גרורות. עבור חולים נבחרים, ניתוח ואחריו אימונותרפיה או טיפול תחזוקתי ממושך אחרי כימו–אימונותרפיה יכולה לשמור על המחלה תחת שליטה במשך שנים, אם כי התופעות הלוואי ואיכות החיים מצריכות מעקב קפדני.
חיסונים מדור הבא, טיפולי תאים ואבחון חכם
מכיוון שוירוס אפשטיין–באר מרכזי בסרטן זה, מדענים מפתחים חיסונים וטיפולי תאים שמזהים באופן ספציפי רכיבים וירליים. חיסוני mRNA ניסיוניים המקודדים חלבוני וירוס מקוצצים, לעיתים בשילוב עם תאי הרג טבעיים או תאי T מהונדסים, הראו אפקטים אנטי-גידוליים חזקים במודלים של בעלי חיים, אם כי ניסויים אנושיים מוקדמים הראו כמה קושי לתרגם הישגים אלה לשגרת טיפול. במקביל, גל של ביומרקרים חדשים שואף להכווין החלטות ביתר דיוק. בדיקות דם שמעקבות חלקיקי DNA ויראלי, חלבונים הנשאים בשלפוחיות זעירות או סמנים פשוטים של דלקת וכולסטרול יכולות לסייע בהערכת סיכון ולעקוב אחרי תגובת הטיפול. ניתוח דימות מתקדם ובינה מלאכותית המיושמת על סריקות שגרתיות ופרוסות רקמה יכולים למפות את הנוף החיסוני של כל גידול, ולחזות מי צפוי להרוויח מאימונותרפיות מסוימות ומי עשוי להזדקק לשילובים אגרסיביים יותר. 
להתמודד עם עמידות ולהתאמת טיפול אישית
למרות ההתקדמות הזו, גידולים רבים או שאינם מגיבים כלל לאימונותרפיה או שמוצאים דרכים להימלט אחרי תגובה התחלתית, לעיתים בהשפעת הווירוס המשיכה על בית הגידול. המחברים טוענים שהקפיצה הבאה תבוא מהבנת המערכת האקולוגית המתפתחת הזו ברזולוציה של תא יחיד ומרחבית ושימוש בידע הזה לתכנן שילובים נקיים יותר שפוגעים בכמה נקודות תורפה בלי להציף את המטופל בתופעות לוואי. הם רואים מסלולי טיפול מותאמים אישית שבהם עומס ויראלי, דפוסי תאי חיסון, מאפייני דימות וסמנים דם פשוטים משתלבים על‑ידי בינה מלאכותית לבחירה והתאמת הטיפול לאורך זמן. עבור חולים ורופאים, המסקנה המרכזית היא שקרצינומה של האף-לוע משתנה מסרטן השולט בו בעיקר כימותרפיה וקרינה, אל גישה שבה ניצול והכוונת המערכת החיסונית—במקביל להתמודדות עם וירוס ערמומי—מציע דרך לחיים ארוכים ואיכותיים יותר.
ציטוט: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
מילות מפתח: קרצינומה של האף-לוע, וירוס אפשטיין–באר, אימונותרפיה של סרטן, מעכבי נקודות ביקורת חיסוניות, מיקרו-סביבת הגידול