Clear Sky Science · pt
Aproveitando o microambiente imune: avanços na imunoterapia do carcinoma nasofaríngeo
Por que isso importa para a saúde do dia a dia
O carcinoma nasofaríngeo é um câncer de garganta incomumente comum em certas regiões da Ásia e está fortemente ligado a um vírus disseminado chamado vírus Epstein–Barr. Muitos pacientes só são diagnosticados depois que a doença já se espalhou, e quimioterapia e radioterapia padrão não funcionam para todos. Este artigo explica como os cientistas estão aprendendo a reativar o próprio sistema imune do corpo contra esse câncer, usando novos medicamentos, combinações inteligentes de tratamentos e exames melhores para alinhar a terapia certa à pessoa certa.
Um câncer moldado por um vírus comum
O carcinoma nasofaríngeo cresce em uma área de difícil visualização atrás do nariz, portanto sintomas iniciais são frequentemente perdidos. Quase todos os tumores desse tipo carregam o vírus Epstein–Barr de forma latente, que silenciosamente reprograma as células infectadas. O vírus faz com que as células tumorais exibam sinais que desativam as células imunes atacantes, escondam etiquetas-chave usadas para o reconhecimento imune e recrutem outras células que atenuam as respostas imunes. Ao microscópio, esses tumores estão repletos de células imunes, mas muitas delas estão exaustas ou bloqueadas. Essa mistura estranha de forte presença imune e paralisação imune torna a doença ao mesmo tempo um desafio e um campo de prova ideal para novas terapias baseadas no sistema imune.
Transformando freios imunes em alvos terapêuticos
O progresso mais dramático veio de medicamentos chamados inibidores de checkpoint imunológico, que liberam os “freios” moleculares sobre os linfócitos T, os principais soldados do corpo na destruição do câncer. Em grandes ensaios clínicos, medicamentos que bloqueiam a via PD-1/PD-L1, quando adicionados à quimioterapia padrão, estenderam a sobrevida e se tornaram o novo tratamento de primeira linha para pessoas com doença recorrente ou metastática. Drogas semelhantes estão sendo usadas mais cedo no curso da doença, combinadas com quimioterapia e radioterapia precisa para pacientes cujos tumores ainda estão confinados à região da cabeça e pescoço, mas apresentam alto risco. Resultados iniciais mostram taxas mais altas de resposta completa e períodos mais longos sem recidiva, sugerindo que reiniciar o sistema imune antes ou durante a radioterapia pode aprofundar e estabilizar o controle do câncer. 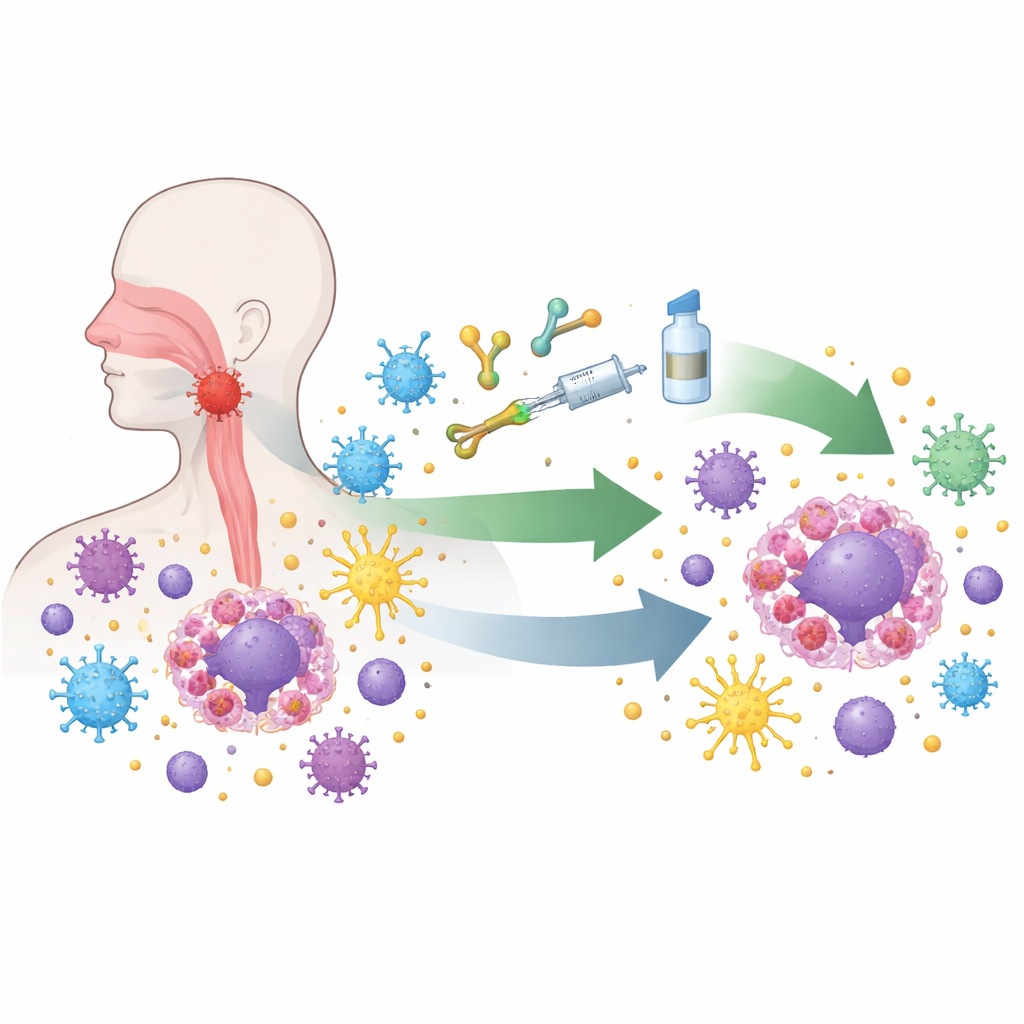
Combinando forças para respostas mais fortes
Como o vírus e o microambiente tumoral usam muitos artifícios sobrepostos para suprimir a imunidade, medicamentos isolados raramente resolvem o problema. Pesquisadores testam anticorpos biespecíficos que atingem dois checkpoints ao mesmo tempo, bem como combinações de imunoterapia com fármacos que atacam o crescimento de vasos sanguíneos, remodelam o tecido de suporte do tumor ou modulam o metabolismo. A própria radioterapia pode atuar como uma vacina in situ ao provocar a morte das células cancerosas de modo a alertar as células imunes; adicionar bloqueadores de checkpoint pode amplificar esse efeito, especialmente em pacientes com número limitado de metástases. Para pacientes selecionados, cirurgia seguida de imunoterapia ou tratamento imune de manutenção prolongado após quimio–imunoterapia inicial pode manter a doença controlada por anos, embora efeitos colaterais e qualidade de vida exijam monitoramento cuidadoso.
Vacinas de próxima geração, terapias celulares e diagnósticos inteligentes
Como o vírus Epstein–Barr é central nesse câncer, cientistas estão desenvolvendo vacinas e terapias celulares que reconhecem especificamente componentes virais. Vacinas experimentais de RNA mensageiro que codificam proteínas virais reduzidas, frequentemente combinadas com células natural killer ou linfócitos T geneticamente modificados, produziram fortes efeitos antitumorais em modelos animais, embora ensaios humanos grandes e iniciais tenham mostrado como é difícil traduzir esses ganhos para a prática clínica rotineira. Em paralelo, uma onda de novos biomarcadores busca orientar decisões com mais precisão. Testes sanguíneos que monitoram fragmentos de DNA viral, proteínas transportadas em pequenas vesículas, ou marcadores simples de inflamação e colesterol podem ajudar a estimar risco e acompanhar a resposta ao tratamento. Análises avançadas de imagem e inteligência artificial aplicadas a tomografias e lâminas de tecido de rotina podem mapear a paisagem imune de cada tumor, prevendo quem tem mais probabilidade de se beneficiar de imunoterapias específicas e quem pode precisar de combinações mais agressivas. 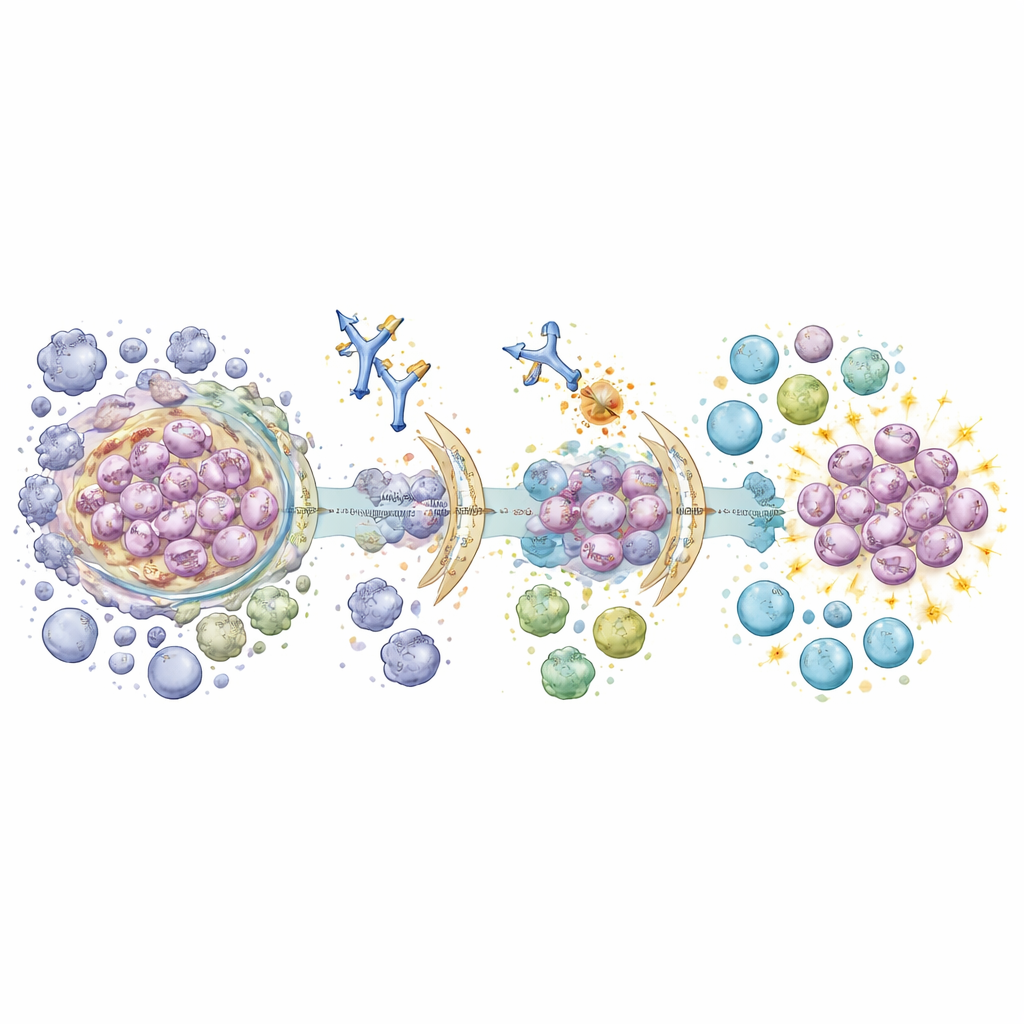
Enfrentando a resistência e personalizando o cuidado
Apesar desses avanços, muitos tumores ou não respondem nunca à imunoterapia ou encontram formas de escapar após uma resposta inicial, muitas vezes impulsionados pela influência contínua do vírus sobre o habitat tumoral. Os autores argumentam que o próximo salto virá do entendimento desse ecossistema em evolução em resolução de célula única e espacial e do uso desse conhecimento para projetar combinações mais limpas que atinjam múltiplos pontos fracos sem sobrecarregar o paciente com efeitos adversos. Eles imaginam vias de tratamento personalizadas nas quais carga viral, padrões de células imunes, características de imagem e marcadores sanguíneos simples sejam integrados por inteligência artificial para escolher e ajustar a terapia ao longo do tempo. Para pacientes e clínicos, a conclusão principal é que o carcinoma nasofaríngeo está mudando de um câncer dominado por quimioterapia e radioterapia para um em que aproveitar e guiar o sistema imune — enquanto se supera um vírus astuto — oferece um caminho para vidas mais longas e melhores.
Citação: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
Palavras-chave: carcinoma nasofaríngeo, vírus Epstein–Barr, imunoterapia contra o câncer, inibidores de checkpoint imunológico, microambiente tumoral