Clear Sky Science · fr
Exploiter le microenvironnement immunitaire : avancées de l’immunothérapie du carcinome nasopharyngé
Pourquoi cela compte pour la santé quotidienne
Le carcinome nasopharyngé est un cancer de la gorge exceptionnellement fréquent dans certaines régions d’Asie et étroitement lié à un virus répandu, le virus Epstein-Barr. De nombreux patients sont diagnostiqués seulement après que la maladie s’est propagée, et la chimiothérapie et la radiothérapie standard n’aident pas tout le monde. Cet article explique comment les scientifiques apprennent à réactiver le système immunitaire de l’organisme contre ce cancer, en utilisant de nouveaux médicaments, des associations de traitements réfléchies et de meilleurs tests pour associer la bonne thérapie à la bonne personne.
Un cancer modelé par un virus commun
Le carcinome nasopharyngé se développe dans une zone difficile à voir, derrière le nez, si bien que les symptômes précoces sont souvent manqués. Presque toutes les tumeurs de ce type contiennent le virus Epstein-Barr à l’état latent, qui reprogramme discrètement les cellules infectées. Le virus amène les cellules tumorales à afficher des signaux qui désactivent les cellules immunitaires attaquantes, à masquer des marqueurs essentiels pour la reconnaissance immunitaire et à attirer d’autres cellules qui atténuent les réponses immunitaires. Au microscope, ces tumeurs regorgent de cellules immunitaires, mais beaucoup d’entre elles sont épuisées ou bloquées. Ce mélange paradoxal d’une forte présence immunitaire et d’une paralysie immunitaire marquée rend la maladie à la fois problématique et un terrain d’essai idéal pour de nouvelles approches immunitaires.
Transformer les freins immunitaires en cibles thérapeutiques
Les progrès les plus spectaculaires proviennent des médicaments appelés inhibiteurs de points de contrôle immunitaire, qui libèrent les « freins » moléculaires des cellules T, les principaux soldats de l’organisme contre le cancer. Dans de larges essais cliniques, des médicaments bloquant la voie PD-1/PD-L1, ajoutés à la chimiothérapie standard, ont prolongé la survie et sont devenus le nouveau traitement de première intention pour les personnes atteintes de maladie récidivante ou métastatique. Des médicaments similaires sont désormais introduits plus tôt dans le cours de la maladie, en association avec la chimiothérapie et une radiothérapie ciblée pour les patients dont les tumeurs sont encore confinées à la tête et au cou mais présentent un haut risque. Les premiers résultats montrent des taux de réponse complète plus élevés et des périodes sans rechute prolongées, suggérant que réinitialiser le système immunitaire avant ou pendant la radiothérapie peut approfondir et stabiliser le contrôle de la tumeur. 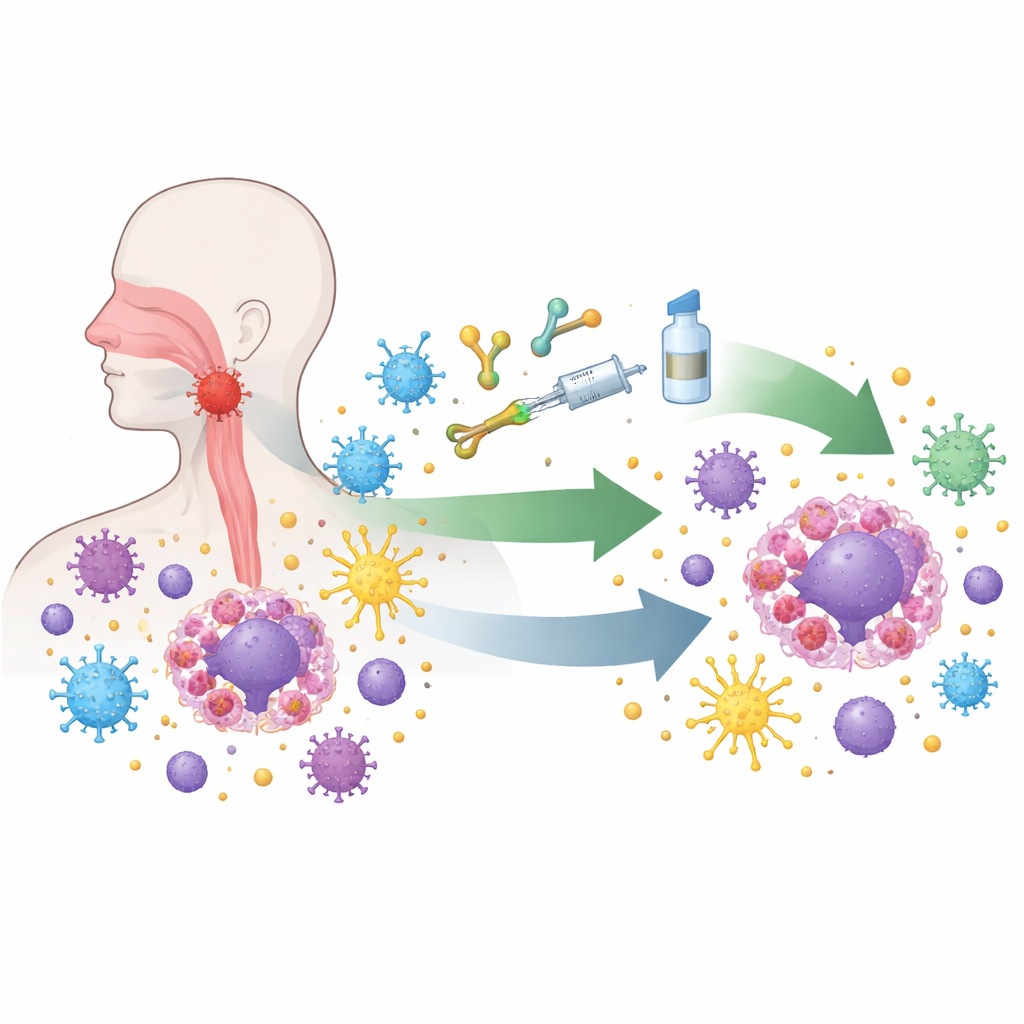
Combiner les forces pour des réponses plus fortes
Parce que le virus et le microenvironnement tumoral utilisent de nombreux mécanismes qui se recoupent pour supprimer l’immunité, un seul médicament résout rarement le problème. Les chercheurs testent des anticorps bispécifiques qui ciblent deux points de contrôle à la fois, ainsi que des combinaisons d’immunothérapie avec des médicaments qui ciblent la croissance des vaisseaux, reconfigurent le tissu de soutien tumoral ou modulent le métabolisme. La radiothérapie elle-même peut agir comme un vaccin in situ en provoquant la mort des cellules cancéreuses d’une manière qui alerte les cellules immunitaires ; l’ajout d’inhibiteurs de points de contrôle peut amplifier cet effet, en particulier chez les patients présentant un nombre limité de métastases. Pour des patients sélectionnés, la chirurgie suivie d’immunothérapie ou un traitement d’entretien immunitaire prolongé après une chimio-immunothérapie initiale peut maintenir la maladie sous contrôle pendant des années, bien que les effets secondaires et la qualité de vie nécessitent une surveillance attentive.
Vaccins de nouvelle génération, thérapies cellulaires et diagnostics intelligents
Parce que le virus Epstein-Barr est si central dans ce cancer, les chercheurs conçoivent des vaccins et des thérapies cellulaires qui reconnaissent spécifiquement des composants viraux. Des vaccins expérimentaux à ARN messager codant des protéines virales allégées, souvent combinés à des cellules tueuses naturelles ou à des cellules T génétiquement modifiées, ont produit de forts effets anti-tumoraux dans des modèles animaux, bien que de grands essais humains précoces aient montré la difficulté de traduire ces gains en soins de routine. Parallèlement, une vague de nouveaux biomarqueurs vise à guider les décisions de façon plus précise. Des tests sanguins qui suivent des fragments d’ADN viral, des protéines transportées dans de petites vésicules, ou des marqueurs simples d’inflammation et de cholestérol peuvent aider à estimer le risque et à suivre la réponse au traitement. L’analyse d’imagerie avancée et l’intelligence artificielle appliquées aux scans et aux lames de tissu courants peuvent cartographier le paysage immunitaire de chaque tumeur, prédisant qui bénéficiera le plus de quelles immunothérapies et qui peut nécessiter des combinaisons plus agressives. 
Faire face à la résistance et personnaliser les soins
Malgré ces avancées, de nombreuses tumeurs ne répondent jamais à l’immunothérapie ou trouvent des moyens d’échapper après une réponse initiale, souvent sous l’influence persistante du virus sur l’habitat tumoral. Les auteurs soutiennent que le prochain saut viendra de la compréhension de cet écosystème évolutif à résolution unicellulaire et spatiale et de l’utilisation de ces connaissances pour concevoir des combinaisons plus ciblées qui attaquent plusieurs points faibles sans submerger le patient d’effets indésirables. Ils envisagent des parcours de traitement personnalisés dans lesquels la charge virale, les profils de cellules immunitaires, les caractéristiques d’imagerie et des marqueurs sanguins simples sont intégrés par l’intelligence artificielle pour choisir et ajuster la thérapie au fil du temps. Pour les patients et les cliniciens, la conclusion clé est que le carcinome nasopharyngé évolue d’un cancer dominé par la chimiothérapie et la radiothérapie vers un modèle où exploiter et orienter le système immunitaire — tout en déjouant un virus astucieux — offre une voie vers des vies plus longues et de meilleure qualité.
Citation: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
Mots-clés: carcinome nasopharyngé, virus Epstein-Barr, immunothérapie du cancer, inhibiteurs de points de contrôle immunitaire, microenvironnement tumoral