Clear Sky Science · it
Sfruttare il microambiente immunitario: progressi nell’immunoterapia del carcinoma nasofaringeo
Perché questo è importante per la salute quotidiana
Il carcinoma nasofaringeo è un tumore della gola particolarmente comune in alcune aree dell’Asia ed è strettamente associato a un virus diffuso, il virus di Epstein–Barr. Molti pazienti vengono diagnosticati solo dopo che la malattia si è diffusa e la chemioterapia e la radioterapia standard non funzionano per tutti. Questo articolo spiega come gli scienziati stiano imparando a riattivare il sistema immunitario del corpo contro questo tumore, usando farmaci nuovi, combinazioni intelligenti di terapie e test migliori per abbinare la terapia giusta alla persona giusta.
Un cancro plasmato da un virus comune
Il carcinoma nasofaringeo cresce in una zona difficile da vedere dietro il naso, quindi i sintomi iniziali spesso vengono persi. Quasi tutti i tumori di questo tipo ospitano il virus di Epstein–Barr, che riorganizza silenziosamente le cellule infette. Il virus induce le cellule tumorali a esprimere segnali che bloccano le cellule immunitarie attaccanti, a nascondere marcatori chiave usati per il riconoscimento immunitario e ad attrarre altre cellule che attenuano la risposta immunitaria. Al microscopio, questi tumori sono pieni di cellule immunitarie, ma molte di queste sono esauste o bloccate. Questa combinazione insolita di forte presenza immunitaria e profonda paralisi immunitaria rende la malattia sia una sfida sia un terreno ideale per testare nuove terapie basate sul sistema immunitario.
Trasformare i freni immunitari in bersagli terapeutici
I progressi più spettacolari sono arrivati dai farmaci chiamati inibitori dei checkpoint immunitari, che rilasciano i “freni” molecolari sui linfociti T, i principali soldati dell’organismo contro il cancro. In grandi studi clinici, medicinali che bloccano la via PD-1/PD-L1, aggiunti alla chemioterapia standard, hanno prolungato la sopravvivenza e sono diventati il nuovo trattamento di prima linea per le persone con malattia ricorrente o metastatica. Farmaci simili vengono ora impiegati in fasi più precoci della malattia, in combinazione con chemioterapia e radioterapia mirata per pazienti i cui tumori sono ancora confinati alla regione testa-collo ma ad alto rischio. I primi risultati mostrano tassi di risposta completa più elevati e periodi più lunghi senza recidiva, suggerendo che ripristinare il sistema immunitario prima o durante la radioterapia può approfondire e stabilizzare il controllo del tumore. 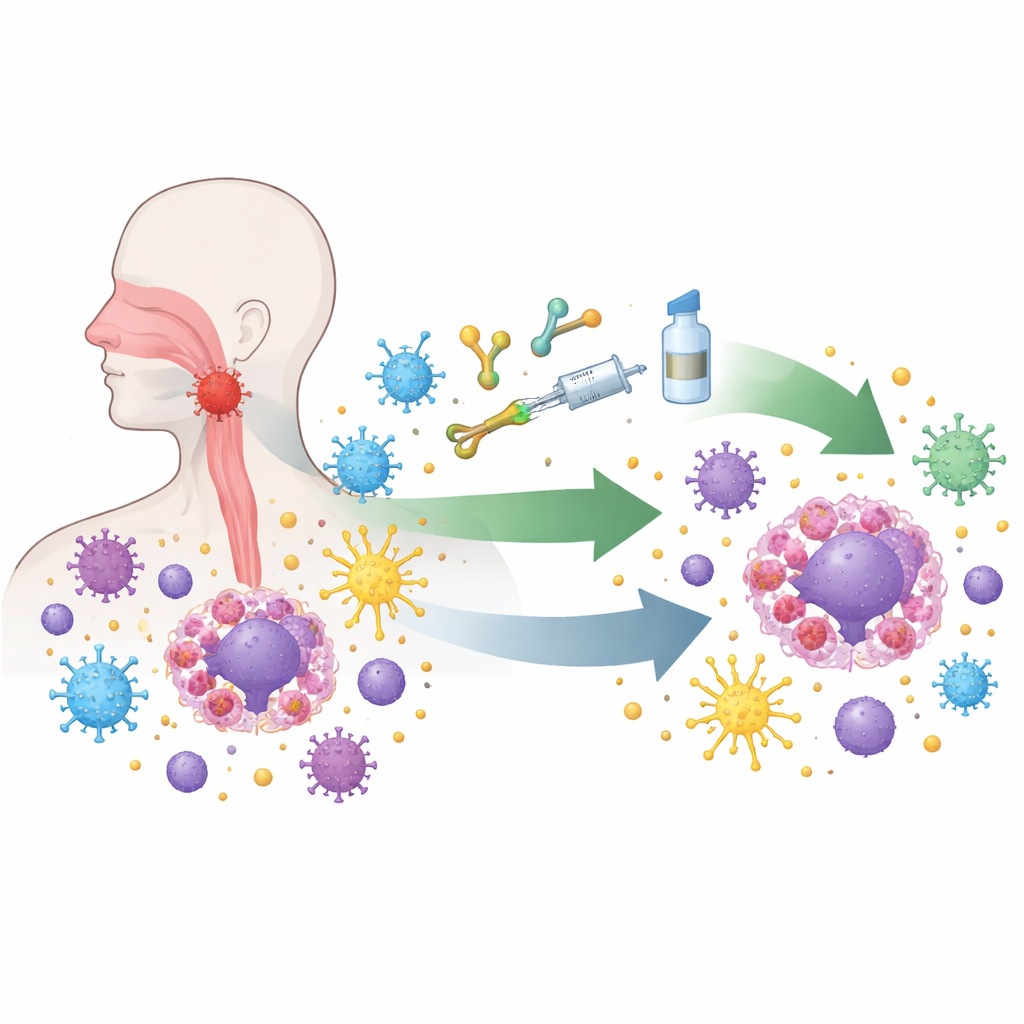
Combinare le forze per risposte più forti
Poiché il virus e il microambiente tumorale usano molti stratagemmi sovrapposti per sopprimere l’immunità, un singolo farmaco raramente risolve il problema. I ricercatori stanno testando anticorpi bispecifici che colpiscono due checkpoint contemporaneamente, così come combinazioni di immunoterapia con farmaci che mirano alla crescita dei vasi sanguigni, rimodellano il tessuto di supporto del tumore o modulano il metabolismo. La radioterapia stessa può agire come un vaccino in loco causando la morte delle cellule tumorali in modo che attiri le cellule immunitarie; l’aggiunta di bloccanti dei checkpoint può amplificare questo effetto, specialmente nei pazienti con un numero limitato di metastasi. Per pazienti selezionati, interventi chirurgici seguiti da immunoterapia o trattamenti di mantenimento immunitario prolungati dopo una chemioterapia–immunoterapia iniziale possono mantenere la malattia sotto controllo per anni, pur richiedendo un’attenta valutazione degli effetti collaterali e della qualità della vita.
Vaccini di nuova generazione, terapie cellulari e diagnostica intelligente
Poiché il virus di Epstein–Barr è centrale in questo tumore, gli scienziati stanno progettando vaccini e terapie cellulari che riconoscano specificamente componenti virali. Vaccini sperimentali a RNA messaggero che codificano proteine virali ridotte, spesso combinati con cellule natural killer o linfociti T ingegnerizzati, hanno prodotto forti effetti antitumorali nei modelli animali, anche se i primi grandi studi sull’uomo hanno evidenziato quanto sia difficile tradurre questi risultati in cure di routine. Parallelamente, una nuova ondata di biomarcatori mira a guidare le decisioni in modo più preciso. Test ematici che tracciano frammenti di DNA virale, proteine trasportate in minuscole vescicole o semplici marcatori di infiammazione e colesterolo possono aiutare a stimare il rischio e a seguire la risposta al trattamento. Analisi avanzate delle immagini e intelligenza artificiale applicate a scansioni di routine e vetrini tissutali possono mappare il paesaggio immunitario di ciascun tumore, prevedendo chi è più probabile che tragga beneficio da specifiche immunoterapie e chi potrebbe aver bisogno di combinazioni più aggressive. 
Affrontare la resistenza e personalizzare le cure
Nonostante questi progressi, molti tumori non rispondono mai all’immunoterapia o trovano modi per sfuggire dopo una risposta iniziale, spesso guidati dall’influenza persistente del virus sull’habitat tumorale. Gli autori sostengono che il prossimo salto in avanti deriverà dalla comprensione di questo ecosistema in evoluzione a risoluzione cellulare e spaziale e dall’uso di queste conoscenze per progettare combinazioni più pulite che colpiscano più punti deboli senza sovraccaricare il paziente con effetti avversi. Immaginano percorsi di cura su misura in cui carica virale, modelli di cellule immunitarie, caratteristiche di imaging e semplici marcatori ematici siano integrati da intelligenza artificiale per scegliere e adattare la terapia nel tempo. Per pazienti e clinici, il messaggio principale è che il carcinoma nasofaringeo sta passando da un cancro dominato da chemioterapia e radioterapia a uno in cui sfruttare e guidare il sistema immunitario—mentre si supera l’astuzia di un virus intelligente—offre una via verso vite più lunghe e migliori.
Citazione: Zhu, Y., Liu, Y., Yin, Z. et al. Harnessing the immune microenvironment: advances in nasopharyngeal carcinoma immunotherapy. Cell Death Discov. 12, 144 (2026). https://doi.org/10.1038/s41420-026-02999-y
Parole chiave: carcinoma nasofaringeo, virus di Epstein–Barr, immunoterapia oncologica, inibitori dei checkpoint immunitari, microambiente tumorale