Clear Sky Science · ru
Высвобождение митохондриальной ДНК через VDAC1 в кератиноцитах: ключевой фактор врожденного иммунитета и патогенеза витилиго
Почему эта история про кожу важна
Белые участки кожи при витилиго могут причинять серьёзное эмоциональное страдание, а существующие методы лечения часто действуют лишь частично и нередки рецидивы. В этом исследовании изучается неожиданный виновник внутри обычных клеток кожи — крошечные «электростанции» митохондрии. Авторы показывают, как стресс в этих структурах может инициировать сигналы тревоги, которые активируют иммунную систему и способствуют потере пигмента. Проследив эту цепочку шаг за шагом, они также указывают на новую терапевтическую идею, направленную не на иммунную систему напрямую, а на то, как клетки кожи первыми подают сигнал о помощи.
Клетки кожи как активные посланцы тревоги
Витилиго давно рассматривают как заболевание, при котором клетки иммунной системы ошибочно атакуют меланоциты — клетки, синтезирующие пигмент. Однако внешние клетки кожи — кератиноциты — по числу значительно превосходят меланоциты и всё чаще считаются ранними сторожами болезни. У людей с витилиго кожа испытывает высокий «окислительный стресс» — химическое напряжение, похожее на то, что возникает при сильном солнечном облучении или загрязнении. Кератиноциты в таком состоянии выделяют воспалительные медиаторы, привлекающие цитотоксические Т‑клетки в кожу. Ключевой вопрос, который задают авторы: что именно превращает этот химический стресс в мощный сигнал опасности, включающий антивирусный и воспалительный ответ организма?
Электростанции, которые одновременно служат маяками тревоги
Митохондрии содержат собственные маленькие кольца генетического материала — митохондриальную ДНК. Когда эта ДНК попадает в цитоплазму, иммунная система часто воспринимает её как вирусную или бактериальную. Исследователи показывают, что обработка кератиноцитов пероксидом водорода — классическим индуктором окислительного стресса — повреждает митохондрии, не убивая клетки сразу. Под микроскопом митохондрии деформируются, а фрагменты митохондриальной ДНК появляются за пределами органеллы, тогда как общий уровень митохондриальной ДНК в клетке остаётся примерно прежним. Эта утёкшая ДНК включает два мощных сенсорных пути, которые обычно охраняют от инфекций, что приводит к продукции интерферонов (белков, усиливающих иммунные ответы) и хемокинов (сигналов, привлекающих иммунные клетки). 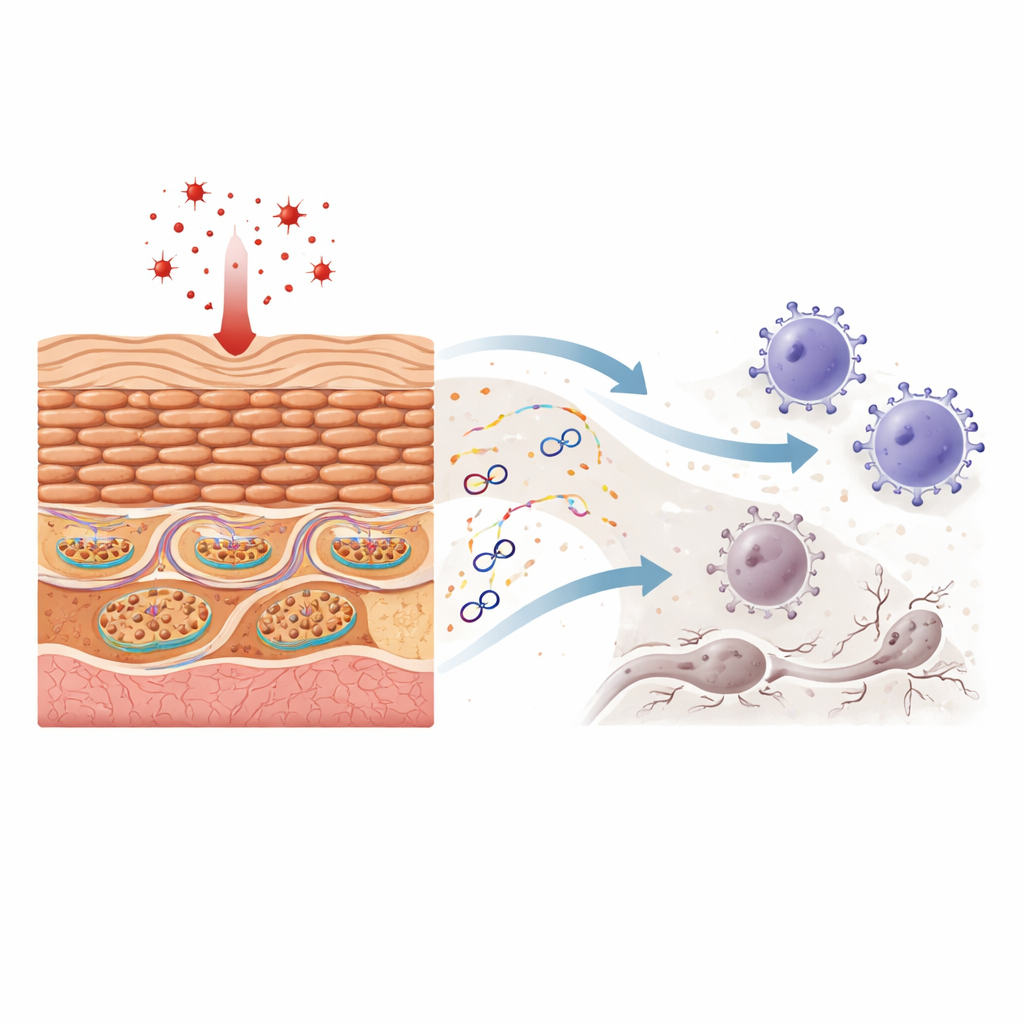
Как митохондриальная ДНК покидает свою «клетку»
Чтобы понять, как эта ДНК выходит наружу, авторы сосредоточились на двух воротах в митохондриальных мембранах. Одна — поровый комплекс проницаемости во внутренней мембране, который может открываться под стрессом. Другая — VDAC1, канал во внешней мембране, способный кластеризоваться в большие отверстия. С помощью красителей для живых клеток и молекулярных проб они показали, что окислительный стресс сначала открывает внутренний поровый путь, а затем способствует кластеризации VDAC1, при этом не активируя классические пути апоптоза. Блокирование внутреннего порового комплекса препятствует перемещению ДНК из матрикса митохондрии в межмембранное пространство, тогда как блокирование VDAC1 останавливает её переход через внешнюю мембрану в цитозоль. Оба вмешательства резко сокращают количество митохондриальной ДНК в цитоплазме, подтверждая пошаговый маршрут побега, зависящий от VDAC1.
От внутренней тревоги к огненному клеточному смерти
Дальше команда исследовала, достаточно ли самой утёкшей митохондриальной ДНК, чтобы активировать защиту кератиноцитов. При очищении этой ДНК и введении её прямо в кератиноциты она сильно активировала систему cGAS–STING — внутриклеточный детектор ДНК — и ещё один комплекс, называемый инфламмасомой. Вместе эти цепочки вызывали высокий уровень интерферонов и хемокинов и вели клетки к пироптозу — взрывной, воспалительной форме клеточной гибели, при которой в мембране образуются отверстия. Блокирование cGAS ослабляло эти ответы и снижало пироптоз, показывая, что путь распознавания ДНК лежит выше по каскаду воспалительных реакций. 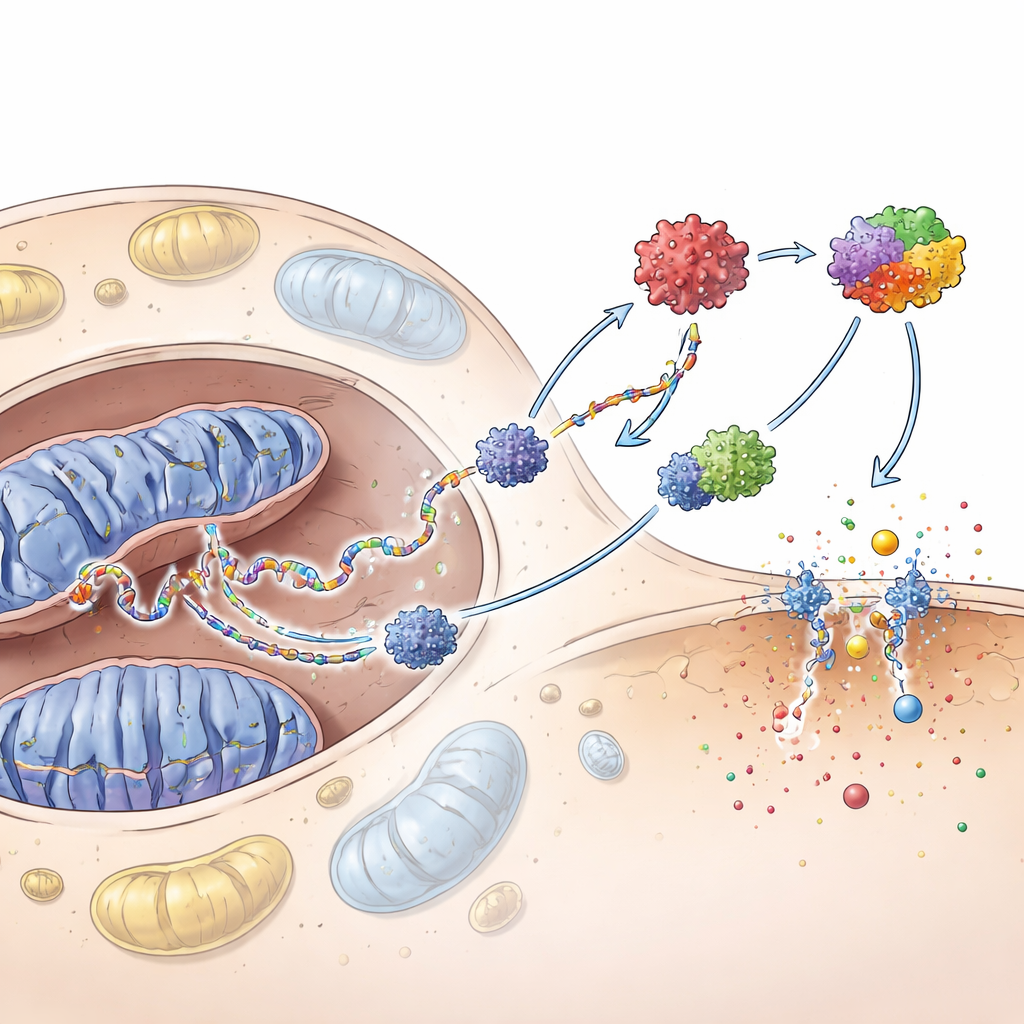
Закрыть врата, чтобы успокоить кожу
Поскольку VDAC1 действует как ключевая внешняя «врата» для утечки ДНК, исследователи проверили, поможет ли их закрыть в борьбе с проявлениями болезни. В культуре клеток небольшая молекула VBIT‑4, препятствующая кластеризации VDAC1, сократила высвобождение митохондриальной ДНК и ослабила активацию как cGAS–STING, так и инфламмасомы, снизив продукцию хемокинов. Подавление гена VDAC1 давало сходные эффекты. В мышиной модели витилиго, индуцированной нанесением пероксида водорода на кожу, животные, получавшие VBIT‑4, развивали меньше бледных участков, сохраняли больше меланоцитов и имели меньше CD8⁺ Т‑клеток в коже. В их коже также отмечались более низкие уровни воспалительных путей, связанных с митохондриальной ДНК.
Новый способ вмешаться на раннем этапе витилиго
Для неспециалиста вывод таков: обычные клетки кожи не просто наблюдают, пока иммунная система выходит из строя — они участвуют в начале конфликта. Под химическим стрессом их митохондрии протекают через VDAC1, и утёкшая ДНК действует как ложная сигнализация об инфекции. Этот сигнал пробуждает мощные антивирусные и воспалительные программы, привлекает агрессивные иммунные клетки и стимулирует разрушительные формы клеточной гибели, закладывая основу для потери пигмента. Нацеливание на «ворота» VDAC1, например с помощью препаратов типа VBIT‑4, может однажды приглушить эту тревогу в её источнике, предлагая способ замедлить или предотвратить витилиго до того, как произойдёт необратимое повреждение пигментных клеток.
Цитирование: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
Ключевые слова: витилиго, митохондриальная ДНК, кератиноциты, врожденный иммунитет, VDAC1