Clear Sky Science · ar
إطلاق الحمض النووي الميتوكوندري عبر VDAC1 في الخلايا الكيراتينية: محرك أساسي للمناعة الفطرية ومَرَض البحر الأبيض
لماذا تهم هذه القصة الجلدية
البقع البيضاء على الجلد الناجمة عن البِهاق قد تكون مُسببة لضيق كبير، ومع ذلك فإن العلاجات الحالية غالبًا ما تعمل جزئيًا فقط وتحدث نكسات متكررة. تبحث هذه الدراسة في سبب مفاجئ داخل خلايا الجلد العادية: محطات طاقة صغيرة تُدعى الميتوكوندريا. يبيّن المؤلفون كيف أن الإجهاد داخل هذه البُنى يمكن أن يطلق إشارة إنذار تُنبه جهاز المناعة وتساعد على دفع فقدان لون الجلد. من خلال تتبّع سلسلة الأحداث هذه خطوة بخطوة، يشيرون أيضًا إلى نوع جديد من العلاجات الذي لا يستهدف الجهاز المناعي نفسه، بل الطريقة التي تطلب بها خلايا الجلد المساعدة في المقام الأول.
الخلايا الجلدية كمرسلِات إنذار نشطات
طُرح البِهاق طويلاً على أنه مرض تهاجم فيه خلايا المناعة عن طريق الخطأ الخلايا المنتجة للصبغة، المسماة الخلايا الصِباغية. ومع ذلك، فإن الخلايا السطحية الأبعد—الخلايا الكيراتينية—تفوق الخلايا الصباغية عددًا وتُدرك بشكل متزايد كحارسات مبكرة في المرض. في الأشخاص المصابين بالبِهاق، يكون الجلد تحت "إجهاد تأكسدي" عالٍ، وهو ضغط كيميائي يشبه ما يحدث تحت ضوء الشمس القوي أو التلوث. الخلايا الكيراتينية تحت هذا الضغط تطلق رسائل التهابية تجذب خلايا T القاتلة إلى الجلد. والسؤال المحوري الذي يطرحه المؤلفون هو: ما الذي يحول بالضبط هذا الإجهاد الكيميائي إلى إشارة خطر قوية تُفعّل آليات الجسم المضادة للفيروسات والالتهابات؟
محطات طاقة تعمل كمنارات تحذير
تحمل الميتوكوندريا حلقات صغيرة من المادة الوراثية، هي الحمض النووي الميتوكوندري. عندما يهرب هذا الحمض النووي إلى جسد الخلية الرئيسي، يتعامل معه جهاز المناعة غالبًا كما لو كان فيروسًا أو بكتيريا. يبيّن الباحثون أن تعريض الخلايا الكيراتينية لبيروكسيد الهيدروجين—عامل إجهاد تأكسدي كلاسيكي—يُتلف الميتوكوندريا دون أن يقتل الخلايا تمامًا. تحت المجهر، تصبح بنية الميتوكوندريا مشوّهة، وتظهر قطع من الحمض النووي الميتوكوندري خارج العضية بينما يبقى مجموع الحمض النووي الميتوكوندري داخل الخلية تقريبًا ثابتًا. هذا الحمض النووي المتسرّب يُفعّل بعد ذلك نظامي استشعار قويين عادةً ما يحميان من العدوى، ما يؤدي إلى إنتاج الإنترفيرونات (بروتينات تُضخّم الاستجابات المناعية) والكيموكينات (إشارات تستدعي خلايا المناعة). 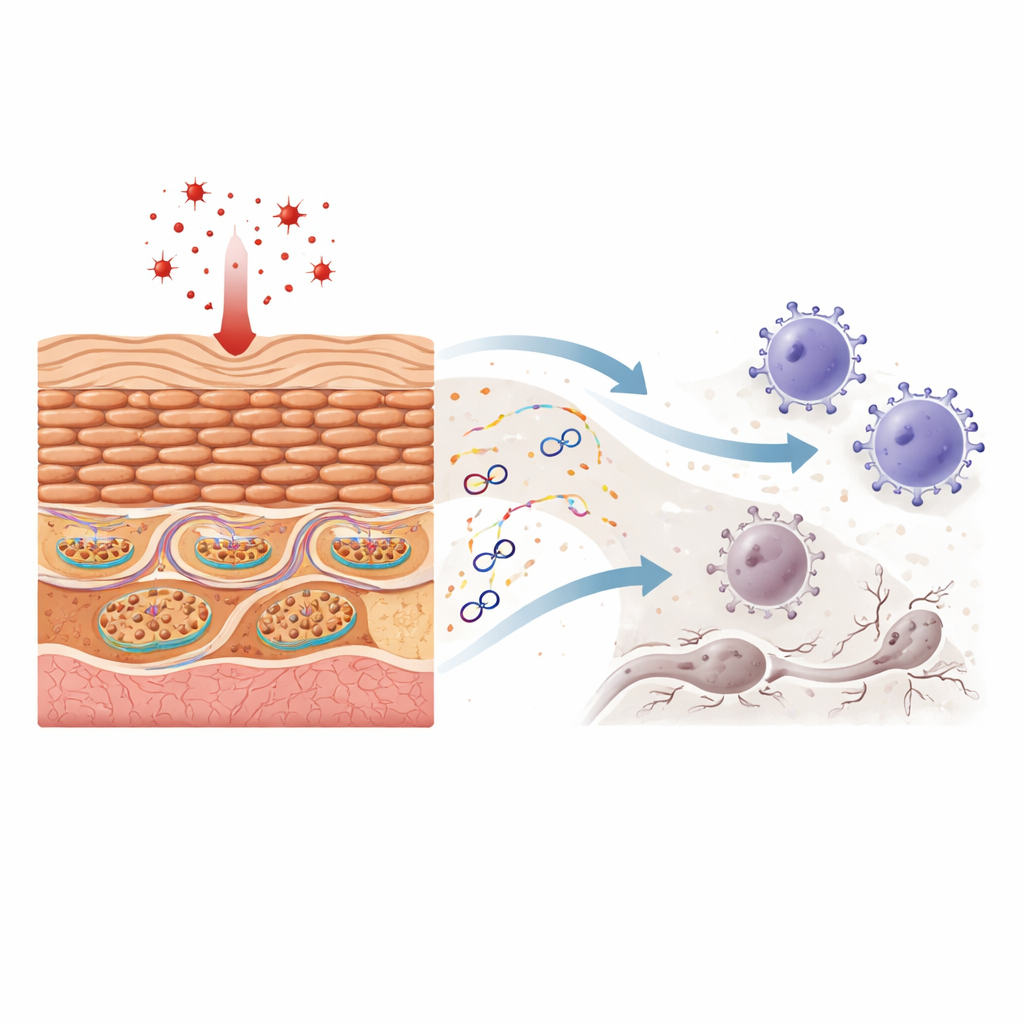
كيف يهرب الحمض النووي الميتوكوندري من قفصه
لفهم كيفية خروج هذا الحمض النووي، ركّز المؤلفون على بوابتين في أغشية الميتوكوندريا. إحداهما هي مسام النفاذية الانتقالية في الغشاء الداخلي، التي يمكن أن تفتح تحت الإجهاد. والأخرى هي VDAC1، قناة في الغشاء الخارجي يمكن أن تتجمّع لتكوّن فتحات أكبر. باستخدام صبغات للخلايا الحية ومجسات جزيئية، يُظهرون أن الإجهاد التأكسدي يفتح أولًا المسام الداخلية ثم يعزّز تجمّع VDAC1، وكل ذلك دون تحفيز مسارات انتحار الخلايا الكلاسيكية. حجب المسام الداخلية يمنع الحمض النووي من الانتقال من نواة الميتوكوندريا إلى الفراغ بين أغشيتها، بينما إيقاف VDAC1 يردع عبوره للحدود الخارجية إلى داخل الخلية. كلا التدخّلَين يقللان بشكل كبير من كمية الحمض النووي الميتوكوندري في السيتوسول، مؤكّدين مسار هروب تدريجي يعتمد على VDAC1.
من إنذار داخلي إلى موت خلوي متقدّم وملتهب
سأل الفريق بعد ذلك ما إذا كان الحمض النووي الميتوكوندري الضال بحد ذاته كافياً لتفعيل دفاعات الخلايا الكيراتينية. عندما نقّوا هذا الحمض النووي وأدخلوه مباشرة إلى الخلايا الكيراتينية، فعّل بقوة نظام cGAS–STING—كاشف داخلي للحمض النووي—ومعقّداً آخر يُسمى الإنفلاماسوم. معًا دفعت هذه الدوائر إلى مستويات عالية من الإنترفيرونات والكيموكينات ودفعت الخلايا نحو البيروبتوز، وهو شكل متفجّر وملتهب من موت الخلايا يخرّب غشاء الخلية. إيقاف cGAS خفّض هذه الاستجابات وقلّل البيروبتوز، ما يظهر أن هذا المسار المستشعر للحمض النووي يقع أعلى كثير من التسلسل الالتهابي. 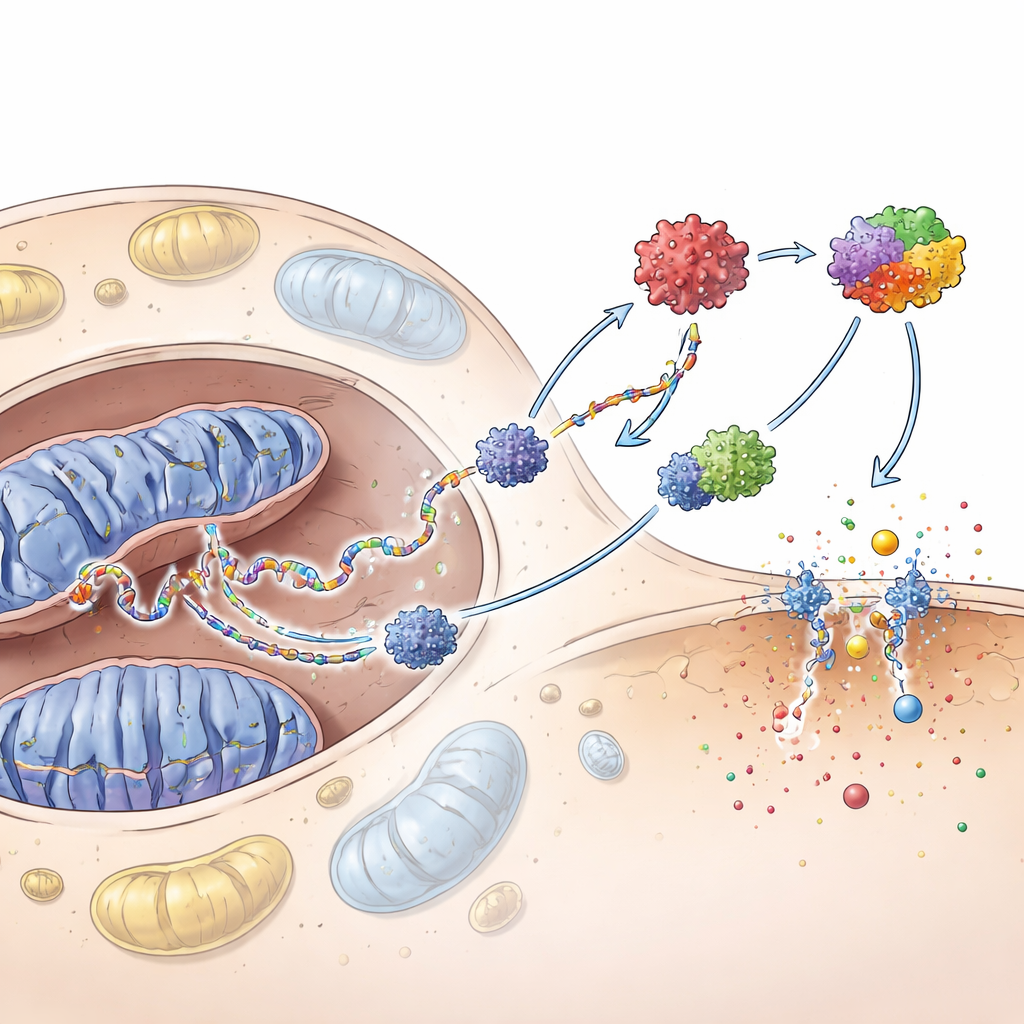
إغلاق البوابة لتهدئة الجلد
نظرًا لأن VDAC1 يعمل كبوابة خارجية رئيسية لهروب الحمض النووي، اختبر الباحثون ما إذا كان إغلاق هذه البوابة يمكن أن يخفّف علامات المرض. في زراعة الخلايا، جزئ صغير يُدعى VBIT‑4، والذي يمنع تجمّع VDAC1، خفّض إطلاق الحمض النووي الميتوكوندري وقلّل تفعيل كل من cGAS–STING والإنفلاماسوم، مما خفّض إنتاج الكيموكينات. إسكات جين VDAC1 أعطى تأثيرات مماثلة. في نموذج فأري للبِهاق مُستثار بواسطة تطبيق بيروكسيد الهيدروجين على الجلد، طورت الحيوانات المعالجة بـVBIT‑4 بقعًا شاحبة أقل، واحتفظت بعدد أكبر من الخلايا الصباغية، وأظهرت عددًا أقل من خلايا CD8⁺ في الجلد. كما عرض جلدها مستويات أدنى من المسارات الالتهابية المرتبطة بالحمض النووي الميتوكوندري.
طريقة جديدة لاعتراض البِهاق مبكّرًا
بالنسبة لغير المتخصص، الخلاصة هي أن خلايا الجلد العادية لا تبقى مكتوفة الأيدي بينما ينقلب جهاز المناعة—بل تساهم في بدء المشكلة. تحت الإجهاد الكيميائي، تتسرّب مكوّنات من حمضها النووي الميتوكوندري عبر "بوابات" VDAC1، ويعمل هذا الحمض النووي المتسرّب كإنذار إصابة زائفة. هذا الإنذار يوقظ برامج قوية مضادة للفيروسات والالتهابات، ويجذب خلايا مناعية عدوانية، ويعزّز أشكالًا مدمّرة من موت الخلايا، مما يمهّد الطريق لفقدان الصبغة. باستهداف بوابة VDAC1، قد تتمكن أدوية مثل VBIT‑4 يومًا ما من إسكات هذا الإنذار عند مصدره، مما يوفر وسيلة لإبطاء أو منع البِهاق قبل حصول ضرر دائم للخلايا الصباغية.
الاستشهاد: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
الكلمات المفتاحية: البِهاق, الحمض النووي الميتوكوندري, الخلايا الكيراتينية, المناعة الفطرية, VDAC1