Clear Sky Science · pt
Liberação de DNA mitocondrial via VDAC1 em queratinócitos: um motor-chave da imunidade inata e da patogênese do vitiligo
Por que essa história da pele importa
As manchas brancas na pele causadas pelo vitiligo podem ser profundamente angustiantes, mas os tratamentos atuais frequentemente têm eficácia parcial e recaídas são comuns. Este estudo investiga um culpado surpreendente dentro de células cutâneas comuns: pequenas usinas de energia chamadas mitocôndrias. Os autores mostram como o estresse nessas estruturas pode disparar um sinal de alarme que desperta o sistema imunológico e contribui para a perda da pigmentação. Ao rastrear essa cadeia de eventos passo a passo, eles também apontam para um novo tipo de terapia que não mira diretamente o sistema imune, mas sim a forma como as células da pele primeiro pedem socorro.
Células da pele como emissoras ativas de alarme
O vitiligo há muito é visto como uma doença em que células imunes atacam equivocadamente as células produtoras de pigmento, os melanócitos. Entretanto, as células mais externas da pele — os queratinócitos — superam em número os melanócitos e são cada vez mais reconhecidas como sentinelas iniciais da doença. Em pessoas com vitiligo, a pele sofre alto “estresse oxidativo”, uma tensão química semelhante ao que ocorre sob luz solar intensa ou poluição. Queratinócitos sob esse estresse liberam mensageiros inflamatórios que atraem células T citotóxicas para a pele. A pergunta central que os autores colocam é: o que exatamente converte esse estresse químico em um sinal de perigo poderoso que liga as máquinas antivirais e inflamatórias do corpo?
Usinas de energia que também servem de faróis de aviso
As mitocôndrias carregam seus próprios pequenos anéis de material genético, o DNA mitocondrial. Quando esse DNA escapa para o corpo celular, o sistema imune frequentemente o trata como se fosse viral ou bacteriano. Os pesquisadores mostram que expor queratinócitos ao peróxido de hidrogênio — um agente clássico de estresse oxidativo — danifica as mitocôndrias sem matar imediatamente as células. Ao microscópio, a estrutura mitocondrial fica distorcida e fragmentos de DNA mitocondrial surgem fora do orgânulo, enquanto a quantidade total de DNA mitocondrial dentro da célula se mantém aproximadamente constante. Esse DNA vazado então ativa dois sistemas sensores poderosos que normalmente defendem contra infecções, levando à produção de interferons (proteínas que amplificam respostas imunes) e quimiocinas (sinais que recrutam células imunes). 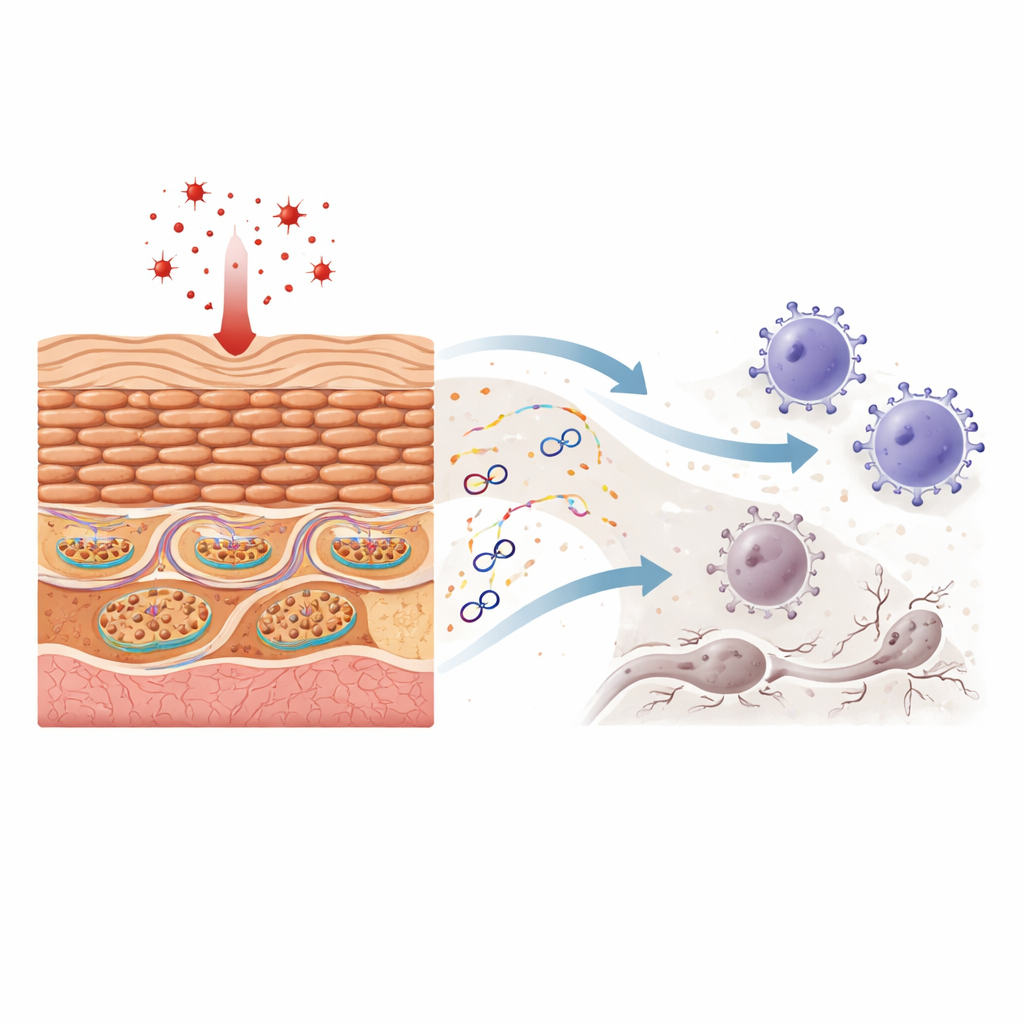
Como o DNA mitocondrial escapa de sua gaiola
Para entender como esse DNA sai, os autores se concentram em dois portais nas membranas mitocondriais. Um é o poro de transição de permeabilidade na membrana interna, que pode se abrir sob estresse. O outro é o VDAC1, um canal na membrana externa que pode se agrupar formando aberturas maiores. Usando corantes em células vivas e sondas moleculares, mostram que o estresse oxidativo primeiro abre o poro interno e depois promove o agrupamento do VDAC1, tudo isso sem disparar as vias clássicas de suicídio celular. Bloquear o poro interno impede que o DNA se mova do núcleo mitocondrial para o espaço entre as membranas, enquanto bloquear o VDAC1 o impede de atravessar a fronteira externa rumo ao citosol. Ambas as intervenções reduzem drasticamente a quantidade de DNA mitocondrial no citosol, confirmando uma rota de escape em etapas que depende do VDAC1.
Do alarme interno à morte celular inflamatória
A equipe então investigou se o DNA mitocondrial extraviado por si só é suficiente para ativar defesas dos queratinócitos. Quando purificaram esse DNA e o introduziram diretamente nos queratinócitos, ele ativou fortemente o sistema cGAS–STING — um detector interno de DNA — e outro complexo chamado inflamasoma. Juntos, esses circuitos impulsionaram altos níveis de interferons e quimiocinas e induziram piroptose, uma forma explosiva e inflamatória de morte celular que perfura a membrana celular. Bloquear o cGAS atenuou essas respostas e reduziu a piroptose, mostrando que essa via de detecção de DNA está a montante de grande parte da cascata inflamatória. 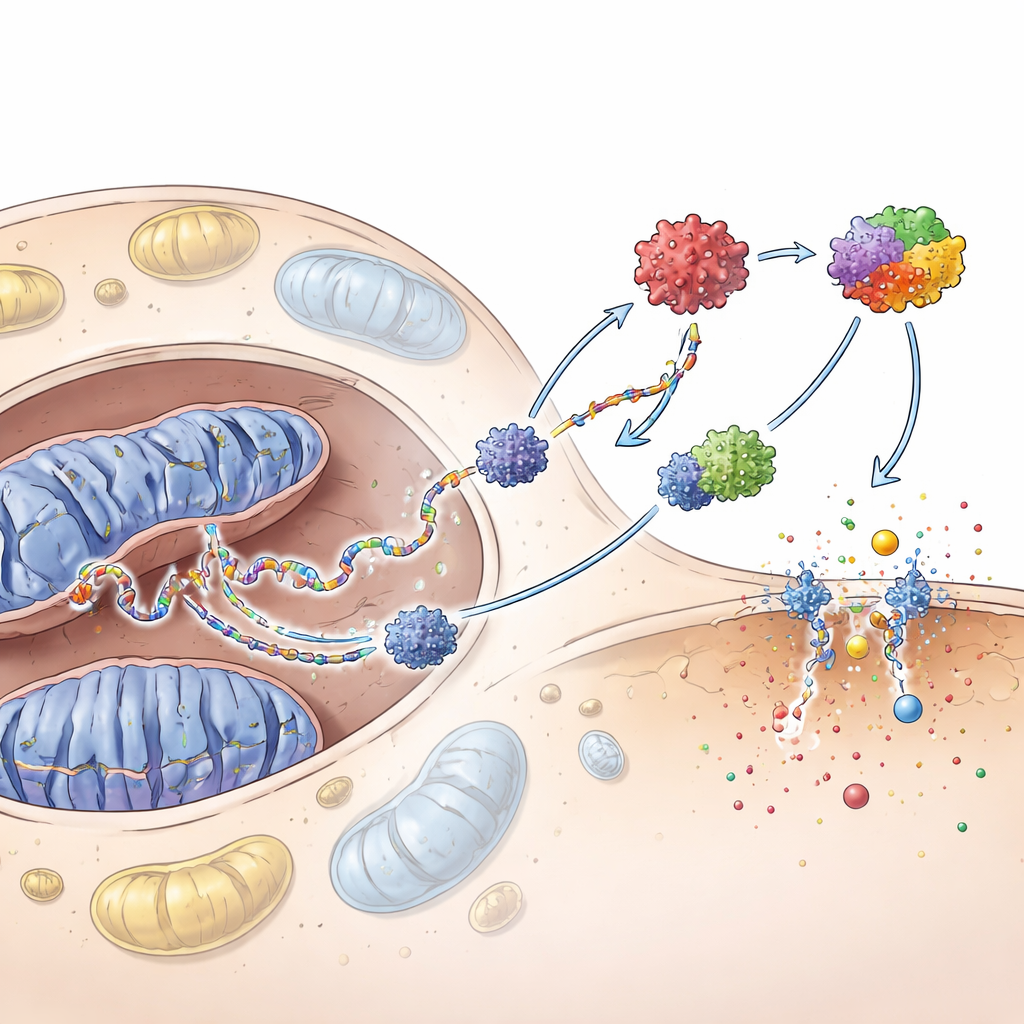
Fechando o portão para acalmar a pele
Porque o VDAC1 funciona como um portão externo crucial para o escape do DNA, os pesquisadores testaram se fechar esse portão poderia aliviar os sinais da doença. Em cultura celular, uma pequena molécula chamada VBIT‑4, que impede o agrupamento do VDAC1, reduziu a liberação de DNA mitocondrial e debilitou a ativação tanto do cGAS–STING quanto do inflamasoma, diminuindo a produção de quimiocinas. Silenciar o gene VDAC1 teve efeitos semelhantes. Em um modelo murino de vitiligo induzido por aplicação cutânea de peróxido de hidrogênio, animais tratados com VBIT‑4 desenvolveram menos manchas pálidas, mantiveram mais melanócitos e exibiram menos células CD8⁺ na pele. A pele desses animais também mostrou níveis mais baixos das vias inflamatórias relacionadas ao DNA mitocondrial.
Uma nova forma de interceptar o vitiligo cedo
Para o não especialista, a conclusão é que células comuns da pele não ficam passivas enquanto o sistema imune se descontrola — elas ajudam a iniciar o problema. Sob estresse químico, suas mitocôndrias vazam fragmentos de DNA através dos “portões” VDAC1, e esse DNA vazado age como um falso alarme de infecção. Esse alarme desperta programas antivirais e inflamatórios poderosos, atrai células imunes agressivas e promove formas destrutivas de morte celular, preparando o terreno para a perda de pigmento. Ao visar o portão VDAC1, fármacos como o VBIT‑4 podem, um dia, silenciar esse alarme na sua origem, oferecendo uma forma de retardar ou prevenir o vitiligo antes que ocorram danos duradouros às células produtoras de pigmento.
Citação: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
Palavras-chave: vitiligo, DNA mitocondrial, queratinócitos, imunidade inata, VDAC1