Clear Sky Science · it
Rilascio di DNA mitocondriale tramite VDAC1 nei cheratinociti: un motore chiave dell’immunità innata e della patogenesi della vitiligine
Perché questa storia cutanea conta
Le chiazze bianche della pelle causate dalla vitiligine possono essere profondamente angoscianti, ma i trattamenti attuali spesso funzionano solo parzialmente e le recidive sono comuni. Questo studio indaga un colpevole sorprendente all’interno delle cellule cutanee ordinarie: piccole centrali energetiche chiamate mitocondri. Gli autori mostrano come lo stress all’interno di queste strutture possa innescare un segnale d’allarme che attiva il sistema immunitario e contribuisce alla perdita del pigmento cutaneo. Tracciando questa catena di eventi passo dopo passo, indicano anche un nuovo tipo di terapia che non mira al sistema immunitario in sé, ma al modo in cui le cellule della pelle chiedono aiuto all’inizio del processo.
Le cellule della pelle come inviatori attivi di allarmi
La vitiligine è stata a lungo vista come una malattia in cui le cellule immunitarie attaccano erroneamente le cellule produttrici di pigmento, i melanociti. Tuttavia, le cellule più esterne della pelle — i cheratinociti — sono molto più numerose dei melanociti e sono sempre più riconosciute come sentinelle precoci della malattia. Nelle persone con vitiligine, la pelle è sottoposta a un alto “stress ossidativo”, una tensione chimica simile a quella indotta da luce solare intensa o inquinamento. I cheratinociti sottoposti a questo stress rilasciano messaggeri infiammatori che attirano cellule T citotossiche nella pelle. La domanda chiave che gli autori si pongono è: cosa trasforma esattamente questo stress chimico in un potente segnale di pericolo che attiva la macchina antivirale e infiammatoria del corpo?
Centrali energetiche che fungono anche da segnali di allerta
I mitocondri portano con sé piccoli anelli di materiale genetico, il DNA mitocondriale. Quando questo DNA sfugge nel citoplasma della cellula, il sistema immunitario lo tratta spesso come se fosse virale o batterico. I ricercatori mostrano che l’esposizione dei cheratinociti al perossido d’idrogeno — un classico agente di stress ossidativo — danneggia i mitocondri senza uccidere le cellule. Al microscopio, la struttura mitocondriale diventa distorta e frammenti di DNA mitocondriale compaiono all’esterno dell’organello mentre la quantità totale di DNA mitocondriale nella cellula rimane grosso modo costante. Questo DNA fuoriuscito attiva quindi due potenti sistemi sensori che normalmente difendono contro le infezioni, portando alla produzione di interferoni (proteine che amplificano le risposte immunitarie) e chemiochine (segnali che richiamano cellule immunitarie). 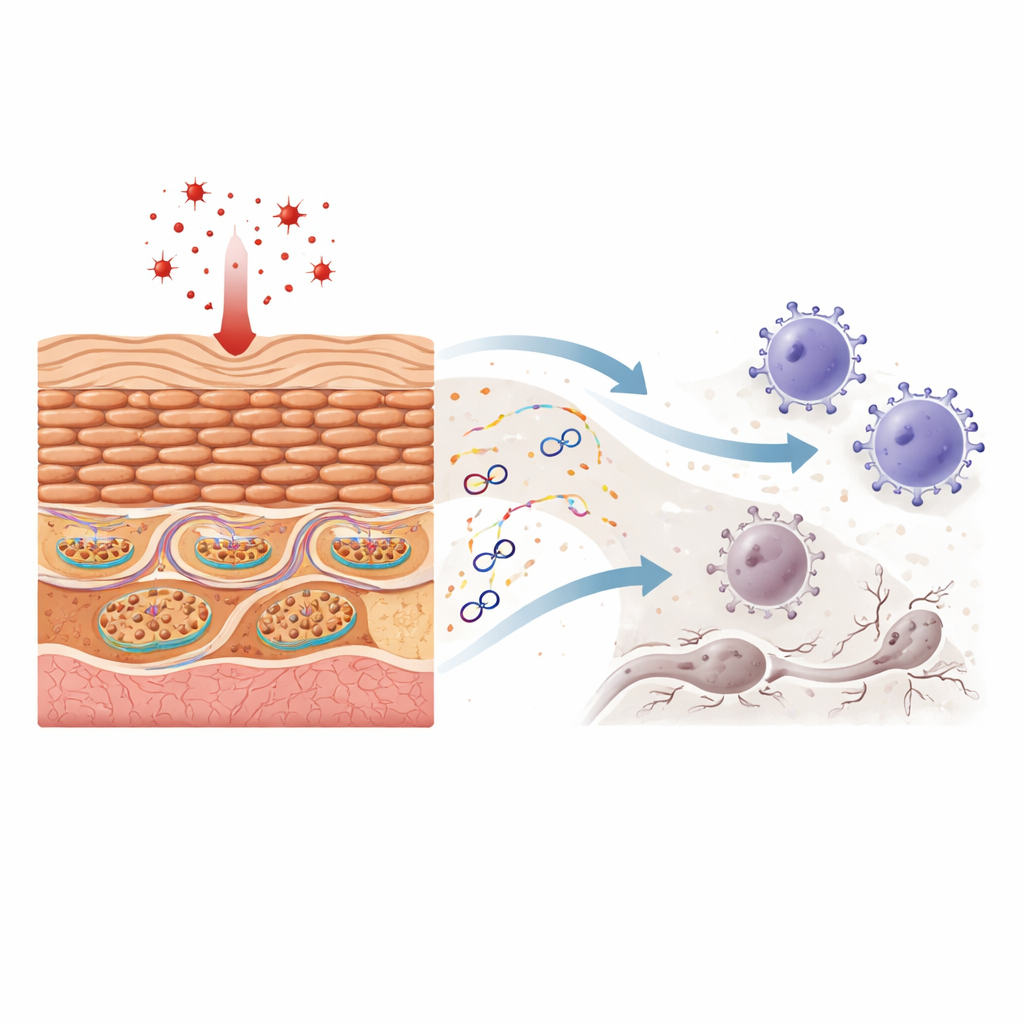
Come il DNA mitocondriale scappa dalla sua gabbia
Per capire come questo DNA esca, gli autori si concentrano su due passaggi nelle membrane mitocondriali. Uno è il poro di transizione della permeabilità nella membrana interna, che può aprirsi sotto stress. L’altro è VDAC1, un canale nella membrana esterna che può aggregarsi in aperture più grandi. Utilizzando coloranti per cellule vive e sonde molecolari, mostrano che lo stress ossidativo apre prima il poro interno e poi favorisce l’aggregazione di VDAC1, il tutto senza attivare le classiche vie di suicidio cellulare. Bloccare il poro interno impedisce al DNA di spostarsi dal nucleo mitocondriale nello spazio tra le membrane, mentre bloccare VDAC1 ne impedisce il passaggio attraverso il confine esterno nel citosol. Entrambi gli interventi riducono nettamente la quantità di DNA mitocondriale nel citosol, confermando una via di fuga graduale che dipende da VDAC1.
Dall’allarme interno alla morte cellulare infiammatoria
Il gruppo ha quindi chiesto se il DNA mitocondriale disperso fosse sufficiente ad attivare le difese dei cheratinociti. Quando hanno purificato questo DNA e lo hanno introdotto direttamente nei cheratinociti, ha attivato fortemente il sistema cGAS–STING — un rilevatore interno di DNA — e un altro complesso chiamato inflammasoma. Questi circuiti insieme hanno indotto alti livelli di interferoni e chemiochine e hanno spinto le cellule verso la piroptosi, una forma esplosiva e infiammatoria di morte cellulare che provoca fori nella membrana cellulare. Bloccare cGAS ha attenuato queste risposte e ridotto la piroptosi, mostrando che questa via di rilevamento del DNA è a monte di gran parte della cascata infiammatoria. 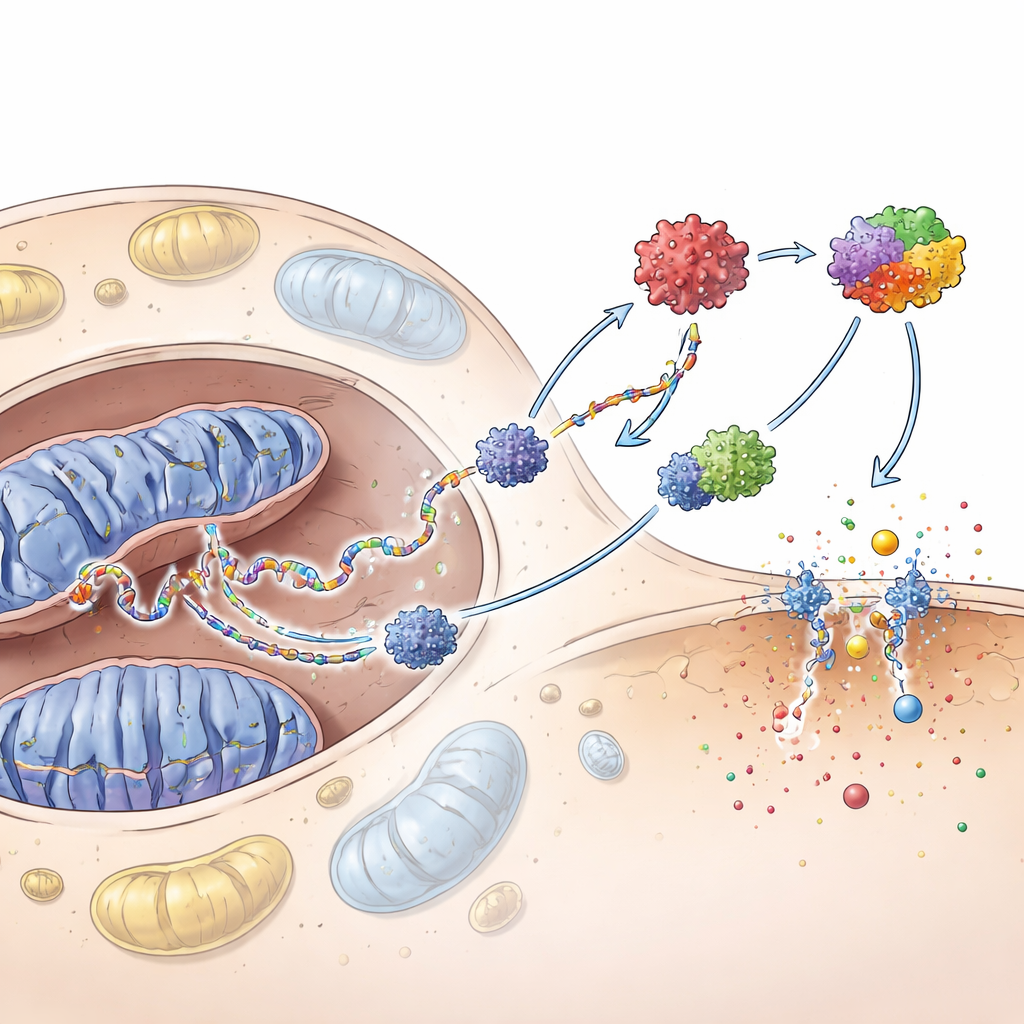
Chiudere il cancello per calmare la pelle
Poiché VDAC1 agisce come un cancello esterno chiave per la fuga del DNA, i ricercatori hanno testato se chiudere questo cancello potesse attenuare i segni della malattia. in coltura cellulare, una piccola molecola chiamata VBIT‑4, che impedisce l’aggregazione di VDAC1, ha ridotto il rilascio di DNA mitocondriale e smorzato l’attivazione sia di cGAS–STING sia dell’inflammasoma, abbassando la produzione di chemiochine. Anche il silenziamento del gene VDAC1 ha prodotto effetti simili. In un modello murino di vitiligine indotta dall’applicazione cutanea di perossido d’idrogeno, gli animali trattati con VBIT‑4 hanno sviluppato meno chiazze pallide, hanno mantenuto più melanociti e hanno mostrato meno cellule CD8⁺ nella pelle. La loro cute ha anche mostrato livelli inferiori dei percorsi infiammatori collegati al DNA mitocondriale.
Un nuovo modo per intercettare precocemente la vitiligine
Per un non specialista, la conclusione è che le normali cellule della pelle non restano semplicemente a guardare mentre il sistema immunitario va fuori controllo: aiutano a scatenare il problema. Sotto stress chimico, i loro mitocondri perdono frammenti di DNA attraverso i “cancelli” VDAC1, e questo DNA fuoriuscito funge da falso allarme di infezione. Quell’allarme risveglia potenti programmi antivirali e infiammatori, richiama cellule immunitarie aggressive e favorisce forme distruttive di morte cellulare, preparando il terreno per la perdita di pigmento. Mirando al cancello VDAC1, farmaci come VBIT‑4 potrebbero un giorno placare questo allarme alla sua fonte, offrendo un modo per rallentare o prevenire la vitiligine prima che si verifichi un danno permanente alle cellule produttrici di pigmento.
Citazione: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
Parole chiave: vitiligine, DNA mitocondriale, cheratinociti, immunità innata, VDAC1