Clear Sky Science · es
Liberación de ADN mitocondrial vía VDAC1 en queratinocitos: un impulsor clave de la inmunidad innata y la patogenia del vitíligo
Por qué importa esta historia cutánea
Las manchas blancas de la piel causadas por el vitíligo pueden ser profundamente angustiosas, y sin embargo los tratamientos actuales a menudo funcionan solo parcialmente y las recaídas son frecuentes. Este estudio profundiza en un culpable sorprendente dentro de las células cutáneas comunes: unas pequeñas centrales energéticas llamadas mitocondrias. Los autores muestran cómo el estrés dentro de estas estructuras puede desencadenar una señal de alarma que activa el sistema inmunitario y contribuye a la pérdida del color de la piel. Al trazar esta cadena de sucesos paso a paso, también señalan un nuevo tipo de terapia que no se dirige al sistema inmunitario en sí, sino a la forma en que las células de la piel piden ayuda en primer lugar.
Las células de la piel como emisoras activas de alarma
El vitíligo se ha visto durante mucho tiempo como una enfermedad en la que las células inmunitarias atacan por error a las células productoras de pigmento, llamadas melanocitos. Sin embargo, las células más externas de la piel—los queratinocitos—superan en número a los melanocitos y se reconocen cada vez más como centinelas tempranos en la enfermedad. En personas con vitíligo, la piel sufre un alto “estrés oxidativo”, una tensión química similar a la que ocurre bajo luz solar intensa o contaminación. Los queratinocitos bajo esta tensión liberan mensajeros inflamatorios que atraen células T citotóxicas a la piel. La pregunta clave que plantean los autores es: ¿qué convierte exactamente este estrés químico en una señal de peligro poderosa que activa la maquinaria antiviral e inflamatoria del cuerpo?
Centralitas que también hacen de balizas de advertencia
Las mitocondrias contienen sus propios pequeños anillos de material genético, el ADN mitocondrial. Cuando este ADN escapa al cuerpo principal de la célula, el sistema inmunitario a menudo lo trata como si fuera viral o bacteriano. Los investigadores muestran que exponer queratinocitos a peróxido de hidrógeno—un agente clásico de estrés oxidativo—daña las mitocondrias sin matar las células de inmediato. Bajo el microscopio, la estructura mitocondrial se distorsiona y fragmentos de ADN mitocondrial aparecen fuera del orgánulo mientras que la cantidad total de ADN mitocondrial dentro de la célula se mantiene aproximadamente constante. Este ADN filtrado activa entonces dos potentes sistemas sensores que normalmente protegen contra infecciones, conduciendo a la producción de interferones (proteínas que amplifican las respuestas inmunitarias) y quimiocinas (señales que reclutan células inmunitarias). 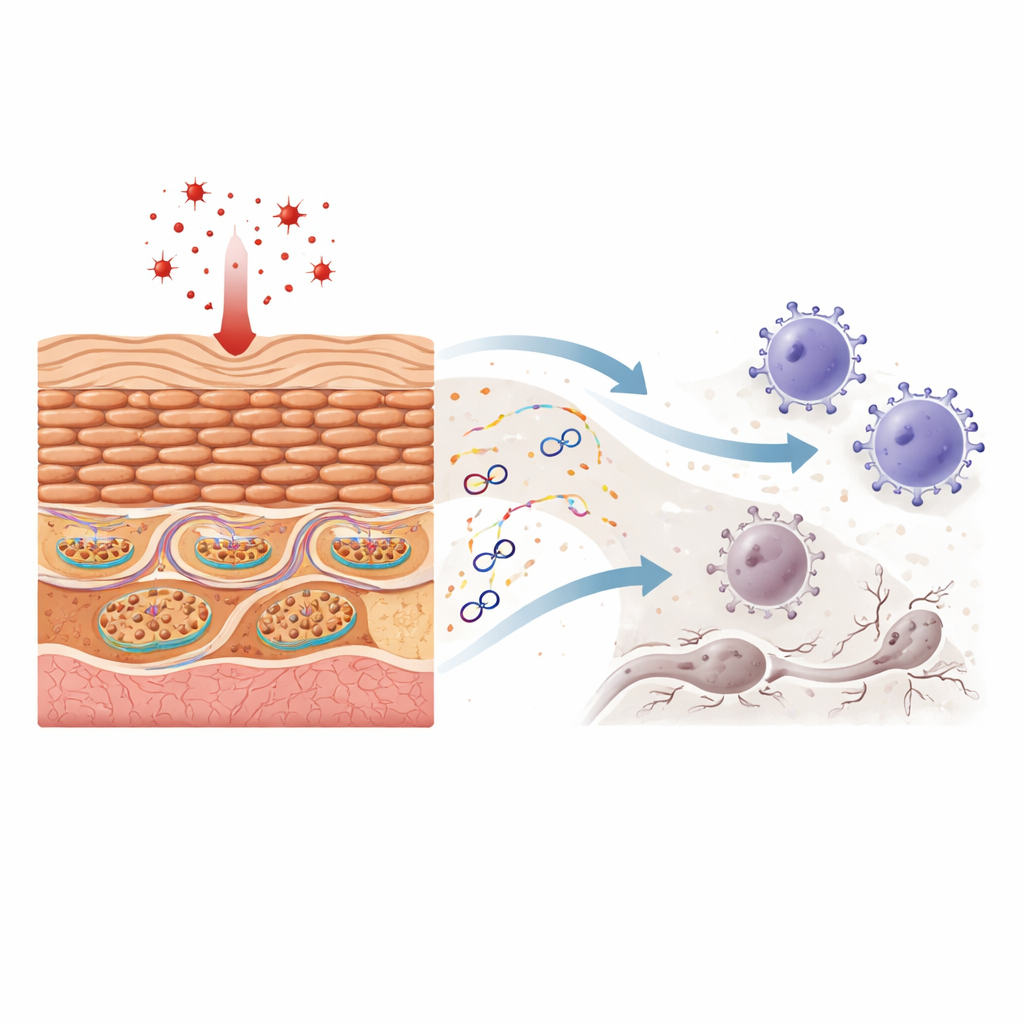
Cómo el ADN mitocondrial sale de su jaula
Para entender cómo sale este ADN, los autores se centran en dos puertas en las membranas mitocondriales. Una es el poro de transición de permeabilidad en la membrana interna, que puede abrirse bajo estrés. La otra es VDAC1, un canal en la membrana externa que puede agruparse en aberturas mayores. Usando colorantes en células vivas y sondas moleculares, muestran que el estrés oxidativo primero abre el poro interno y luego favorece la agregación de VDAC1, todo ello sin desencadenar las vías clásicas de suicidio celular. Bloquear el poro interno impide que el ADN se mueva desde el núcleo mitocondrial hacia el espacio entre membranas, mientras que bloquear VDAC1 impide que cruce el límite externo hacia el interior celular. Ambas intervenciones reducen drásticamente la cantidad de ADN mitocondrial en el citosol, confirmando una ruta de escape escalonada que depende de VDAC1.
De la alarma interna a una muerte celular inflamatoria
El equipo preguntó luego si el ADN mitocondrial errante es por sí solo suficiente para activar las defensas de los queratinocitos. Cuando purificaron este ADN y lo introdujeron directamente en queratinocitos, activó con fuerza el sistema cGAS–STING—un detector interno de ADN—y otro complejo llamado inflamasoma. En conjunto, estos circuitos promovieron altos niveles de interferones y quimiocinas y empujaron a las células hacia la piroptosis, una forma explosiva e inflamatoria de muerte celular que perfora la membrana celular. Bloquear cGAS atenuó estas respuestas y redujo la piroptosis, mostrando que esta vía de detección de ADN se sitúa aguas arriba de gran parte de la cascada inflamatoria. 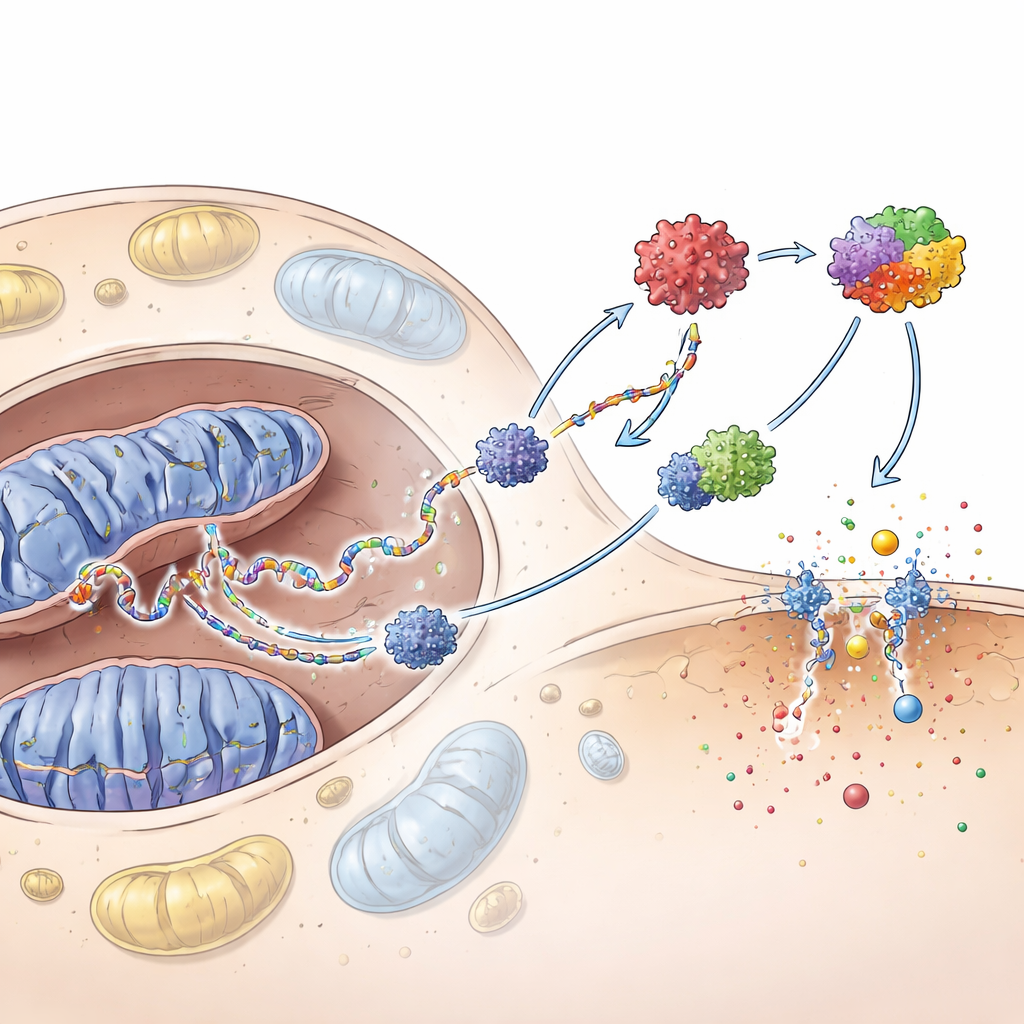
Cerrar la puerta para calmar la piel
Puesto que VDAC1 actúa como una puerta exterior clave para la fuga de ADN, los investigadores probaron si cerrar esta puerta podría aliviar los signos de la enfermedad. En cultivo celular, una molécula pequeña llamada VBIT‑4, que evita la agregación de VDAC1, redujo la liberación de ADN mitocondrial y atenuó la activación tanto de cGAS–STING como del inflamasoma, disminuyendo la producción de quimiocinas. Silenciar el gen VDAC1 tuvo efectos similares. En un modelo murino de vitíligo inducido por aplicación cutánea de peróxido de hidrógeno, los animales tratados con VBIT‑4 desarrollaron menos manchas pálidas, conservaron más melanocitos y mostraron menos células CD8⁺ en la piel. Su piel también mostró niveles más bajos de las vías inflamatorias vinculadas al ADN mitocondrial.
Una nueva forma de interceptar el vitíligo en sus inicios
Para un público no especialista, la conclusión es que las células cutáneas comunes no se limitan a observar mientras el sistema inmunitario se descontrola: contribuyen a iniciar el problema. Bajo estrés químico, sus mitocondrias filtran fragmentos de ADN a través de las “puertas” VDAC1, y ese ADN filtrado actúa como una falsa alarma de infección. Esa alarma despierta potentes programas antivirales e inflamatorios, atrae células inmunitarias agresivas y promueve formas destructivas de muerte celular, preparando el terreno para la pérdida de pigmento. Al dirigir la puerta VDAC1, fármacos como VBIT‑4 podrían algún día silenciar esta alarma en su origen, ofreciendo una forma de frenar o prevenir el vitíligo antes de que se produzca un daño duradero a las células pigmentarias.
Cita: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
Palabras clave: vitíligo, ADN mitocondrial, queratinocitos, inmunidad innata, VDAC1