Clear Sky Science · de
Freisetzung von mitochondrialer DNA über VDAC1 in Keratinozyten: ein zentraler Auslöser der angeborenen Immunität und der Pathogenese von Vitiligo
Warum diese Hautgeschichte wichtig ist
Weiße Hautflecken durch Vitiligo können stark belastend sein, und die derzeitigen Behandlungen wirken oft nur teilweise und Rückfälle sind häufig. Diese Studie geht einem unerwarteten Schuldigen in normalen Hautzellen nach: winzigen Kraftwerken, den Mitochondrien. Die Autoren zeigen, wie Stress in diesen Strukturen ein Alarmsignal auslösen kann, das das Immunsystem aktiviert und zum Verlust der Hautfarbe beiträgt. Indem sie diese Ereigniskette Schritt für Schritt nachzeichnen, deuten sie zugleich auf eine neue Therapieform hin, die nicht direkt das Immunsystem angreift, sondern darauf abzielt, wie Hautzellen überhaupt erst um Hilfe rufen.
Hautzellen als aktive Alarmsender
Vitiligo wurde lange als Erkrankung betrachtet, bei der Immunzellen fälschlich pigmentbildende Zellen, die Melanozyten, angreifen. Die äußersten Hautzellen – Keratinozyten – sind jedoch weitaus zahlreicher als Melanozyten und werden zunehmend als frühe Wächter der Erkrankung erkannt. Bei Menschen mit Vitiligo steht die Haut unter hohem „oxidativem Stress“, einer chemischen Belastung ähnlich der durch intensive Sonneneinstrahlung oder Umweltverschmutzung. Keratinozyten unter dieser Belastung setzen entzündliche Botenstoffe frei, die Killer-T-Zellen in die Haut locken. Die Kernfrage der Autoren ist: Was verwandelt genau diesen chemischen Stress in ein kräftiges Gefahrensignal, das die antiviralen und entzündlichen Mechanismen des Körpers einschaltet?
Kraftwerke, die zugleich Warnleuchten sind
Mitochondrien tragen eigene kleine Ringe genetischen Materials, die mitochondriale DNA. Wenn diese DNA in das Zellplasma entweicht, behandelt das Immunsystem sie oft, als stamme sie von Viren oder Bakterien. Die Forschenden zeigen, dass die Exposition von Keratinozyten gegenüber Wasserstoffperoxid – einem klassischen Oxidationsmittel – die Mitochondrien schädigt, ohne die Zellen unmittelbar abzutöten. Unter dem Mikroskop wird die mitochondriale Struktur verzerrt, und Stücke mitochondrialer DNA erscheinen außerhalb des Organells, während die Gesamtmenge an mitochondrialer DNA in der Zelle weitgehend konstant bleibt. Diese ausgelaufene DNA aktiviert dann zwei kraftvolle Sensorsysteme, die normalerweise vor Infektionen schützen, und führt zur Produktion von Interferonen (Proteine, die Immunreaktionen verstärken) und Chemokinen (Signale, die Immunzellen anlocken). 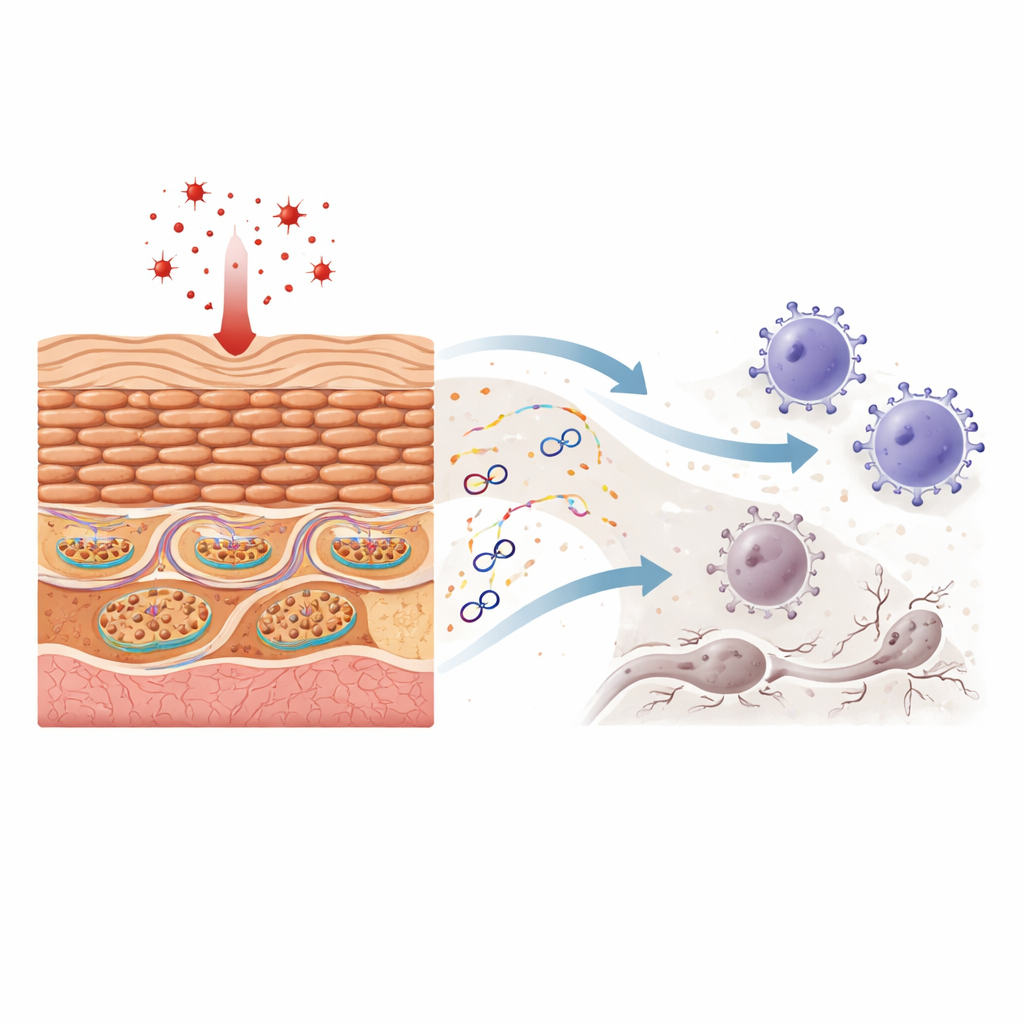
Wie mitochondriale DNA ihr Gefängnis verlässt
Um zu verstehen, wie diese DNA entkommt, konzentrieren sich die Autoren auf zwei Tore in den Mitochondrienmembranen. Eines ist der Permeabilitätsübergangspore in der inneren Membran, der unter Stress öffnen kann. Das andere ist VDAC1, ein Kanal in der äußeren Membran, der zu größeren Öffnungen klustern kann. Mithilfe von Farbstoffen für lebende Zellen und molekularen Sonden zeigen sie, dass oxidativer Stress zuerst die innere Pore öffnet und dann die Clusterbildung von VDAC1 fördert, und das alles ohne klassische Wege des programmierten Zelltods auszulösen. Das Blockieren der inneren Pore verhindert, dass DNA aus dem mitochondrialen Kern in den Intermembranraum gelangt, während das Blockieren von VDAC1 dessen Übertritt in das Zellinnere stoppt. Beide Interventionen verringern die Menge mitochondrialer DNA im Zytosol deutlich und bestätigen damit einen schrittweisen Fluchtweg, der von VDAC1 abhängt.
Vom internen Alarm zum feurigen Zelltod
Das Team fragte dann, ob die herumirrende mitochondriale DNA allein ausreicht, um die Abwehrmechanismen der Keratinozyten zu aktivieren. Als sie diese DNA reinigten und direkt in Keratinozyten einbrachten, aktivierte sie stark das cGAS–STING-System – einen internen DNA-Detektor – sowie einen weiteren Komplex, das Inflammasom. Zusammen trieben diese Schaltkreise hohe Spiegel an Interferonen und Chemokinen und trieben die Zellen in Pyroptose, eine explosive, entzündliche Form des Zelltods, die Löcher in die Zellmembran sticht. Das Blockieren von cGAS dämpfte diese Reaktionen und verringerte die Pyroptose, was zeigt, dass dieser DNA-Sensorweg dem Großteil der entzündlichen Kaskade vorgelagert ist. 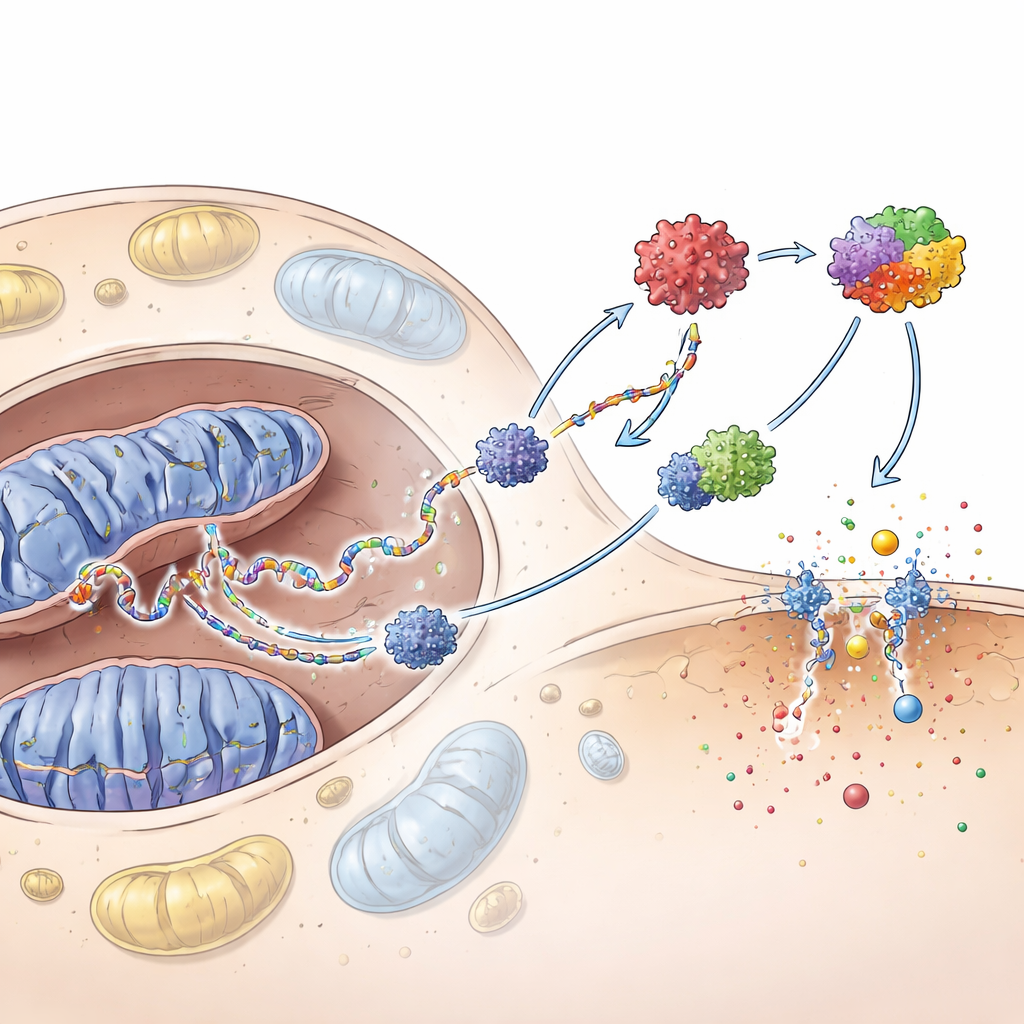
Das Tor schließen, um die Haut zu beruhigen
Da VDAC1 als wichtiges äußeres Tor für den DNA-Austritt fungiert, prüften die Forschenden, ob das Schließen dieses Tores die Krankheitszeichen lindern könnte. In Zellkultur verringerte ein kleines Molekül namens VBIT‑4, das die Clusterbildung von VDAC1 verhindert, die Freisetzung mitochondrialer DNA und dämpfte die Aktivierung von sowohl cGAS–STING als auch des Inflammasoms, wodurch die Chemokinproduktion sank. Die Stilllegung des VDAC1-Gens zeigte ähnliche Effekte. In einem Mausmodell von Vitiligo, ausgelöst durch lokal aufgetragenes Wasserstoffperoxid, entwickelten mit VBIT‑4 behandelte Tiere weniger blasse Flecken, behielten mehr Melanozyten und zeigten weniger CD8⁺-T-Zellen in der Haut. Ihre Haut wies zudem geringere Aktivität der mit mitochondrialer DNA verknüpften Entzündungswege auf.
Ein neuer Weg, Vitiligo früh abzufangen
Für Nichtfachleute lautet die Quintessenz: Normale Hautzellen sitzen nicht passiv da, während das Immunsystem außer Kontrolle gerät – sie tragen zur Entstehung des Problems bei. Unter chemischem Stress lecken ihre Mitochondrien DNA-Stücke durch VDAC1-„Tore“ aus, und diese ausgelaufene DNA wirkt wie ein falscher Infektionsalarm. Dieser Alarm weckt starke antivirale und entzündliche Programme, lockt aggressive Immunzellen an und begünstigt zerstörerische Formen des Zelltods, die den Boden für Pigmentverlust bereiten. Indem man das VDAC1-Tor anvisiert, könnten Medikamente wie VBIT‑4 eines Tages diese Alarmmeldung an der Quelle beruhigen und so helfen, Vitiligo zu verlangsamen oder zu verhindern, bevor dauerhafter Schaden an den Pigmentzellen entsteht.
Zitation: Lv, J., Xu, W., Jiang, P. et al. Mitochondrial DNA release via VDAC1 in keratinocytes: a key driver of innate immunity and vitiligo pathogenesis. Cell Death Dis 17, 318 (2026). https://doi.org/10.1038/s41419-026-08585-5
Schlüsselwörter: Vitiligo, mitochondriale DNA, Keratinozyten, angeborene Immunität, VDAC1